
- •Занятие 13. Углеводы. Олиго– и полисахариды.
- •Вопросы для самоподготовки к занятию
- •Литература:
- •Содержание лабораторного практикума
- •Задачи для самостоятельного решения
- •Занятие 14 природные -аминокислоты.
- •Вопросы для самоподготовки к занятию
- •Литература
- •1. Подготовить теоретический материал по вопросам для самоподготовки к занятиям.
- •2. Оформить протокол лабораторной работы.
- •2. Напишите схемы реакций, обозначьте графически действующие реакционные центры, укажите, где возможно, тип и механизм реакций:
- •Содержание лабораторного практикума
- •Задачи для самостоятельного решения
- •Занятие 15. Пептиды и белки.
- •Вопросы для самоподготовки к занятию
- •Литература:
- •1. Подготовить теоретический материал по вопросам для самоподготовки к занятиям.
- •2. Оформить протокол лабораторной работы.
- •2. Напишите схемы реакций, обозначьте графически действующие реакционные центры, укажите, где возможно, тип и механизм реакций:
- •Содержание лабораторного практикума.
- •Задачи для самостоятельного решения
- •Занятие 16 нуклеиновые кислоты. Коллоквиум № 2 (модуль№3) «биополимеры и их структурные компоненты».
- •Вопросы для самоподготовки к занятию
- •Литература:
- •1. Подготовить теоретический материал по вопросам для самоподготовки к занятиям.
- •2. Оформить протокол лабораторной работы.
- •Содержание лабораторного практикума.
- •Задачи для самостоятельного решения
- •Сводные вопросы коллоквиума №2 (Модуль №3).
- •Занятие 17. Контроль практических навыков.
- •Уровень требований:
- •Перечень функциональных групп:
- •Методики выполнения общих качественных
- •Реакция идентификации многоатомных спиртов
- •Идентификация первичных и вторичных спиртов реакцией окисления бихроматом калия в кислой среде
- •Реакция идентификации фенольного гидроксида
- •2. Реакция “медного зеркала”
- •Б. Определение уксусного альдегида
- •Занятие 18. Липиды.
- •Вопросы для самоподготовки к занятию
- •Литература:
- •1. Подготовить теоретический материал по вопросам для самоподготовки к занятиям.
- •2. Оформить протокол лабораторной работы.
- •2. Напишите схемы реакций, обозначьте графически действующие реакционные центры, укажите, где возможно, тип и механизм реакций:
- •Содержание лабораторного практикума
- •Задачи для самостоятельного решения
- •Занятие 19. Некоторые природные и синтетические биологически активные соединения. Стероиды. Терпены. Терпеноиды.
- •Вопросы для самоподготовки
- •Литература:
- •1. Подготовить теоретический материал по вопросам для самоподготовки к занятиям.
- •2. Оформить протокол лабораторной работы.
- •2. Напишите схемы реакций, обозначьте графически действующие реакционные центры, укажите, где возможно, тип и механизм реакций:
- •Содержание лабораторного практикума
- •Задачи для самостоятельного решения
- •Сводные вопросы к теоретическому экзамену по биоорганической химии.
- •Теоретические основы строения и реакционной способности органических соединений.
- •II. Общие закономерности реакционной способности органических соединений как химическая основа их биологического функционирования.
- •III. Биополимеры и их структурные компоненты. Липиды.
Занятие 15. Пептиды и белки.
ЦЕЛЬ: Сформировать знания:
– принципов структурного построения пептидов и белков;
– первичной структуры пептидов и белков, методов ее определения;
– пространственной организации полипептидной цепи;
– кислотно-основных свойств и гидролиза пептидов;
– синтеза пептидов in vitro.
Cформировать умения:
– писать структуру ди- и трипептидов, используя знания формул -аминокислот;
– определять изоэлектрическую точку пептидов;
– изображать разные ионные формы пептидов в зависимости от рН среды;
– выполнять характерные и качественные реакции на пептиды и белки.
Вопросы для самоподготовки к занятию
Биологические функции пептидов и белков.
Принцип структурного построения пептидов и белков. Электронное строение и свойства пептидной связи.
Свойства пептидов. Изоэлектрическое состояние и изоэлектрическая точка пептидов, кислотный и щелочной гидролиз пептидов.
Первичная структура пептидов и белков. Определение аминокислотной последовательности по Эдману (фенилизотиоцианатный метод).
Синтез пептидов in vitro методом «активации» и «защиты» функциональных групп. Понятие о стратегии пептидного синтеза.
Вторичная структура пептидов и белков. Регулярные -спиральные и -структурные участки полипептидных цепей. Понятие о третичной и четвертичной структурах белков.
Понятие о сложных белках. Гемоглобин, строение, свойства, значение.
Литература:
[1]. Тюкавкина Н.А., Биоорганическая химия. / Н.А.Тюкавкина, Ю.И. Бауков– М.: Медицина, 1991.– С. 344-377.
[2]. Гидранович Л.Г. Биоорганическая химия: Учеб. пособие. /Л.Г.Гидранович. – Витебск: ВГМУ, 2009.– С. 230-262.
[3]. Гидранович Л.Г. Лабораторные занятия по биоорганической химии.: Учеб. пособие / Л.Г.Гидранович. – Витебск: ВГМУ, 2012.– С.107-113.
[4]. Гидранович Л.Г. Курс лекций по биоорганической химии.– Витебск.– 2003.– С. 197-210.
ЗАДАНИЯ ДЛЯ КОНТРОЛЯ САМОПОДГОТОВКИ К ЗАНЯТИЮ.
1. Подготовить теоретический материал по вопросам для самоподготовки к занятиям.
2. Оформить протокол лабораторной работы.
3. Решить задачи 1-6,9,14, представленные на страницах 111-113 данного лабораторного практикума.
Примерный вариант заключительного контроля:
1. Напишите ионные формы дипептида Гис-Про при рН 1,0 и 7,5.
2. Напишите схемы реакций, обозначьте графически действующие реакционные центры, укажите, где возможно, тип и механизм реакций:

Содержание лабораторного практикума.
Опыт 1. Биуретовая реакция на пептидную связь.
В пробирку поместите 5-6 капель раствора яичного белка, добавьте равный объем 2 н раствора NaOH и по стенке добавьте 1-2 капли раствора сульфата меди (II). Наблюдается появление красно-фиолетовой окраски.
Возможная схема реакции:
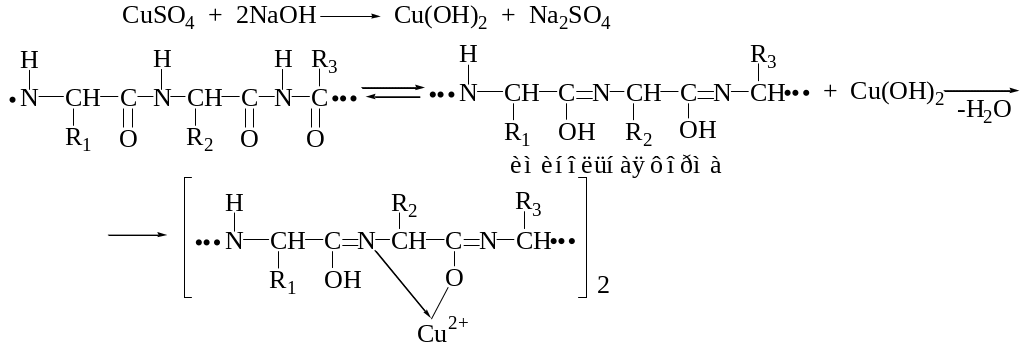
Вопросы:
1. С какой целью может быть использована данная реакция в качественном анализе?
2. Могут ли дать положительную биуретовую реакцию –аминокислоты?
Опыт 2. Ксантопротеиновая реакция белков.
В пробирку поместите 5 капель раствора яичного белка и 2 капли концентрированной азотной кислоты. Содержимое пробирку осторожно нагрейте, все время встряхивая. Раствор и осадок окрашиваются в желтый цвет. Охладив пробирку, осторожно добавьте 1-3 капли 2н раствора гидроксида натрия до появления ярко-оранжевой окраски.
Схема реакции:
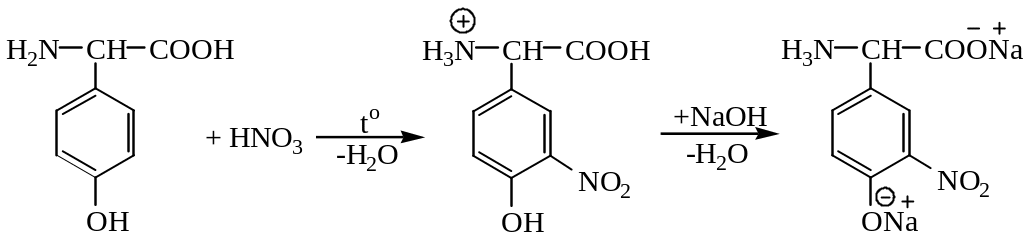
Вопросы:
1.Объясните ориентацию NO2 в бензольное кольцо.
2. Укажите тип и механизм реакции нитрования.
3. С какой целью может быть использована данная реакция в качественном анализе?
Опыт 3. Реакция на присутствие серосодержащих -аминокислот.
В пробирку поместите 5 капель раствора яичного белка и вдвое больший объем 2н раствора NaOH. Содержимое пробирки перемешайте, нагрейте до кипения (1-2 мин). К полученному щелочному раствору добавьте 5 капель 10% ацетата свинца (П) и вновь прокипятите. Отметьте появление серо-черного осадка.
Схема реакции:

Вопросы:
1. По какому реакционному центру цистеина протекает данная реакция?
2. С какой целью может быть использована данная реакция в качественном анализе?
Опыт 4. Осаждение белков трихлоруксусной и сульфосалициловой кислотами.
К 5 каплям раствора белка добавьте 2 капли раствора сульфосалициловой кислоты. Повторите этот опыт с раствором трихлоруксусной кислоты. Выпадает осадок белка.
Вопросы:
1. Является ли обратимым процесс осаждения белков органическими кислотами?
2. Какие изменения протекают с белками в процессе денатурации?
Опыт 5. Осаждение белков дегидратирующими агентами.
В две пробирки поместите по 5 капель раствора яичного белка. В первую пробирку добавьте 10-15 капель этилового спирта, во вторую-столько же ацетона. Выпадает осадок белка.
Вопросы:
1. Является ли процесс денатурации под действием ацетона и спирта обратимым?
2. Какие изменения в степени гидратации белка наблюдаются под влиянием ацетона и спирта?
