
- •4.Выделение н-парафиновых углеводородов из нефтяных фракций с помощью цеолитов. Целевые направленности процесса. Характеристика стадий гидроочистки сырья, адсорбции и десорбции н-парафинов
- •1). Адсорбционное разделение при изомеризации
- •3). Депарафинизация бензина и кгф с целью получения н-парафинов (для нхс) и кондиционного топлива
- •6. Методы очистки выделенных из нефтяных фракций н-парафинов от примесей ароматических углеводородов Методы очистки выделенных из нефтяных фракций н-парафинов от примесей ароматических углеводородов.
- •7.Производство изопарафиновых углеводородов каталитической изомеризацией н-парафинов. Химизм и механизм изомеризации. Промышленные процессы и их основные показатели.
- •8. Технологическая схема процесса изомеризации н-бутана «Бутамер». Технологическая схема процесса изомеризации пентан-гексановой фракции фирмы British Petroleum.
- •11.Получение циклогексана каталитическим гидрированием бензола. Химизм и термодинамика процесса. Типы используемых катализаторов, требования к сырью.
- •12.Условия, показатели и технология процессов гидрирования бензола в циклогексан. Типы реакторов, методы теплоотвода. Схема гидрирования бензола в циклогексан в трубчатом реакторе.
- •Металлические катализаторы.
- •Сульфидные катализаторы
- •Технология
- •13. Схема процесса производства цг фирмы Atlantic Richfield. Схема гидрирования бензола в цг с рециркуляцией цг.
- •14. Схема гидрирования бензола в циклогексан с отводом тепла реакции поддувом циркулирующего газа.
- •15.Приципиальная технологическая схема установки по производству циклогексана по методу фин. Схема процесса пр-ва цг, разработанного фирмой Haines Associates.
- •20. Производство высших линейных олефинов каталитическим дегидрированием н-парафинов (химизм, термодинамика, условия и особенности технологии процесса). Процесс «Пакол-Олекс» фирмы uop.
- •21. Технологическая схема процесса «Пакол-Олекс».
- •22. Получение высших линейных а-олефинов каталитической олигомеризацией этилена в присутствии катализаторов Циглера. Химизм, технология, условия и показатели процессов.
- •23. Схема «Альфрен» с рециркуляцией AlR3. Схема производства линейных а-олефинов с чётным числом углеродных атомов методом фирмы Gulf Research.
- •24.Получение высших линейных а-олефинов олигомеризацией этилена в присутствии комплексных металлоорганических катализаторов. Условия и технология процесса.
- •25. Схема получения высших линейных а-олефинов низкотемпературной олигомеризацией этилена методом фирмы Mitsui Petrochemical.
- •26.Получение высших линейных а-олефинов и олефинов нормального строения с внутренним положением двойных связей методом фирмы Shell (схема с блоками изомеризации и диспропорционирования олефинов).
- •30.Технологическая схема дегидрирования этилбензола(1). Технологическая схема дегидрирования изопропилбензола(2).
- •1) Рис. 120. Техн схема производства стирола. Аппараты :
- •2) Рис. 86. Техн схема производства альфа-метилстирола. Аппараты :
- •31. Принципиальные схемы разделения катализатов дегидрирования эб и ипб.
- •31. Применение стирола и альфа-метилстирола
- •35. Разделение ароматических углеводородов с6-с8. Проблемы разделения фракции с8. Выделение п-ксилола методами фракционной кристаллизации и адсорбции цеолитами..
- •37Схема фракционной кристаллизации. Рис. 5.25.
- •36. Поточная схема производства и разделения ароматики.
- •1)Процесс фирмы ici
- •39.Процесс «xis» (включая его технологическую схему).
- •40.Изомеризация алкилароматических углеводородов. Процесс «Octafming» (условия,, показатели, технологическая схема). Процесс «Isomar».
- •42.Катализаторы, условия и показатели процесса каталитического гидродеалкилирования толуола (и ксилолов). Технология гидродеалкилирования. Типы реакторов, способы теплоотвода.
- •43 Схема уст термического гда толуола по методу фирмы Мицубиси Схема процесса кат гидродеалкилирования толуола
- •44.Гидродеалкилирование бензина пиролиза. Схема переработки пиролизного бензина с получением ароматических углеводородов.
- •46 Схема установки гда бензина пиролиза (had)
- •48.Показатели процессов термического и каталитического гидродеалкилирования алкилнафталинов. Схема процесса «Юнидак». Схема полочного реактора и температурная кривая гидродеалкилирования.
- •49.Производство бензола и нафталина конверсией водяным паром соответствующих алкилароматических углеводородов (химизм, катализаторы, условия и показатели процессов).
- •49.Производство бензола и нафталина конверсией водяным паром соответствующих алкилароматических углеводородов (химизм, катализаторы, условия и показатели процессов).
- •50.Каталитическое диспропорционирование алкилароматических углеводородов. Химизм, катализаторы, условия, технология и показатели процессов диспропорционирования толуола.
- •53.Условия, технология и показатели процесса алкилирования бензола пропиленом в присутствии а1с1з.
- •54. Принципиальная схема алкилирования бензола пропиленом. Общий вид алкилатора. Схема разделения алкилата.
- •55.Получение изопропилбензола алкилированием бензола пропиленом на твердом фосфорнокислотном катализаторе. Условия, технология, показатели, преимущества и недостатки процесса.
- •57.Производство высших алкилбензолов алкилированием бензола высшими олефинами (или высшими хлорпарафинами). Условия, технология и показатели процесса. Схема разделения алкилата.
- •58. Основные направления химической переработки ароматики
- •Инициирование
- •Продолжение цепи
- •Вырожденное разветвление
- •Обрыв цепи
- •68. Технология (типы реакторов, способы отвода тепла), условия, показатели стадии окисления ипб в гп ипб. Способы разделения оксидата.
- •70. Технологическая схема стадии окисления ипб и кислотного разложения гп ипб.Применение гп ипб, фенола и ацетона.
- •71. Получение бензойной кислоты жидкофазным окислением толуола. Химизм, механизм, условия и показатели процесса. Технологическая схема производства бензойной кислоты окислением толуола.
- •72. Жидкофазное окисление п-ксилола в терефталевую кислоту. Химизм, катализаторы, условия, технология и показатели двухстадийного совмещённого процесса.
- •73. Окисление циклогексана в смесь циклогексанона и циклогексанола в присутствии солей кобальта. Химизм, условия, технология и показатели процесса. Применение циклогексанона.
- •73.(Продолжение) Окисление циклогексана в смесь циклогексанола и циклогексанона в присутствии борной кислоты. Химизм, условия, технология и показатели процесса.
- •74. Окисление циклогексана в адипиновую кислоту. Химизм, катализаторы, условия, технология и показатели второй стадии двухстадийного процесса.
- •75. Газофазное окисление нафталина и о-ксилола во фталевый ангидрид. Химизм, катализаторы, условия, показатели, технология.
- •76. Газофазное окисление бензола в малеиновый ангидрида. Химизм, катализаторы, условия, показатели, тезнология.
- •77. Производство вжс каталитическим гидрированием сжк и их эфиров.
- •78. Технология гидрирования эфиров сжк. Стадии промышленного процесса. Принципиальная технологическая схема гидрирования метиловых эфиров сжк в реакторах со стационарным слоем катализатора.
- •79. Технологическая схема прямого гидрирования сжк в высшие спирты в суспендированном слое.
- •81. Выделение вжс из вторых неомыляемых производства сжк. Сырьевая база. Методы выделения и их сущность. Условия и показатели процесса.
- •83. Производство вжс алюминийорганическим синтезом. Стадии промышленного процесса. Их химизм, условия, технология, показатели.
- •1. Синтез триалкилалюминия осуществляется 3 способами:
- •84. Поточная схема получения вжс алюминийорганическим синтезом. Применение вжс.
- •85. Структура молекул пав
- •86. Физико-химич основы и мех-м действия пав и Моющ вешеств
- •88. Схема пр-ва Сульфонола нп-3
- •90. Схема получения альфа-олефинсульфонатов.
- •97. Технологическая схема получения алкилсульфонатов натрия сульфоокислением н-парафинов.
- •98. Схема производства вторичных алкилсульфатов натрия
- •99. Схема сульфатирования спиртов или сульфирования алкилбензолов фирмы Balestra.
Инициирование
С 6H5
– СН(СН3)2
+ О2
+ С6H5CH(CH3)2
C6H5C(CH3)2
+ H2O2
+ C6H5C(CH3)2
(1)
6H5
– СН(СН3)2
+ О2
+ С6H5CH(CH3)2
C6H5C(CH3)2
+ H2O2
+ C6H5C(CH3)2
(1)
Продолжение цепи
 CH3
CH3
С
 6H5С(СH3)2
+
O2
C6H5COO
(2)
6H5С(СH3)2
+
O2
C6H5COO
(2)
CH3
Гидропероксид образуется в результате взаимодействия пероксирадикала с исходным ИПБ
CH3 CH3
C6H5 COO + C6H5CH(CH3)2 C6H5 COOH +C6H5C(CH3)2 (3)
CH3 CH3
Пероксирадикал может параллельно распадаться с образованием ацетофенона
CH3
С 6H5COO C6H5COCH3 + CH3O (4)
CH3
Образующийся метоксирадикал взаимодействует с ИПБ
С H3O + C6H5CH(CH3)2 CH3OH + C6H5C(CH3)2 (5)
Метиловый спирт обычно окисляется дальше
CH3OH O2 CH2O O2 HCOOH O2 CO2 + H2O
Вырожденное разветвление
Разветвление цепи происходит в результате термического распада гидроперекиси
 CH3
CH3
CH3
CH3
С 6H5COOH C6H5CO + OH (6)
CH3 CH3
 CH3
CH3
CH3
CH3
C 6H5CO + C6H5CH(CH3)2 C6H5COH + C6H5C(CH3)2 (7)
CH3 CH3
Образуется диметилфенилкарбинол – основной побочный продукт процесса.
OH + C6H5CH(CH3)2 H2O + C6H5C(CH3)2 (8)
Образовавшийся радикал может взаимодействовать с гидропероксидом

 CH3
CH3
CH3
CH3
CH3
CH3
С

 6H5C(CH3)2
+ C6H5COOH
C6H5COH
+ C6H5CO
(9)
6H5C(CH3)2
+ C6H5COOH
C6H5COH
+ C6H5CO
(9)
CH3 CH3 CH3
Реакция (9) – один из основных маршрутов образования диметилфенилкарбинола.
Кроме того, возможна еще следующая реакция
CH3
С 6H5CO C6H5COCH3 + CH3 (10)
CH3
Обрыв цепи
CH3 CH3
2 С6H5C(CH3)2 C6H5C CC6H5 (11)
CH3 CH3
CH3 CH3 CH3
2C6H5COO C6H5COOCC6H5 + O2 (12)
CH3 CH3 CH3
Большое влияние на обрыв цепи и на скорость окисления могут оказывать ингибиторы. Ингибиторами являются кислые продукты, например HCOOH, фенол, сернистые и ненасыщенные соединения.
68. Технология (типы реакторов, способы отвода тепла), условия, показатели стадии окисления ипб в гп ипб. Способы разделения оксидата.
В промышленных условиях инициатором процесса окисления может служить сам гидропероксид ИПБ. Его концентрация в исходной смеси обычно составляет 2,5-5%. Окисление проводят в гомогенной среде при след условиях:
Температура, оС … 110-130
Давление, МПа …. 0,29-0,49
Скорость окисления 5-7% гидропероксида в час
В процессе окисления по мере накопления гидропероксида начинается частичный его распад, который становится особенно заметным при содержании гидропероксида в реакционной массе ~ 18 % и более. Поскольку распаду гидропероксида способствует повышенная температура, очень важно, чтобы в конце зоны реакции температура не превышала 110—120 °С. При высоких температурах может идти распад гидропероксида со взрывом. Количество продуктов распада колеблется от 0,5 до 5 % (в зависимости от условий окисления и конечной концентрации гидропероксида).
Для окисления изопропилбензола применяют реакторы следующих типов;
реакторы колонного типа;
реакторы с перемешивающим устройством;
реакторы эрлифтного типа.
Р еактор
колонного типа
представляет
собой секционированную
колонну с барботажными
тарелками.
На
каждой тарелке
расположен змеевик водяного
охлаждения для отвода теплоты
реакции, составляющей около 1970
кДж на 1 кг превращенного изопропилбензола.
Изопропилбензол подается на верхнюю
тарелку и по
сливным трубам перетекает на нижележащие
тарелки. Воздух поступает
под нижнюю тарелку и поднимается
вверх, барботируя через
слой жидкости на каждой тарелке.
Температуру на каждой тарелке
регулируют подачей воды в змеевик.
Число секций окисления достигает
8—9.
еактор
колонного типа
представляет
собой секционированную
колонну с барботажными
тарелками.
На
каждой тарелке
расположен змеевик водяного
охлаждения для отвода теплоты
реакции, составляющей около 1970
кДж на 1 кг превращенного изопропилбензола.
Изопропилбензол подается на верхнюю
тарелку и по
сливным трубам перетекает на нижележащие
тарелки. Воздух поступает
под нижнюю тарелку и поднимается
вверх, барботируя через
слой жидкости на каждой тарелке.
Температуру на каждой тарелке
регулируют подачей воды в змеевик.
Число секций окисления достигает
8—9.
Р еакторы
эрлифтного
типа.
Принцип
работы такого
реактора основан
на разности плотностей аэрированного
и
неаэрированного столбов
жидкости в реакторе, состоящем
из двух сообщающихся сосудов. В эрлифт
снизу подается
распыленный воздух, который барботирует
через слой жидкости
в виде мелких пузырьков. ИПБ поступает
в нижнюю
часть неаэрированного слоя. Благодаря
разности плотностей происходит
«выталкивание» более легкой жидкости
тяжелой. В эрлифте
происходит окисление изопропилбензола.
Реакционная масса
через верх эрлифта перетекает в
неаэрированный слой и выводится.
Отработанный воздух отделяется в верхней
части аппарата. Реакторы
эрлифтного типа также располагают в
виде каскада.
еакторы
эрлифтного
типа.
Принцип
работы такого
реактора основан
на разности плотностей аэрированного
и
неаэрированного столбов
жидкости в реакторе, состоящем
из двух сообщающихся сосудов. В эрлифт
снизу подается
распыленный воздух, который барботирует
через слой жидкости
в виде мелких пузырьков. ИПБ поступает
в нижнюю
часть неаэрированного слоя. Благодаря
разности плотностей происходит
«выталкивание» более легкой жидкости
тяжелой. В эрлифте
происходит окисление изопропилбензола.
Реакционная масса
через верх эрлифта перетекает в
неаэрированный слой и выводится.
Отработанный воздух отделяется в верхней
части аппарата. Реакторы
эрлифтного типа также располагают в
виде каскада.
Реакторы с перемешивающим устройством располагают в виде каскада. ИПБ поступает в первый реактор, далее реакционная масса последовательно перетекает из реактора в реактор, а воздух подастся ступенчато в каждый реактор.
Преимущество реактора колонного типа заключается в его компактности. Применение такого реактора позволяет регулировать работу только одного аппарата. Преимуществом каскада реакторов с перемешивающим устройством является простота их конструкции. Благодаря ступенчатой подаче воздуха легкие продукты распада—муравьиная кислота и формальдегид, являющиеся ингибиторами окисления, не попадают вместе с воздухом с последующих ступеней окисления па первые, как это происходит в противоточной колонне.
Выделение гидропероксида из реакционной массы должно осуществляться в очень мягких условиях (начинает разлагаться с заметной скоростью при 145 °С, причем разложение сопровождается саморазогреванием). Гидропероксид изопропилбензола может быть извлечен из реакционной массы окисления химическим или физическим методами.
В первом случае гидропероксид путем
обработки раствором едкого
натра превращают в твердую натриевую
соль
которую затем отфильтровывают. Для
удаления увлеченного осадком
маточного раствора соль промывают
легким растворителем или
растворяют в воде. Из водно-щелочного
раствора гидропероксид
выделяют в виде мутного маслянистого
слоя путем пропускания
через раствор диоксида углерода. Таким
путем получается 97—98%-ный
технический гидропероксид.
первом случае гидропероксид путем
обработки раствором едкого
натра превращают в твердую натриевую
соль
которую затем отфильтровывают. Для
удаления увлеченного осадком
маточного раствора соль промывают
легким растворителем или
растворяют в воде. Из водно-щелочного
раствора гидропероксид
выделяют в виде мутного маслянистого
слоя путем пропускания
через раствор диоксида углерода. Таким
путем получается 97—98%-ный
технический гидропероксид.
Физический метод выделения сводится к концентрированию гидропероксида перегонкой. Реакционная масса после окисления подвергается двухступенчатой ректификации в вакууме для отгонки не прореагировавшего изопропилбензола и воды (концентрированный гидропероксид содержит 90—93% основного вещества).
Технико-экономическое сравнение двух методов выделения гидропероксида изопропилбензола показало, что физический метод обладает бесспорными преимуществами.
Потоки I-Воздух, II-ИПБ, III- свежий ИПБ, IV-а-метилстирольная фрация на переработку, V-смола на переработку, VI-товарный ацетон, VII-углеводороды, VIII-товарный фенол, IX-смола на переработку.
Аппараты. 1-подогреватель воздуха, 2-окислительная колонна, 3-теплообменник, 4, 8, 10, 14, 16, 18, 20, 22-конденсаторы, 5-насосы, 6-отстойник, 7-емкость, 9-колонна концентрирования гидроперекиси, 11-реактор разложения ГП, 12-нейтрализатор, 13-колонна отгонки ацетона-сырца, 15-колона товарного ацетона, 17-колонна отгонки фенольного дстиллята, 19-колонна фенола-сырца, 21-колонна товарного фенола.
Свежий изопропилбензол вместе с возвратным изопропилбензолом и с добавкой некоторого количества реакционной массы окисления (для введения гидроперекиси) нагревается в теплообменнике 3 за счет тепла продуктов окисления до 110 °С и подается на верхнюю тарелку окислительной колонны 2. Сжатый воздух для окисления через паровой подогреватель /, где нагревается также до 110°С, поступает в нижнюю часть окислительной колонны 2.
Давление в колонне 2 поддерживается до 5кгс/см2 (0,49 Мн/м2), температура 110—120 °С. Для отвода тепла реакции на каждой тарелке колонны установлен змеевик водяного охлаждения, через который подается умягченная вода. Регулирование температуры в каждой секции осуществляется автоматически.
Газы из верхней части колонны 2 проходят конденсаторы 4, где конденсируются пары изопропилбензола, и конденсат через отстойник 6 возвращается на окисление.
Продукты окисления из нижней части колонны 2 проходят теплообменник 3, где охлаждаются до 60 °С, и направляются в вакуумперегонную колонну 9 для концентрирования гидроперекиси изопропилбензола. Вакуум создается пятиступенчатым паровым эжектором, кипятильник колонны обогревается водяным паром. Для предотвращения подъема температуры в кубе колонны предусмотрены автоматическое отключение подачи пара и дистанционная подача воды в кипятильник. Пары изопропилбензола из колонны 9 конденсируются в конденсаторе 8, откуда после нейтрализации муравьиной кислоты изопропилбензол через отстойник 6 возвращается на окисление.
Техническую гидроперекись направляют в реактор 11 на разложение. Туда же поступает катализатор (50%-ный раствор серной кислоты в ацетоне). Разложение осуществляют в избытке ацетона при 60 °С. Тепло реакции разложения гидроперекиси отводится путем частичного испарения ацетона. Пары ацетона .конденсируются в конденсаторе 10 и возвращаются в реактор 11,
Продукты разложения из реактора 11 подают на нейтрализацию в скрубберы 12, заполненные анионитом АН-1. Каждый скруббер работает 3 суток, после чего останавливается для регенерации анионита щелочью. Нейтрализованная реакционная масса из скрубберов 12 направляется на ректификацию. В ректификационной колонне 13 отгоняется ацетон-сырец, конденсирующийся в конденсаторе 14. Часть ацетона-сырца возвращается на орошение колонны 13, остальное поступает в колонну 15. В колонне 15 сверху отбирается товарный ацетон, а с одной из верхних тарелок — ацетон, подаваемый в реактор 11 для отвода тепла реакции. С низа колонны 15 отбирается ct-метилстирольная фракция.
Остаток из колонны 13 направляется в колонну 17, где отгоняется фенол с примесью более низкокипящих компонентов (изопропилбензол, а-метилстирол). Кубовый остаток выводится из системы, а пары после конденсации поступают в колонну 19. Сверху из колонны 19 отбирается углеводородная фракция, а снизу фенол-сырец, направляемый в колонну 21 для выделения товарного фенола.
Режим работы окислительной колонны 2 характеризуется снижением температуры по секциям (120-110°С). Такое распределение температур позволяет свести до минимума количество продуктов термического распада.
Режим работы колонн:
9 13 15 17 19 21
Давление, мм рт. ст.
верх..................................................................1—3 400 Атмосф. 100 100 100
низ........... ……………………………………….5—7 460 То же 160 160 160
Температура, °С
верх.....................................................................28 40 58 120 85 115
низ........... …………………………………………95 160 102-104 180 133 127
Кубовая жидкость из колонны 21 содержит ацетофенон, диме-тилфенилкарбинол, димер а-метилстирола и смолы.
В процессе образуется около 7% побочных'продуктов по отношению к продуктам основной реакции. Они получаются главным образом на стадии образования гидроперекиси. Состав побочных продуктов реакции (в %):
а-Метилстирол (15,7)Димер а-метилстирола и смолы (43) Ацетофенон (7,0)Кумилфенол (33,4) Диметилфешлкарбинол (0,9)
Применение ГП ИПБ.
Используется для получения фенола и ацетона.
Применение фенола и ацетона.
Фенола. Основная часть фенола (около 60—65%) перерабатывается в феноло-формальдегидные смолы, полиэпоксиды и поликарбонаты. Фенол служит исходным веществом для получение адипиновой кислоты и капролактама, идущих на изготовление синтетических волокон, неионогенных моющих средств, присадок к топливам и маслам, гербицидов, некоторых лекарственных веществ (аспирин и салол) и многих других химических продуктов.
69. Стадия кислотного разложения ГП ИПБ на фенол и ацетон. Химизм (основная и побочные реакции), механизм, условия, технология (в т. ч. типы реакторов, способы отвода теплоты реакции), показатели. Технологическая схема стадии кислотного разложения ГП ИПБ.
Под действием серной кислоты гидроперекись разлагается в основном на фенол и ацетон:
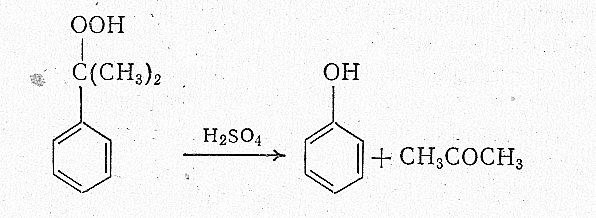
Предлагается следующий механизм этой реакции:
Образование оксониевого иона и его дегидратация:
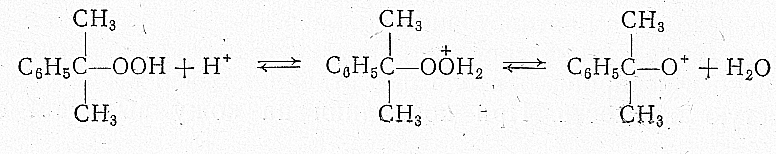
Перегруппировка образовавшегося иона с миграцией фениль-ной группы к кислородному атому:
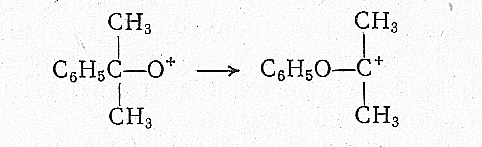
Взаимодействие иона карбония с молекулой гидроперекиси:
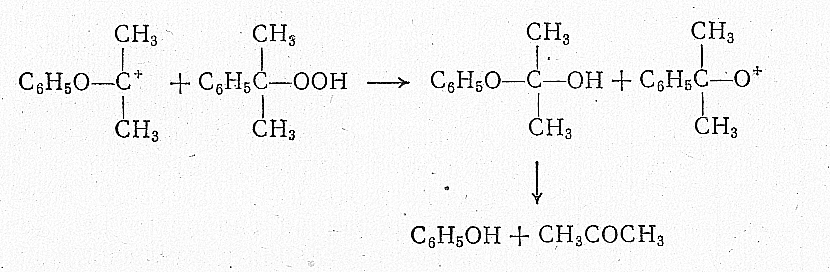
Техническая гидроперекись изопропилбензола содержит также небольшие количества диметилфенилкарбинола и ацетофенона, образовавшихся в результате ее термического распада. Из диметилфенилкарбинола далее могут образоваться сложный фенол (кумилфенол), а-метилстирол, димер а-метилстирола и смолистые вещества:
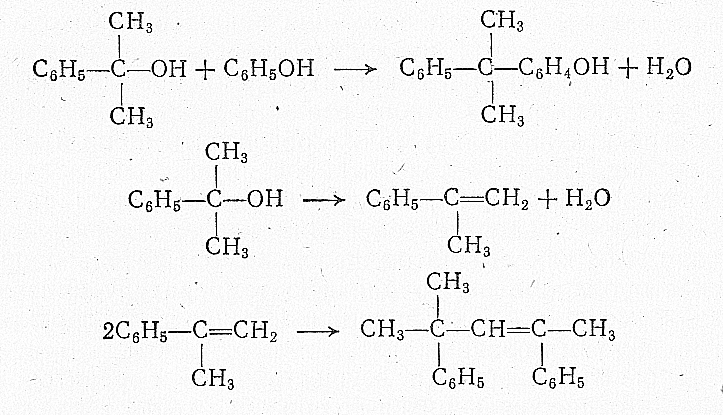
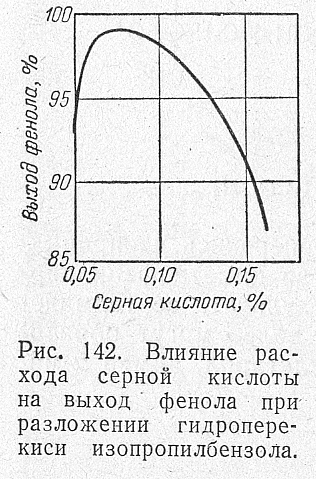
Слабые кислоты (щавелевая, метафосфорная) в количестве 2—3% от массы гидроперекиси действуют лишь при температурах 100—120°С и дают низкий выход фенола и ацетона. В промышленных условиях применяют 98%-ную серную кислоту в виде раствора в ацетоне. Максимальный выход целевых продуктов достигается при концентрации 0,07—0,1% H2 SO4 от массы гидроперекиси.
При повышении температуры с 50 до 80°С выход ацетона снижается с 98—99 до 89%, а фенола с 98 до 80—82% от теории. При более низких температурах (например, 30 °С) резко возрастает продолжительность реакции и остается, неразложившаяся гидроперекись. Оптимальная температура 50—60°С при времени контакта примерно 3,5 мин.
Технологическое оформление процесса разложения гидроперекиси изопропилбензола. Кислотное разложение ГП ИПБ протекает с выделением тепла в количестве 486 ккал (2080 кДж) на 1 кг гидроперекиси.
На разложение чаще всего поступает концентрированная ГП ИПБ (за исключением окисления в эмульсии, когда подается 25%-ная гидроперекись). Однако разложение концентрированной ГП ИПБ небезопасно, так как в случае повышения температуры в зоне реакции возможен неконтролируемый ГП, который вследствие мгновенного подъема давления может привести к взрыву. Кроме того, для понижения выхода побочных продуктов желательно понизить концентрацию ГП и сократить время пребывания фенола и диметилфенилкарбинола в зоне реакции. Понижение концентрации ГП позволяет также обеспечить полный распад ее за один проход. Поэтому концентрированную ГП разбавляют в зоне реакции каким-либо циркулирующим разбавителем. Разбавление ГП самим изопропилбензолом нецелесообразно, так как его потом необходимо тщательно очистить от а-метилстирола, имеющего близкую температуру кипения, что усложнило бы систему ректификации. Обычно ГП разбавляют продуктами реакции.
Разложение ГП осуществляется в реакторах двух типов, различающихся по способу отвода тепла реакции.
Работа реактора адиабатического типа (Л) основана на циркуляции реакционной массы или разбавителя (например, разбавленной серной кислоты) в системе реактор—холодильник— реактор. Часть тепла реакции воспринимается разбавителем, благодаря чему уменьшается перепад температур в реакторе. Количество циркулирующего разбавителя определяется допустимым подъемом температуры в реакторе и температурой разбавителя.
Более совершенный тип реактора изотермический (Б). В этом реакторе разложение гидроперекиси изопропилбензола осуществляется в избытке ацетона с отводом тепла реакции за счет испарения ацетона. Пары ацетона конденсируются в конденсаторе, и ацетон вновь стекает в реактор. Эта схема отвода тепла очень эффективна. Кроме того, разбавление ацетоном должно понижать выход побочных продуктов благодаря специфическому тормозящему действию ацетона на конденсацию фенола с диметилфенилкарбинолом. В реакторе адиабатического типа выход фенола составляет 93—95% и ацетона94—95% от теоретического, в реакторе изотермического типа выход фенола и ацетона может достигать 98% от теоретического.

