
- •1. Введение
- •Альберт Эйнштейн, 1935 г.
- •2. Первый закон термодинамики
- •3.Второй закон термодинамики
- •4. Фазовые переходы. Аллотропия
- •5.Водяной пар
- •6. Термодинамика открытых систем. Течение газов
- •7. Дросселирование газов и паров
- •8.Температура адиабатического торможения
- •9. Компрессоры. Детандеры
- •10.Циклы поршневых двигателей внутреннего сгорания (двс)
- •11. Циклы газотурбинных установок и реактивных двигателей
- •12. Циклы паротурбинных установок (пту)
- •13. Циклы холодильных установок
- •14. Цикл теплового насоса
- •1.Стационарные задачи теплопроводности твердых тел
- •2.Нестационарные задачи теплопроводности твердых тел
- •Tаблица 2. Расчетные выражения для составляющих формул (28,29).
- •3. Пути интенсификации теплопередачи
- •4.Конвективный теплообмен
- •5. Теплообмен излучением
- •6.Теплообменные аппараты
- •Раздел II. Лабораторные работы по разделу “Теплопередача” курса “Техническая термодинамика и теплопередача”.
- •Стационарный метод определения коэффициента теплопроводности материалов
- •4. Методические указания по выполнению работы
- •Работа № 2 нестационарный метод исследования тепловых свойств веществ
- •Метод регулярного теплового режима первого рода
- •Определение коэффициента температуропроводности
- •4. Методические указания по выполнению работы
- •Работа № 4 исследование условий теплообмена в термокамере
- •4. Методические указания по выполнению работы
- •5. Порядок выполнения работы
- •Литература
4. Фазовые переходы. Аллотропия
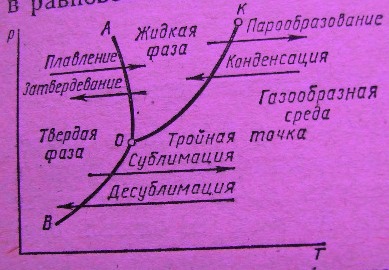 Агрегатные состояния чистого вещества
обычно имеют газообразную , жидкую и
твердую фазы. На рис. 4.1 изображены
линии фазовых переходов вещества.
Промежуточное состояние вещества
между жидкостью и газом называется
паром. Водяной пар – рабочее тело .
Агрегатные состояния чистого вещества
обычно имеют газообразную , жидкую и
твердую фазы. На рис. 4.1 изображены
линии фазовых переходов вещества.
Промежуточное состояние вещества
между жидкостью и газом называется
паром. Водяной пар – рабочее тело .
Линия ОА - кривая плавления ( затвердевания),
линия ОВ – кривая сублимации (десублимации),
линия ОК – кривая кипения (конденсации ) ,она оканчивается в точке К ,которую называют критической. Для воды это Ткр= 647К , tкр = 3740C и pкр =22,14 МПа = 221 кг/см2, выше точки К – только перегретый пар .(vкр = 0,0032 м3/кг, ρкр = 320кг/м3).
Состояние , в котором существуют три фазы , называется тройной точкой -точка О. Для воды это Т0 = 273,15К , t0 = 00C и p0 = 610 Па =0,0062 кг/см2. Рис.4.1. Диаграмма фазовых переходов.
Количество теплоты, погоглощаемой (или выделяющейся) при равновесном изотермическом переходе единицы вещества (1 кг.) из одной фазы в другую , называется удельной скрытой теплотой фазового перехода. Различают скрытые теплоты испарения и конденсации, плавления и затвердевания , сублимации (десублимации). Их значения приводятся в справочной литературе.
Некоторые вещества в твердом состоянии образуют несколько кристаллических модификаций (аллотропических модификаций). Например , алмаз при высоких температурах и давлениях превращается в графит ,но и наоборот – при определенных условиях из графита получается исскуственный алмаз. Его сейчас получают из жидкого углерода ( Т ≈ 4000К и р ≈104 МПа , 1атм ≈ 0,1 МПа ) охлаждением при высоких давлениях + катализаторы . Таким же образом в 1987г. исскуственно получен и борозан ВN (нитрид бора с натрием), более твердый , чем алмаз ( –при охлажении компонентов от Т =2500К , р= 105 атм .+ катализатор ). В твердой фазе лед воды имеет 6 различных модификаций, кроме основной первой ,но все они лежат в области выше 200 мПа и здесь не рассматриваются.
5.Водяной пар
Испарение воды – парообразование на свободной поверхности при температуре меньшей температуры кипения t < ts при данном давлении. Сушка – рабочее тело есть влажный воздух : сухой воздух плюс водяной пар (газовая смесь ). Содержание водяного пара в атмосфере зависит от метеорологических условий и от источников испарения воды (от малых долей до 4 % по массе).
Влажный воздух бывает двух типов : насыщенным и ненасыщенным (смесь сухого воздуха и насыщенного или перегретого водяного пара соответственно ). Температура , до которой надо охлаждать ненасыщенный влажный воздух, чтобы перегретый пар в нем стал насыщенным наз. температурой точки росы Тросы ( коалесценция туманов ). При дальнейшем охлаждении водяной пар конденсируется, точку Тросы часто используют, как меру содержания в воздухе воды в парообразном состоянии .
5.1. ПАРООБРАЗОВАНИЕ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ .
Кипение воды - интенсивное испарение не только на свободной поверхности , но и внутри нее образующихся пузырьков пара.
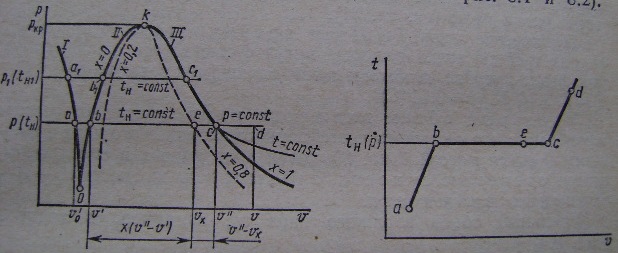
Рис.5.1. Процессы подогрева жидкости a-b , парообразования b-c ,перегрева c-d .
При подводе теплоты жидкость нагревается до температуры кипения tн , соответствующей давлению p , удельный объем незначительно возрастает от v/ 0 до v/ ( точка b ) . В изобарно – изотемическом процессе b-c кипящая жидкость полностью переходит в пар. Точка c –сухой насыщенный пар . Смесь жидкости и сухого насыщенного пара называют влажным паром (например ,точка e ).При подводе теплоты к сухому насыщенному пару его температура возрастает и он переходит в перегретый пар ( например , точка d ).В области перегретого пара изобара и изотерма разделяются ,изотерма идет ниже изобары (рис.5.1 ).
Для процессов
парообразования при давлениях р , р1
и т. д. состоянию жидкости при 00 С
соответствуют точки a
, a1
и т. д. , состоянию кипящей жидкости
–точки b, b1
и т. д. , состоянию сухого насыщенного
пара – точки с ,с1 и т. д. . При
соединении этих точек получаются
соответственно линии :изотермы жидкости
при 00 С; пограничная кривая жидкости
или нижняя (левая ) пограничная кривая;
пограничная кривая пара или верхняя (
правая ) пограничная кривая.
Пересечение пограничных кривых жидкости и пара в точке к дает критическую точку.Жидкость и ее насыщенный пар существуют только при температурах ниже критической .Выше критической точки есть только перегретый пар. Значение критической температуры Ткр ≈ 647К , tкр ≈ 374 0С при давлении pкр ≈22,1 МПа ≈225 атм.
Массовая доля пара x в смеси сухого насыщенного пара и жидкости называется степенью сухости , а массовая доля жидкости y =( 1 – x ) –степенью влажности .Степень сухости может изменяться от 0 до 1 .
5.2. ДИАГРАММЫ s-T и s-I ДЛЯ ВОДЯНОГО ПАРА
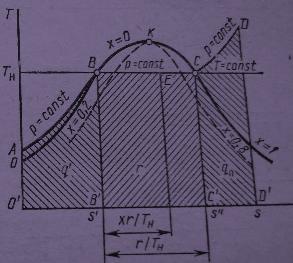 На рис.5.2 и рис. 5.3 представлены s-T
и s-i диаграммы
водяного пара , построенные по тем же
данным ,что и диаграмма v-p
(рис.5.1 ) , и с применением формул для
энтропии и энтальпии. ( Диаграмму
s –I предложил
использовать в 1904 году Молье ).
На рис.5.2 и рис. 5.3 представлены s-T
и s-i диаграммы
водяного пара , построенные по тем же
данным ,что и диаграмма v-p
(рис.5.1 ) , и с применением формул для
энтропии и энтальпии. ( Диаграмму
s –I предложил
использовать в 1904 году Молье ).
Точки А,В,Е,С,Д и К этих диаграмм соответствуют точкам a b e c d и к диаграммы v-p . Они определяют при давлении p состояния жидкости при t = 00C , кипящей жидкости при температуре насыщения tн , влажного пара , сухого насыщенного пара , перегретого пара и критическую точку к с tкр≈3740 С , pкр ≈225атм. .
Рис.5.2. Диаграмма s-T.
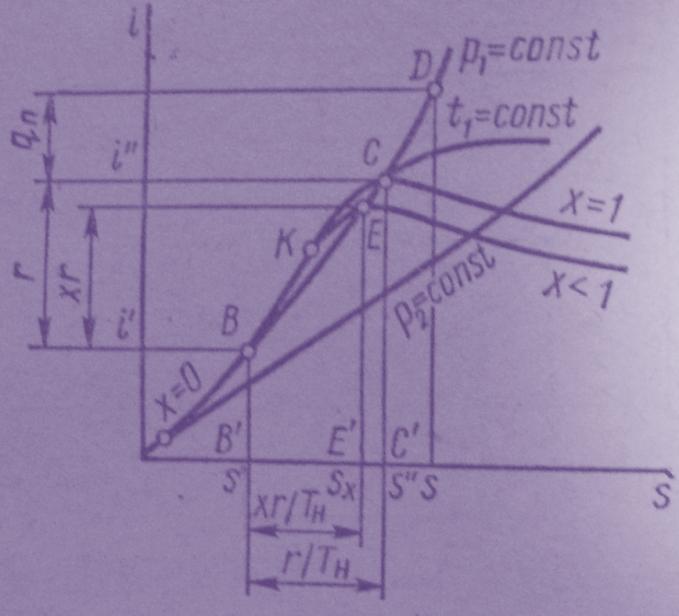
Следует заметить ,что критическая точка К на диаграмме s-I находится ниже её экстремального положения на диаграмме s-T. Видимо, поэтому и появились определения нижней и верхней пограничных кривых, взамен левой и правой.
Подогрев воды при р = const от 00 С до t0 C .
При постоянной теплоемкости с0= с/ =с
Рис.5.3. Диаграмма s-I.
q/ = c/ t =u/ = i/ , (u0/ = 0 ) …(5.1)
s/ = c/ ln( Tн/273 ) , (s0/ = 0) . …(5.2)
Парообразование .
Количество теплоты , затраченное на перевод кипящей жидкости в сухой насыщенный пар при постоянном давлении (процесс В-С ),называют теплотой парообразования и обозначают r .
r = (u// – u/) + p (v// - v / ) , …(5.3)
i// = i/ +r , …(5.4)
s// = s/ + r/Tн . …(5.5)
Для влажного пара при степени сухости x очевидны формулы
rx = xr , uX = u/ + x ( u// -u/ ) , ix =i/ +xr , sx = s/ +xr/Tн . … (5.6)
Перегрев пара . При подводе тепла к сухому насыщенному пару ( в точке С )получается перегретый пар(например,состояние в точке D ). Теплота перегрева при средней теплоемкости ср
qп = cp ( t – t н ) , а …(5.7)
i = i// + qп , u = i – pv , s = s// +cp ln(T/Tн ) . …(5.8),
* * *
На Рис.5.1 .-5.3. изображены
кривые ао , ок , кс (АО .ОК , КС ) ,
соответствующие реальным стабильным
процессам , т. наз. бинодали . Но
есть еще и кривые предельных метастабильных
(неустойчивых )состояний - т. наз.
спинодали . Они лежат слева ао
и внутри области окс , отличаясь
на (5 – 10)%. Между бинодалями и спинодалями
– область неустойчивых состояний, за
их границы выхода нет . Например,
при cтрого p≡const
, q ≡const
переохлаждение или перегрев воды, когда
при нормальных физических условиях она
обращается в лед при ≈-200С и
закипает при
 +1200С
( хотя бы малейший толчок – и они
становятся обычными в практике
субстанциями ) . Но эти экзотические
случаи здесь не рассматриваются , о
них есть специальная литература .
(Некоторые стекла – переохлажденный
жидкий кремний не перешедший в
кристаллическое состояние ).
+1200С
( хотя бы малейший толчок – и они
становятся обычными в практике
субстанциями ) . Но эти экзотические
случаи здесь не рассматриваются , о
них есть специальная литература .
(Некоторые стекла – переохлажденный
жидкий кремний не перешедший в
кристаллическое состояние ).
5.3 . ПАРОВЫЕ ПРОЦЕССЫ
В практике чаще имеют случаи , когда процесс протекает в области влажного и перегретого пара, т. е. надо знать его начальные и конечные параметры: изменение внутренней энергии , энтальпии и подведенного ( отведенного ) количества теплоты. Это определяется либо расчетным путем или по s-T и s-I диаграммам , и комментариев здесь не требует .
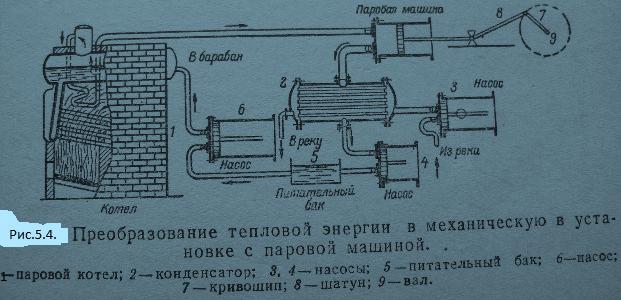
![]() В паровой машине (рис.5.4) тепловая энергия
обращается в механическую за счет
возвратно-поступательного движения
ее поршня , т.е. непосредственно за счет
расширения пара – обычные уравнения
первого закона термодинамики (2.8 -2.12).
Так же работает и паровоз ,но с выбросом
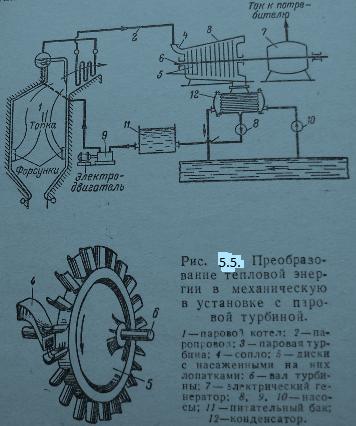
пара) . В паровых
турбинах
(рис.5.5) , газовых турбинах и реактивных
двигателях работа производится за счет
внешней кинетической энергии движущегося
пара или газа. Теплота движущегося в
канале газа расходуется на разгон потока
и увеличение его внешней кинетической
энергии, которая далее в тепловых
двигателях переводится в механическую
работу и передается потребителю.
В паровой машине (рис.5.4) тепловая энергия
обращается в механическую за счет
возвратно-поступательного движения
ее поршня , т.е. непосредственно за счет
расширения пара – обычные уравнения
первого закона термодинамики (2.8 -2.12).
Так же работает и паровоз ,но с выбросом
пара) . В паровых
турбинах
(рис.5.5) , газовых турбинах и реактивных
двигателях работа производится за счет
внешней кинетической энергии движущегося
пара или газа. Теплота движущегося в
канале газа расходуется на разгон потока
и увеличение его внешней кинетической
энергии, которая далее в тепловых
двигателях переводится в механическую
работу и передается потребителю.
