
- •Grundtext 4.
- •2 Lies: [pwa'so:] — Пуассон
- •Vorübungen
- •1. Von wem ist hier die Rede (um wen handelt es sich, wessen Name wird genannt)? — Hier ist von Ostwald die Rede usw. 2. Mit welchen
- •Vorübungen
- •Muster I. Es entwickelt sich Äthylen. Beobachten wir dabei starke Schaumbildung? — Ja, Äthylen entwickelt sich unter starker Schaumbildung.
- •Muster II. Man versetzt die Lösung mit 300 ml Methanol. Muß man dabei kräftig rühren? — Ja, man versetzt die Lösung mit 300 ml Methanol unter kräftigem Rühren.
- •Von Quellungsvorgängen.
- •II) Brief
- •3 Lies: flju:is]—Льюис, Гильберт Ньютон
- •4 Lies: ['laerimju:r] —Лёнгмюр, Ирвинг
- •1 Lies: [pur 1э me'rit] — für das Verdienst. Я
- •1 Ibid., s. 263 ff; Голодников г. В., Манделштам т. В. Практикум по органическому синтезу, с. 64 и сл.
- •2 Sieh: Organikum, s. 218.
ЛЕНИНГРАДСКИИ ОРДЕНА ЛЕНИНА И ОРДЕНА ТРУДОВОГО КРАСНОГО ЗНАМЕНИ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ им. А. А. ЖДАНОВА
Е. В. ДУБРАВИНА
ТЕКСТЫ И УПРАЖНЕНИЯ ПО НЕМЕЦКОМУ ЯЗЫКУ ДЛЯ СТУДЕНТОВ-ХИМИКОВ
Учебное пособие
![]()
Издательство Ленинградского университета Ленинград 1980
I. ANALYTISCHE LEKTÜRE
GRUNDTEXTE UND ÜBUNGEN
GRUNDTEXT 1.
DIE PSEUDOBINAREN SYSTEME
An manchen Stoffen macht man die eigentümliche Beobachtung, daß ihre Schmelz- und Siedetemperaturen veränderlicn sind und von der Erhitzungs- und Abkühlungsgeschwindigkeit, von der beim Erhitzen erreichten Temperatur und von der Anwesenheit geringer katalytisch wirksamer Beimengungen abhängen, obwohl die Stoffe durch ihre bestimmte, unverändert bleibende, chemisch-analytische Zusammensetzung als reine Stoffe charakterisiert sind. Es sind dies durchweg solche Stoffe, welche als isomer oder polymer erkannt worden sind, also im dampfförmigen ш d kristallisierten Zustand aus mehreren Molekülarten bestehen, welche bei gegebener Temperatur und gegebenem Druck nicht in beliebigen Mengenverhältnissen koexistieren können, sondern sich umwandeln, bis eine bestimmte Konzentration des Gleichgewichtes erreicht ist.
Bei solchen Systemen sind die Erscheinungen des heterogenen Gleichgewichtes vom Molekularzustand abhängig, da die Änderungen des Molekularzustandes innerhalb der Phasen, die an und für sich auch sonst auftreten mögen, hier so langsam verlaufen, daß sie die Ausbildung des heterogenen Gleichgewichtes beeinflussen. Es muß daher in solchen Fällen, um die Verhältnisse klarzulegen, das homogene Gleichgewicht berücksichtigt werden. Der Einfluß des Molekularzustandes einer Phase in einem pseudobinären System auf das heterogene Gleichgewicht hängt nur sehr wesentlich ab von der Geschwindigkeit, mit der die beiden Molekülarten bei ihrer Umwandlung der Gleichgewichtskonzentration zustreben. Ist die Umwandlungsgeschwindigkeit so klein, daß sich das Mengenverhältnis der beiden Molekülarten auch bei langsamer Erhitzung und Abkühlung praktisch nicht ändert, so wird das heterogene Gleichgewicht vom Molekularzustand des Systems unabhängig, synthetisch hergestellte Mischungen der beiden Isomeren bzw. Polymeren zeigen bei den Phasenumwandlungen ein durch ihre jetzt unveränderliche innere Zusammensetzung definiertes Verhalten, das System verhält sich wie ein rein binäres oder allgemeiner polynäres.
Ist dagegen die Umwandlungsgeschwindigkeit so groß, daß beim Erhitzen und Abkühlen sich die Gleichgewichtskonzentration der beiden Molekülarten der Temperatur folgend einstellt, so sind Mischungen von beliebiger synthetischer Zusammensetzung nicht beständig, sondern bei jeder Temperatur nur die der Gleichgewichtskonzentration entsprechende Mischung, nur an dieser kann sich eine Phasenumwandlung vollziehen und hierbei muß, wie im folgenden gezeigt wird, die Zusammensetzung, damit aber auch die Temperatur der sich umwandelnden Phase unverändert bleiben. Das System verhält sich jetzt wie ein rein unäres.
Ein in zwei Molekülarten vorkommender Stoff wird also weder bei sehr kleiner noch bei sehr großer Umwandlungsgeschwindigkeit seiner beiden Molekülarten Störungen infolge der Umwandlungen zeigen und wir würden, wenn die Molekylum- wandlungen immer nur sehr langsam oder sehr schnell verliefen, solche Eigenschaften gar nicht kennen.
Pseudobinäre Eigenschaften mit typischen Störungen treten vielmehr an einem Stoff nur dann in Erscheinung, wenn die Umwandlungsgeschwindigkeit mittlere Werte hat, d. h. so groß ist, daß beim Verweilen des Stoffes auf verschiedenen Temperaturen bzw. bei mittleren Abkühlungs- und Erhitzungsgeschwindigkeiten seine Molekularkonzentration sich verändert, die Gleichgewichtskonzentration aber im allgemeinen nicht erreicht wird. Die Schmelz- und Siedetemperaturen sind dann durch die zufälligen Molekularkonzentrationen in der Flüssigkeit oder im Dampf bestimmt, welche unter den angewandten Erhitzungsoder Abkühlungsbedingungen gerade erreicht worden waren.
Die Deutung der Erscheinungen hat offenbar auf der Basis des Zweistoffsystems zu erfolgen, wobei im Zustandsdiagramm ausnahmsweise auch der Einfluß der molekularen Zusammensetzung der Phasen auf das heterogene Gleichgewicht berücksichtigt werden muß. Aus der Abbildung ist ersichtlich, wie die Schmelztemperatur eines Stoffes, der in zwei Molekülarten а und ß vorkommt, von deren Mengenverhältnis in der Schmelze abhängt, unter der Annahme, daß die beiden Formen keine Mischkristalle bilden. Die Temperaturen, bei denen die flüssigen Gemische von a und ß zu kristallisieren beginnen, wenn ihre Ilmwandlungsgeschwindigkeit so klein ist, daß sich die Molekülkonzentration der Schmelze nicht merklich ändert, sind dann durch zwei Kurven ae und be gegeben, die sich im eutektischen Punkt e schneiden. Jede Mischung kristallisiert völlig genau wie die eines binären Systemes. Die Gleichgewichtsverhältnisse der beiden Molekülarten in der Flüssigkeit bei verschiedenen Temperaturen werden nun beschrieben durch eine Kurve cli, welche verschieden verlaufen kann. Um diese auf das homogene Gleichgewicht bezügliche Kurve von der das heterogene Gleichgewicht betreffenden zu unterscheiden, pflegt man sie als Doppelkurve zu zeichnen.
Texterläuterungen
es sind dies — это
sonst — зд.: при других условиях
die Verhältnisse (nur im PI.) —условия, обстановка, картина.
Übungen zum Wortschatz
ü b u n g 1. Übersetzen Sie.
koexistieren, berücksichtigen, sich einstellen, sich vollziehen, sich schneiden, in Erscheinung treten, pflegen + zu-(-Infinitiv; bis, an und für sich, im allgemeinen, auf etwas bezüglich = etwas betreffend, mehrere, mehr; zufällige Beobachtung, zufällig anwesende Beimengung; die Gleichgewichtskonzentration, dai Konzentrationsgleichgewicht; die Umwandlungswärme, die Wärmeumwandlung;
folgen, folgend, im folgenden, infolge, in der Folge, zur Folge haben, erfolgen, verfolgen;
bestehen (vi), beständig, bestehen aus (Dat.), der Bestandteil, bestehen in (Dat.);
sich verhalten, das Verhältnis, das Verhalten, die Verhältnisse.
Übung 2. Sagen Sie deutsch.
а) достигать, состоять, отличать от ...; исключение, в порядке исключения (как исключение), предположение, предполагая (если предположить, при предположении, что ...);
б) переменные значения, переменный состав, достигнутая температура, новое толкование, небольшая примесь, парообразное состояние, иное поведение, гетерогенное равновесие, медленное охлаждение, большая скорость, различные условия, данное давление, любые количественные соотношения, сколь угодно малые примеси, любой состав, сколь угодно медленно, как угодно изменять скорость;
в) в кристаллическом состоянии, в кристаллическое состояние, в бинарной системе, в бинарную систему, в горячий расплав, в горячем расплаве, в жидкой смеси, в смешанный кристалл;
г) 1. Изменение концентрации влияет на равновесие.
Скорость нагревания повлияла на температуру кипения.
Влияют примеси на температуру плавления? 4. На равновесие влияло молекулярное состояние. 5. Что может влиять на
гетерогенное равновесие? 6. Влияет на гетерогенное равновесие молекулярный состав?
д) 1. Оба вида молекул стремятся к равновесной концентрации. 2. Система стремится к состоянию равновесия. 3. Кривая плавления будет стремиться к нулевой точке.
е) 1. Оба вида молекул превращаются друг в друга, пока не достигается (результативный пассив) определенная концентрация. 2. Мы нагреваем смесь, пока не установится (перфект) состояние равновесия. 3. Жидкую смесь нагревают до тех пор, пока она не начинает кристаллизоваться.
Übung 3. Beantworten Sie die Frage "Was ist aus der Abbildung ersichtlich?" mit folgenden Sätzen. Bilden Sie dabei
Satzgefüge.
1. Происходит превращение фаз. 2. Присутствие небольших примесей влияет на температуру кипения. 3. Кривая плавления стремится к нулевой точке. 4. Кривые пересекаются в эвтектической точке. 5. Изменения температуры учитываются. 6. Обе фазы могут сосуществовать. 7. Кривая может проходить по-разному. 8. Температура плавления зависит от количественных соотношений.
GRUNDTEXT 2.
ATOMGRUPPEN MIT KONJUGIERTEM SYSTEM
Für den Organiker sind besonders Systeme von Interesse, die das Schwefelatom enthalten und in denen der Schwefel mit vier bzw. sechs Valenzen gebunden sein kann. So wurde im Falle der Sulfone die Frage, welche der nachstehenden Formeln der Wirklichkeit am nächsten kommt, stark diskutiert.
О |
о |
II —s— |
■ t —s - |
II о |
!l О |
Im ersten Fall würden um das Schwefelatom 12, im zweiten 10 Elektronen angeordnet sein. Die Untersuchung einzelner Verbindungen zeigte, daß die erste Strukturformel den tatsächlichen Zustand richtig darstellt, während bei anderen Verbindungen Eigenschaften auftraten, die eher anderen Strukturen entsprechen.
Unter der Voraussetzung der Konjugation läßt sich jedoch eine sehr einfache Erklärung finden. Die beiden Strukturen unterscheiden sich voneinander lediglich darin, ob das eine Elektronenpaar wie in der zweiten Formel mit dem dativ gebundenen Sauerstoffatom frei ist, oder ob es, wie in der anderen Formelgezeigt ist, eine Bindung mit dem Schwefelatom herstellt. Bei einzelnen Verbindungen lassen sich zwischen den beiden Formeln, die lediglich mit Hilfe von Valenzlinien die Struktur beschreiben, offensichtlich keine so scharfen Grenzlinien ziehen. Das Elektronenpaar kann in einem mehr oder weniger großen Ausmaß in das Kraftfeld des Schwefelatoms gezogen werden und ist dadurch imstande, mit dem Schwefel eine Bindung herzustellen. Die Stärke der Bindung hängt vom Zustand des Schwefelatoms ab, der seinerseits jedoch davon beeinflußt wird, welche Atomgruppen sich noch an ihm befinden. Einzelne Gruppen können zu einer Verstärkung der Bindung führen, andere wiederum eine Verminderung derselben verursachen. Dementsprechend steht die Elektronenverteilung in einzelnen Fällen der anderen Struktur näher. Das ist auch der Grund, warum zwei verschiedene Verknüpfungsmöglichkeiten zu bestehen scheinen. In Wirklichkeit existiert aber zwischen beiden ein kontinuierlicher Übergang, so daß es nicht möglich ist, mit Hilfe von Valenzlinien die tatsächlichen Strukturen zu formulieren. Stets wird von den Eigenschaften der jeweiligen Atomgruppen bestimmt, welcher Elektronenzustand sich ausbilden kann. Dieser ist hier also komplizierter als in den anderen besprochenen Fällen, da das Schwefelatom im sp3d2-Hybridzustand vorliegt und es bedeutend schwieriger ist, die Art, in der in diesem Zustand eine Konjugation zustande gebracht wird, in der Papierebene anschaulich darzustellen. Wir wollen daher von weiteren Untersuchungen über die Ausbildung der Konjugation Abstand nehmen.
Wir begegnen also in der organischen Chemie der Konjugation sehr häufig und ihr Vorliegen kann für die Reaktionsweise von großer Wichtigkeit sein. Infolge der Konjugation werden Bindungen delokalisiert, so daß sich die Struktur mit Hilfe der Valenzlinien nicht adäquat ausdrücken läßt. Mit den durch sie hervorgerufenen Veränderungen werden wir uns unter anderem im nächsten Kapitel ausführlich beschäftigen, doch lassen sich bereits jetzt gewisse vergleichende Folgerungen ziehen, die nützliche Aufschlüsse zu bieten vermögen.
Der einfaste Fall liegt dann vor, wenn sich Atombahnen mit identischem Elektronenzustand kombinieren. Die Elektronenverteilung wird dadurch symmetrisch, und das Auftreten der Knotenebenen erfolgt im Rahmen der geometrischen Verhältnisse des Moleküls. Sind jedoch die Atome verschieden, verändert sich auch die Elektronenverteilung, da die Bahnen auf Grund ihrer Verschiedenheit nicht mit gleichem Gewicht berücksichtigt werden und daher der sich ausbildende Elektronenzustand verschieden wird. Auf die Ausbildung der Elektronenverteilung übt auch im allgemeinen die Elektronenaffinität der das konjugierte System aufbauenden Atome bis zu einem gewissen Grad einen Einfluß aus, da sich die relative Elektronenverteilung im großen mit dem Elektronegativitätswert ändert.
Die Ausbildung der Bahnen wird naturgemäß auch von der ursprünglichen Zahl der Elektronen beenflußt, die sich auf den die Kombination ermöglichenden Bahnen befinden. Offensichtlich kann eine Bahn dann die stärkste Konjugation zustande bringen, wenn sich kein Elektron auf ihr befindet. Dann wird nämlich durch die Einbeziehung dieser Bahn in das konjugierte System nur der zur Verfügung stehende Raum vergrößert, während die Zahl der Elektronen gleich bleibt. Daher sind zur Anordnung der Elektronen ebenso viele Bahnen erforderlich, als wenn die Bahn nicht einbezogen worden wäre, während der den Elektronen zur Verfügung stehende Raum durch die Einbeziehung anwächst. Das führt aber zu einer Erhöhung der Delokalisierungsenergie im Sinne der Heisenbergschen Relation, d. h. zu einer stärkeren konjugierten Bindung. Eine relative Abnahme der Konjugation ist dann zu erwarten, wenn sich die Bahnen mit einem Elektron bzw. zwei Elektronen stufenweise auffüllen.
Schließlich wird die Ausbildung der Konjugation auch dadurch beeinflußt, ob die Atome, die zu den die Konjugation ermöglichenden Bahnen gehören, über eine positive oder negative Ladung verfügen. Wie wir im Falle des Carboxylatanions sahen, begünstigt der Ladungsüberschuß, falls sich eine Bahn kombiniert, auf der sich ein spinkompensiertes Elektronenpaar befindet, die Konjugation im Verhältnis zu den Fällen, in denen nur ein kleiner Ladungsüberschuß oder gar keiner vorzufinden ist. Auf ähnliche Weise wird die Konjugation im Falle einer leeren Bahn durch ein Atom gefördert, das Elektronenmangel, d. h. eine positive Ladung, aufweist.
Unter Berücksichtigung dieser Ergebnisse sind wir imstande, über die in der Wellenfunktion ausgedrückte Elektronenverteilung bis zu einem gewissen Grad qualitative Aussagen zu machen. In einzelnen Fällen können wir auch die geometrischen .Symmetrieverhältnisse zu Hilfe nehmen. Um aber die Reaktionsweise völlig zu verstehen, reichen diese nicht aus, sondern wir ' müssen auch in verstärktem Maße die qualitativen Werte der l'.lektronenverteilung heranziehen. Diese lassen sich mit Hilfe wollenmechanischer Näherungsmethoden bestimmen, ihre Anwendung ist aber bereits bedeutend schwieriger als in Fällen mit einfachen lokalisierten Bindungen. Bei der Anwendung der Molekülbahnmethode werden die die Konjugation zustandebrin- tfonden Bahnen miteinander kombiniert, um eine Elektronenver- leilung mit möglichst kleinem Energieinhalt zu erreichen. Da bei ilor Durchführung der Berechnungen bedeutend kompliziertere Probleme auftreten als bei den lokalisierten Bindungen, ist die Lösung derselben im allgemeinen für den Organiker nicht möglich. Auf dieselben Schwierigkeiten stößt man bei der Anwendung der Valenzbindungsmethode. Dabei wird das Energieminimum durch die Kombination der verschiedenen möglichen Grenzstruk- <uren angenähert. Im Falle des Benzols werden z. B. die zwei
Kekule- und drei Dewar Strukturen in Betracht gezogen. Bei anderen Verbindugen können aber bedeutend mehr Grenzformen in Erscheinung treten. So lassen sich z. B. beim Naphthalin 42 Strukturen formulieren, und daher ist auch in diesen Fällen eine genaue Durchführung der Berechnungen sehr schwierig.
Texterläuterung im Rahmen der geometrischen Verhältnisse des Moleküls — в пределах геометрии молекулы.
1 Lies: ['dju: э г]—Дьюар
Übungen zum Wortschatz
Übung 1. Übersetzen Sie.
tatsächlich, lediglich, unter anderem, auf Grund (aufgrund), nämlich; die Stärke, die Verteilung, die Ebene, der Überschuß, der Mangel; die Näherungsmethode—die Methodenlehre; das Kraftfeld — die Anziehungskraft; verursachen, hervorrufen, erfolgen, begünstigen, fördern, von Interesse sein, von Wichtigkeit sein, imstande sein, zustande bringen, einen Einfluß ausüben, zur Verfügung stehen, in Erscheinung treten;
ziehen, der Zug, die Zugfestigkeit, Folgerungen ziehen, in Betracht ziehen, anziehen, einbeziehen, heranziehen;
1. Die letzte Formel kommt der Wirklichkeit näher. 2. Der Reaktionspartner nähert sich dem polarisierten Molekül von der elektrostatisch begünstigten Seite her und tritt bei einer bestimmten Entfernung mit ihm in Wechselwirkung.
Ü b u n g 2. Sagen Sie deutsch.
а) зависеть, существовать, сосуществовать, относиться (принадлежать), провести (линию); ослабление (уменьшение), усиление, причина, орбиталь; с учетом (принимая во внимание), дело в том, что. . .;
б) сопряженная система, непрерывный переход, сильное гопряжение, количественные результаты, более четкая граница, более наглядное изображение, сложнейшие расчеты, самое подробное исследование;
в) 1. Вокруг атома серы расположены 10 электронов. 2. Он занимается сложной проблемой. 3. Мы занимаемся сопряженными системами. 4. Система содержит атом серы. 5. Структура не соответствует формуле. 6. Следует различать качественные и количественные изменения. 7. Атом кислорода образует связь с атомом серы. 8. Состояние атома серы влияет на связь. 9. Отдельные группы вызывают (являются причиной) ослабление связи. 10. Структуру выражают с помощью валентных линии. 11. Распределение электронов изменилось. 12. Число электронов оказывает влияние на образование орбиталей.
QRUNDTEXT 3.
DIE --KOMPLEXBINDUNG
Bei den bisher behandelten van der Waalsschen Bindungstypen fanden wir im allgemeinen, daß die Bindung dadurch zustande gebracht wird, daß die Elektronen eines Atoms mit irgend einem anderen Atom eines Moleküls bis zu einem gewissen Grad eine partielle Bindung herstellen. Die Bindung kann von zwei Elektronen hergestellt werden, doch können auch, wenn die auftretenden Asymmetrien bei der Entstehung der Bindungs- und Lockerungsbahnen einen bedeutenden Energieunterschied verursachen, zwei Bindungs- und zwei Lockerungselektronen dieselbe zustande bringen. Im allgemeinen läßt sich bei diesen Bindungen immer feststellen, zwischen welchen Atomen die Bindung stattgefunden hat.
In der organischen Chemie gibt es jedoch auch sehr viele Verknüpfungen, sei es bei der Ausbildung von stabilen oder instabilen Gebilden, bei denen die Feststellung, welche bestimmten Atome verknüpft wurden, nicht möglich ist. In diesen Fällen werden nämlich die Bindungen von den Molekülen als Ganzes zustande gebracht. Die Bindung kann zwischen einem bestimmten Atom und einem Molekül hergestellt werden; wir kennen jedoch auch Fälle, bei denen sich zwei Moleküle verknüpfen. Dieser Bindungstyp tritt im allgemeinen bei Verbindungen auf, deren Moleküle rt-Bindungen enthalten. Es besteht die Wahrscheinlichkeit, daß diese die zwischen den Molekülen bestehenden Bindungen zustande bringen, da die ст-Bindungen ja bedeutend stabiler sind und ihre Aufspaltung die Stabilität der Moleküle gefährden würde. Aus diesen Verbindungen lassen sich durch Erwärmen oder sonstige Einwirkung die unveränderten Ausgangsstoffe leicht zurückgewinnen. Die л-Bindungen bzw. л-Elektronen sind nicht übermäßig stark an einen Ort gebunden, •auch wird durch ihre Anregung oder durch andere Reaktionen die Existenz der Moleküle nicht gefährdet, da die я-Bindungen ja nur dann existenzfähig sind, wenn zwischen den verbundenen Teilen auch bereits eine 0-Bindung besteht, die die Aufrechterhaltung der Bindung sichert.
Ähnlich wie bei der Deutung der dativen Bindung ist der mil Hilfe der я-Bindung zustande kommende van der Waalssche Bindungstyp so zu verstehen, daß die Donorrolle nicht von einem einsamen Elektronenpaar eines Atoms, sondern von den in einer л-Bindung befindlichen Elektronen eines Moleküls ausgeübt wird. Die Bindung wird in diesem Falle, in dem sich das Äthylen oder ein konjugiertes System, z. B. das ganze д-Elektronen- system des Benzols, als donorartige "Base" verhält, nach M. J. S. Dewar я-Komplexbindung genannt. Die л-Komplexbin- dung entspricht in ihrem Wesen einer zwischen einem Kation und einem ungesättigten Bindungssystem auftretenden Ionen- Dipolbindung, wobei das polarisierende Elektronenpaar des Dipols nicht von dem einsamen Elektronenpaar eines Atoms, sondern von dem я-Elektronensystem geliefert wird. Das ungesättigte Bindungssystem besitzt infolge seiner großen Elektronenkonzentration donorartige Eigenschaften, wenn auch in geringerem Maße als ein Atom, das ein einsames Elektronenpaar besitzt. Dementsprechend verhalten sich die ungesättigten Kohlen- stoff-Verbindungen — besonders die Olefine und aromatischen Kohlenwasserstoffe — in Gegenwart koordinativ ungesättigter Kationen als Dipole: die leicht polarisierbaren я-Elektronen- paare greifen als Donor in das Kraftfeld des Kations über. Wie bereits erwähnt, ist die я-Komplexbindung keine ausschließlich im Kraftfeld eines Atoms des Kations und des Dipols lokalisierte Bindung, sondern eine im Kraftfeld des Kations und des gesamten konjungierten Systems zur Geltung kommende Bindung. Die ursprüngliche я-Komplex-Theorie von Dewar rechnet nur mit der einen Ausbildungsmöglichkeit des я-Komplexes, und zwar mit der nicht lokalisierten Art, bei der also der gebundene Teil längs des konjugierten я-Systems statistisch mit gleicher Wahrscheinlichkeit auffindbar ist.
Die Bindung eines X+-Kations an das л-Elektronensystem des Äthylens oder Benzols kann nach Dewar auf folgende Weise dargestellt werden.
![]()
Besonders beim Benzol scheint aber diese Vorstellung physikalisch weniger begründet zu sein. Melander machte bereits im Jahre 1950 auf den Widerspruch aufmerksam, daß es nicht wahrscheinlich ist, daß der elektrophile Substituent den Benzolring senkrecht zu dessen Ebene in der Mitte angreift und sich dort bindet, wie dies Dewar symbolisiert, da bekanntlich die Elektronendichte im Mettelpunkt des Benzolrings ziemlich gering ist. Es ist weit wahrscheinlicher, daß die Bindung des Kations an der Stelle mit der dichtesten я-Elektronenwolke vor sich geht. Das heißt also, daß bei substituierten Benzolen der Substituent mit der größten Wahrscheinlichkeit an den elektronegativsten Stellen anzutreffen ist, also in der Nähe jener Kohlenstoffatome, die das Substitutionsverhältnis aufweisen.
Bei der experimentellen Begründung der Dewarschen я-Кот- |ilr\thcorie pflegt man sich am meisten auf folgende Tatsachen /ti berufen:
I
Ii
C6H0+HF ^ C6HfF~
Fairbrother 1 brachte die bei den Lösungen des Jods in verschiedenen aromatischen Kohlenwasserstoffen beobachtete Änderung des Dipolmoments mit dem nukleophilen Charakter des aromatischen Ringes in Zusammenhang und erklärte die sich vom violetten bis zum bräunlichen ändernden Farben dieser Jodlösungen mit dem Auftreten verschieden starker Verbindungen vom л-Komplex-Typ.
Benesi und Hildebrand prüften später das ultraviolette Ab- sorbtionsspektrum dieser Jodlösungen, aus dem sich ebenfalls ableiten ließ, daß ein Zusammenhang mit dem basischen, nukleophilen Charakter des Ringes vorliegen muß.
Neben den bei der я-Komplextheorie auftretenden physikalischen Widersprüchen wiesen auch sehr bald zahlreiche chemische Untersuchungen darauf hin, daß diese Verknüpfungsart nicht die einzige Möglichkeit für den Bindungszustand zwischen konjugierten Verbindungen und elektrophilen Komponenten darstellen kann.
H. C. Brown2 und Mitarbeiter untersuchten die Natur der Zwischenkomplexe der Alkylbenzole. Bei der Prüfung der Löslichkeit von Salzsäure bzw. von Salzsäure und Aluminiumchlorid, später auch von Bromwasserstoff bzw. Bromwasserstoff und Aluminiumbromid in aromatischen Verbindungen fanden sie, daß die Reihenfolge der Basizität der Alkylbenzole (Toluol, Xylole, Mesitylen, Durol usw.) gegenüber Chlor- bzw. Bromwasserstoff nicht identisch ist mit der, die sie dem System Chlorwasser- stoff+Aluminiumchlorid gegenüber zeigen. Bei einem Vergleich dieser Resultate mit der bei elektrophilen aromatischen Substi- lutionen beobachteten Reihenfolge der Reaktionsgeschwindigkeit ergab sich, daß die mit dem System Salzsäure + Aluminiumchlo- rid gewonnenen Basizitätswerte mit der experimentell bestimmten Reihenfolge bei elektrophilen Substitutionen übereinstimmen, während die der Salzsäure allein gegenüber gezeigte Abstufung der Basizität davon abweicht.
Brown setzte auf Grund seiner experimentellen Resultate die Existenz von zwei Arten intermediärer Komplexe voraus, wobei er den labilen, sich der Salzsäure gegenüber ausbildenden Komplex für einen Dewarschen я-Komplex hielt, während er die sieh mit dem System Salzsäure-hAluminiumchlorid ausbildenden Komplexe cr-Komplexe nannte.
Die Entstehung dieser zwei Arten von Komplexen können wir uns folgendermaßen vorstellen. Bekanntlich ist das Benzol ein planares Molekül, das von einer doppelten Elektronenhülle relativ hoher Elektronenkonzentration umgeben ist. Offenbar tritt ein elektrophiles Reagens dort mit der Elektronenwolke in Bindung, wo die Elektronendichte am größten ist. Die Elektronendichte ist jedoch in der Nähe des Ringzentrums voraussetzungsgemäß gering, während sie über und unter den den Ring aufbauenden Kohlenstoffatomen auf Grund der Überlappung der p-Bahnen zur я-Sextett-Elektronenwolke relativ groß ist. Daher wird sich das elektrophile Reagens offenbar mit den Stellen, die eine relativ hohe Elektronendichte aufweisen, verknüpfen, und wird sich, falls keine großen, raumfüllenden Substituenten vorhanden sind, an diesen Stellen neben der Elektronenhülle aufhalten, ohne eine wesentliche Perturbation derselben zu verursachen. Besitzt jedoch das Reagens einen sehr starken elektro- philen Charakter, ist auch die Möglichkeit zu einer Durchbrechung, einer Perturbation der я-Elektronenwolke gegeben, in deren Folge sich dann an einem der sechs Kohlenstoffatome, die den Ring aufbauen, eine kovalente cr-Bindung auszubilden vermag. Diese Perturbation bzw. Durchdringung der л-Elektronen- wolke erfordert eine bedeutende Aktivierungsenergie, auf Grund der sich die beiden Typen der л- und a-Komplexe unterscheiden lassen.
Texterläuterung
Durchdringung der л-Elektronenwolke — разрушение л-элек- тронного облака.
Übungen zum Wortschatz
Übung 1. Übersetzen Sie.
verursachen, verknüpfen, liefern, ableiten, zur Geltung kommen, übereinstimmen, ein Problem behandeln; hinweisen, sich erweisen, beweisen, nachweisen, eine Eigenschaft aufweisen; rechnen mit etwas, aufmerksam machen auf etwas, halten für etwas; das Gebilde, die Anregung, die Deutung, die Überlappung, der Zusammenhang, die Lockerungselektronen — die Elektronenlockerung; in gewissen Grenzen, einzig, bekanntlich, nämlich, wenn auch, und zwar.
Ü b u n g 2. Sagen Sie deutsch.
значительное различие, нестабильное образование, первоначальное представление, единственная возможность, известный факт, упомянутое противоречие, небольшая электронная плотность; путем нагревания, с помощью а-связи, в присутствии катионов, вблизи углеродных атомов, на месте электронного облака, в ароматическом кольце, в ароматическое кольцо, на вертикальной плоскости, на вертикальную плоскость; образовать связь, считаться с возможностью, обратить внимание на противоречие, изобразить процесс, толковать явление.
Ü b u n g 3. Sagen Sie deutsch, indem Sie den Satz durch je zwei angegebene Varianten vervollständigen.
Мы констатируем:
1. ... возникновение связывающих орбиталей; ... что возникают связывающие орбитали. 2. . .. связь между молекулами; ... что молекулы образуют связь. 3. . . . разрыв (расщепление) связи; ... что связь разрывается. 4. . . . изменение ди- нольного момента; . . . что дипольный момент изменяется. • ». ... появление другого типа связи; ... что появляется дру-
ой тип связи.
Übung 4. Fragen Sie deutsch und beantworten Sie Ihre Frage mit den nachstehenden Sätzen.
Что вытекает отсюда? — Отсюда вытекает:
1. ... связь с нуклеофильным характером кольца. 2. . . . что л комплексная связь по своей сути соответствует ионной ди- иольной связи. 3. ... что ненасыщенное углеродное соединение ведет себя как диполь. 4. ... еще одна возможность возникновения комплексных соединений. 5. . . . что молекула бен- м>ла окружена двойной электронной оболочкой. 6. . . . что '.исктрофильный реагент задерживается на этом месте.
Hbung 5. Übersetzen Sie; beachten Sie die Bedeutung des Suffixes -bar.
ein statistisch auffindbarer Teil; leicht polarisierbare I li'ktronenpaare; die experimentell begründbare Theorie;
17
1. Die direkte Wechselwirkung der Kerne ist nicht beo- Imchtbar. 2. Zahlreiche Reaktionen galten früher als undurchführbar. 3. Die magnetische Kernresonanz hat sich als ein vielseitig mwendbares Verfahren erwiesen. 4. In ihrer potentiellen Bedeu- limg für die chemische Strukturforschung ist die noch recht Hinge magnetische Kernresonanzmethode vielleicht vergleichbar mit der Ultrarotspektroskopie.
Grundtext 4.
DIE ÄNDERUNG VON TEMPERATUR, DRUCK UND KONZENTRATION INNERHALB EINES PHASENKOMPLEXES UND DIE GESCHWINDIGKEIT DER GLEICHGEWICHTSEINSTELLUNG
Ein heterogenes System befindet sich im Gleichgewicht nur <l,iiiii, wenn in allen seinen Punkten die gleiche Temperatur, der Ulriche Druck, nämlich die Temperatur und der Druck des Gleichgewichtes herrscht, und wenn im Fall eines Mehrstoffsystemes |r<!c Phase in allen Punkten diejenige Zusammensetzung hat, welche ihr bei dem herrschenden Druck und der herrschenden Temperatur zukommt. Damit diese Bedingung während einer Umwandlungeines Phasenkomplexes erfüllt, der Gleichgewichtszustand also in jedem Moment erhalten bleibt, müssen sich die mit der Phasenumwandlung verbundenen Änderungen der Temperatur, des Druckes und der Zusammensetzung der Phasen genügend schnell ausgleichen können. Auf den Wärmeausgleich ist von Einfluß das Wärmeleitvermögen, die Strahlung und die Konvektionsströme, auf den Druckausgleich die innere Beweglichkeit (innere Reibung) der Phasen, auf den Konzentrationsausgleich die Diffusion und Konvektion und auf alle drei Gestaltung der Phasenmassen, wodurch die Größe der Berührungsflächen und die Größe der Diffusionswege bestimmt wird.
Günstige Bedingungen für eine schnelle Einstellung des Gleichgewichtes sind also: große Wärmeleitfähigkeit der Komponenten bzw. der Phasen eines Systems (Metalle, Legierungen), Vorhandensein flüssiger und gasförmiger Phasen, wobei der Ausgleich der Wärme und der Konzentration noch durch Rühren gefördert werden kann, sowie feine Verteilung und möglichst allseitige Berührung der Phasen (kleine Kristalle, Kristallpulver, Emulsion).
Ungünstig liegen dagegen die Verhältnisse bei schlechtleitenden Stoffen, bei Systemen aus festen Phasen, wenn jede Phase die andere als große ununterbrochene Masse berührt, und im allgemeinen bei niedrigen Temperaturen. Immerhin verdient hervorgehoben zu werden, daß eine ganze Reihe von polymorphen Umwandlungsgleichgewichten in festen Phasen trotz niedriger Versuchstemperatur (bis —250° herunter) sich noch schnell und gut einstellt.
Wenn die Umwandlung sich mit endlichen Geschwindigkeiten vollzieht, so scheinen die Abweichungen vom Gleichgewicht in erster Linie durch inhomogene Vorgänge der Diffusion und des Temperaturausgleiches verursacht zu sein, während das heterogene Gleichgewicht nicht nennenswert verschoben ist. Normalerweise werden die Bedingungen des Gleichgewichtes, sofern die Umwandlung stattfindet, an der Berührungsgrenze der Phasen gegeben sein und sich, falls die sich umwandelnde Phase unterkühlt bzw. übersättigt ist, beim Eintritt der Umwandlung an der Berührungsgrenze von selbst herstellen. So entsteht beim Eintritt der Kristallisation in einer unterkühlten Flüssigkeit an der Kristallisationsgrenze die Temperatur des Schmelzpunktes, bei der Kristallisation einer übersättigten Lösung ist an der Kristallisationsgrenze die Sättigungskonzentration vorhanden, und wenn man einen polymorphen Stoff zwecks Umwandlung desselben in eine bei höherem Druck stabilere Form über den Gleichgewichtsdruck der beiden Formen hinaus komprimiert, so springt der Druck durch den Eintritt der Umwandlung auf den des Gleichgewichtes zurück. Diese Überlegungen gelten anscheinend mit großer Annäherung für den metallischen Zustand. Bei anderen Stoffen, insbesondere bei Silikaten und organischen Körpern können anscheinend erhebliche Abweichungen, also auch Verzögerungen der heterogenen Reaktionen selbst aufreten.
Bemerkenswert ist noch die Tatsache, daß die Bildung einer neuen Phase mit Vorliebe an der Grenzfläche vorhandener Phasen und in Kristallkonglomeraten an den Korngrenzen beginnt.
Allgemein folgt aus der Erörterung der die Phasenumwandlung bedingenden Faktoren, daß eine langsame Änderung der Zustandsbedingungen (z. B. langsame Abkühlung) das Erreichen stabiler Zustände, dagegen schnelle Änderung (z. B. schnelle Abkühlung) die Entstehung instabiler Zustände begünstigt.
Die Geschwindigkeit, mit der sich der Gleichgewichtszustand in einem Phasenkomplex einstellt, ist von größter Bedeutung für die Erforschung heterogener Systeme, denn die hierzu nötige Ermittlung von Gleichgewichtstemperaturen und Gleichgewichtsdrucken setzt ja voraus, daß der Gleichgewichtszustand sich auch wirklich einstellt. Geschieht dies mit solcher Geschwindigkeit, daß derselbe einer Änderung seiner Bedingungen unmittelbar folgt, z. B. dem Wärmefluß bei der Kristallisation einer Metallegierung, so kann die Änderung des Gleichgewichtszustandes als Folge fortlaufender Änderung einer seiner Bedingungen direkt messend verfolgt werden (kinetische Methoden), z. B. durch Aufnahme einer Abkühlungskurve.
Wenn die Geschwindigkeit der Gleichgewichtseinstellung hingegen kleiner ist, wie allgemein bei niedrigeren Temperaturen, im festen, kristallisierten und im Glaszustand, bei schlecht leitenden Stoffen (Silikaten) und wenn bei großen Phasenmassen ihre gegenseitige Berührungsfläche klein ist, so muß die Ände- ningder Gleichgewichtsbedingung entweder entsprechend langsamer vorgenommen werden (z. B. langsame Abkühlung) oder man muß sich darauf beschränken, schrittweise vorzugehen, Indem man die Einstellung des Gleichgewichtszustandes unter bestimmten Bedingungen, welche man genügend lange Zeit konstant hält (Druck, Temperatur), abwartet und eine andere Eigenschaft, nachdem sie ihren Gleichgewichtswert erreicht hat, benimmt, z. B. die Ermittlung des Gefügegleichgewichtes an Kristallisationskonglomeraten, z. B. Metallegierungen, des Dampfdruckes von festen Phasen (statische Methoden).
Eine beträchtliche Hemmung erleidet die Geschwindigkeit Hner Phasenumwandlung auch dann, wenn die an der Grenze zweier vorhandener neu entstehende Phase kristallisiert ist. Da <l,is Auftreten solcher, die reagierenden Phasen trennenden Schichten bzw. Umhüllungen einer Phase praktische Bedeutung Imt und eine häufige Fehlerquelle bei Gleichgewichtsbestimmun- gen bildet, möge die Erscheinung an einem Beispiel erläutert werden.
Texterläuterung
ungünstig liegen die Verhältnisse — неблагоприятная картина складывается, неблагоприятные условия наблюдаются (vgl. Texterläuterung, S. 8).
Übungen zum Wortschatz
Übung 1. Übersetzen Sie.
erhalten bleiben, sich ausgleichen, sich berühren, verteilen, sich vollziehen, abweichen, gelten; die Ermittlung, die Hemmung, die Aufnahme einer Kurve; innerhalb, nämlich;
1. Das Gleichgewicht wird verschoben. 2. Erläutern wir die Erscheinung an einem Beispiel. 3. Man kann den Ausgleich der Konzentration durch Rühren fördern. 4. Jeder Phase kommt in allen Punkten dieselbe Zusammensetzung zu. 5. Die innere Reibung der Phasen ist auf den Druckausgleich von Einfluß. 6. Für die Reaktionsweise ist die Konjugation von großer Wichtigkeit. 7. Ist die Geschwindigkeit der Gleichgewichtseinstellung von Bedeutung? 8. Auch als analytisches Hilfsmittel kann die magnetische Kernresonanz für spezielle Probleme von großem Nutzen sein.
U b u n g 2. Sagen Sie deutsch.
а) низкая температура, благоприятные условия, большая поверхность, хорошая проводимость, обсуждение условий реакции, частый источник ошибок;
б) 1. Устанавливаетсня равновесие. 3. Закон действителен (сохраняет силу) и в отношении (для) переохлажденного состояния. 3. Мы предполагаем одинаковый состав. 4. Давление поддерживают (держат) постоянным. 5. Следует выполнить целый ряд условий. 6. За кристаллизацией можно проследить. 7. Большая теплопроводность благоприятствует установлению равновесия. 8. Реакция в значительной степени замедляется (наступает значительное замедление реакции).
U b u n g 3. Verbinden Sie die folgenden Substantive mit passenden Bestimmungswörtern; beachten Sie dabei das Geschlecht der Substantive; übersetzen Sie die gebildeten Wortverbindungen.
Druck, Phase, Verteilung, Zusammensetzung, Bedingung. Zustand, Abweichung, Verzögerung, Abkühlung, Beobachtung, Änderung, Rührer, Flüssigkeit, Ausgleich, Temperatur, Berührung.
Flüssig, niedrig, günstig, inner, groß, ununterbrochen, fein, lu lrrogen, gasförmig, allseitig, fest, unterkühlt, übersättigt, rlirbtlch, herrschend, langsam, nötig, fortlaufend, gegenseitig, haufig.
GRUNDTEXT 5.
WERTIGKEIT UND CHEMISCHE BINDUNG
Die Zahl der Atome, mit denen ein Element zu einer neutralen Verbindung verbunden sein kann, ist durch die Zahl seiner locker gebundenen Elektronen nach oben begrenzt. Deshalb nennt man diese locker gebundenen Elektronen, die die maximale Wertigkeit eines Elements bestimmen, Valenzelektronen. Es brauchen sich aber nicht alle Elektronen zu betätigen. Im allgemeinen erweisen sich die Elemente der 5., 6. und 7. Gruppe, soweit sie für die organische Chemie in Frage kommen, nicht als fünf-, sechs- und siebenwertig, wie der Zahl ihrer Valenzelektronen entsprechen würde, sondern als drei-, zwei-, und einwertig. Sie treten also mit einer Wertigkeit auf, bei deren Ausübung die Zahl ihrer Valenzelektronen zu 8 ergänzt wird, z. B. wenn der Stickstoff, der fünf Valenzelektronen besitzt, sich mit drei Wasserstoffatomen, von denen jedes ein Elektron mitbringt, zu Ammoniak verbindet. Es besteht also eine Neigung zur Bildung von Gruppen zu 8 Elektronen, den sogenannten Achterschalen, die sich in den Edelgasen auftreten. Eine solche Gruppe von 8 Elektronen nennt man nach Lewis1 und Langmuir2 auch "Oktett". Die Bildung eines solchen Oktetts kann man in Formeln zum Ausdruck bringen, in denen sämtliche Valenzelektronen als Punkte geschrieben werden, und nicht nur, wie es Couperschen 2Strichformeln entspräche, die bei einer Bindung betätigten.
Die neue Schreibweise von Lewis — Langmuir läßt erkennen, ob in der vorliegenden Verbindung ein Atom sämtliche Valenzelektronen betätigt hat oder nicht, was aus den alten Formeln nicht zu ersehen ist. Da zu einer Bindung stets zwei Elektronen benötigt werden, und die Elemente der ungeradzahligen Gruppen des periodischen Systems nur ungeradzahlige Wertigkeiten, die der geradzahligen Gruppen nur geradzahlige Wertigkeiten betätigen, bleibt stets eine geradzahlige Anzahl von Elektronen des Oktetts frei. Diese faßt man zu Paaren zusammen, die man "einsame Elektronenpaare" nennt; der Stickstoff in Ammoniak hat eins, der Sauerstoff im Wasser deren zwei. Diese einsamen Flektronenpaare können unter Umständen bei der Bindung weiterer Atome mitwirken; so ist z. B. die Additionsfähigkeit des Ammoniaks auf sein einsames Elektronenpaar zurückzuführen, wovon weiter unten die Rede sein wird. Da man in den älteren Formeln diese Additionsfähigkeit nicht besonders zum Ausdruck brachte, obwohl man sie kannte, sprach man früher von "nicht betätigten" oder "latenten" Valenzen — im Grunde genommen genau dasselbe, was man nach Lewis — Langmuir einsame, d.h.
nicht in einer Bindung betätigte, Valenzelektronenpaare nennt.
Die Oktetttheorie fordert, daß jedes Atom beim Eingehen in eine chemische Verbindung bestrebt ist, sich mit acht Elektronen zu umgeben. In dieser strengen Form, als Gesetz, läßt sich die Oktetttheorie nicht aufrechterhalten, obwohl man mehrfach versucht hat, alle Formeln so zu gestalten, daß jedes Atom ein Oktett besitzt.
Für die erste Reihe des periodischen Systems gilt jedoch als Gesetz, daß eine größere Zahl als 8 bei einem Atom nicht möglich ist; es ist dies 3 ein anderer Ausdruck für die Erfahrungstatsache, daß an einem Atom der ersten Reihe sich nie mehr als vier einwertige Substituenten befinden können.
Diese Erfahrung ist wichtig für die Übertragung der Elektronenschreibweise von einfachen auf mehrfache Bindungen. Ehe darauf eingegangen sei, soll zuvor der Begriff der mehrfachen Bindung etwas genauer betrachtet werden. Die hierunter fallenden Bindungsarten, Doppelbindung und dreifache Bindung, sind ursprünglich aus systematischen Gründen zwischen zwei Kohlenstoffatomen angenommen worden; dann hat man entsprechende Vorstellungen auf Bindungen von Kohlenstoff mit Sauerstoff, Schwefel und Stickstoff anzuwenden versucht und sie schließlich auch mit einer gewissen Unbedenklichkeit ganz allgemein au!" Bindungen zwischen allen möglichen Atomen übertragen. Das hat letzten Endes zu einer "anorganischen Strukturchemie" geführt, in der Formeln wie

die Struktur wiedergeben sollen. Eigentlich bedeuten sie nichts weiter, als ein Abzählen der Wertigkeiten und damit der siel; betätigenden Valenzelektronen mit Hilfe des Schemas der Strichvalenz. Da man in diesem Schema keine Aufteilung des Striches vornehmen kann, müssen die Formeln so geschrieben werden, daß die von jedem Atom ausgehenden Striche ihrer Zahl nach gleich seiner Wertigkeit sind, genau so, wie dies beispielsweise für die C = C-Doppelbindung gilt. Es ist aber verfehlt, daraus herzuleiten, daß die Art der Atombindung etwa zwischen "doppelt gebundenem" Schwefel und Sauerstoff, oder Phosphor und Sauerstoff im Grunde genommen dieselbe sei wie etwa zwischen zwei doppelt gebundenen Kohlenstoffatomen, so naheliegend dieser Schluß vom systematischen Standpunkt aus auch ist. Von chemischen Gesichtspunkten aus ist er nicht gerechtfertigt. Denn der Chemiker verknüpft mit dem Begriff der doppelten Kohlenstoff-Kohlenstoffbindung die besondere, im Additionsvermögen zum Ausdruck kommende Reaktionsfähigkeit. Wohl findet man diese, wenn auch modifizierte, in den Verbindungen wieder, die man mit Kohlenstoff-Sauerstoff-Doppelbindung schreibt, wie den Aldehyden und Ketonen, ebenso in den Verbindungen mit mehrfacher Kohlenstoff-Stickstoffbindung, wie den Oximen und Nitri- len. Nicht dagegen tritt eine solche Fähigkeit zur Anlagerung in den Sulfoxyden und Sulfonen, sehr selten in den Nitroverbindungen in Erscheinung; diese Verbindungen haben keine Nei- l>ung, ihre "Doppelbindungen" unter Bildung zweier einfacher Bindungen durch Anlagerung aufgehen zu lassen. Die Nichtberücksichtigung dieses Umstandes hat mit dazu beigetragen, daß die Bedeutung der anorganischen Strukturformeln zeitweilig bedeutend überschätzt wurde.
Übungen zum Wortschatz
0 b u n g 1. Übersetzen Sie.
fordern, fördern, zurückführen auf etwas, eingehen auf «•(was, rechtfertigen, gerechtfertigt; etwa, nie, eigentlich, obwohl, nichts weiter, als...; unter Umständen, im Grunde genommen, .ms systematischen Gründen; immer strenger, immer lockerer, immer seltener.
1. Das Massenwirkungsgesetz gilt ausnahmsweise für alle Reaktionen. 2. Die Grenzkohlenwasserstoffe werden auch als Paraffine bezeichnet, weil sie früher als sehr reaktionsträge gal- len (lat.: parum — мало, affine—находящийся в родстве). II. Das Gesagte gilt für die Doppelbindung. 4. Nicht alle Valenzelektronen betätigen sich. 5. Zur Bindung werden zwei Elektronen benötigt. 6. Die Arbeiten von Lewis trugen zur Entwicklung der Strukturlehre bei. 7. Wir haben es hier mit einem besonderen Fall der Störung der Depolarisation zu tun, auf den hier nicht weiter eingegangen zu werden braucht, da er im letzten Ab- •chnitte einer gesonderten, eingehenden Untersuchung unterzogen werden wird. 8. Für die Anwendung der Methode auf IWichtige Lösungsmittel ist eine Vorsättigung des Trägergasstro- ities naheliegend, die sich bereits in ähnlichen Fällen zur Bestimmung physikalisch-chemischer Größen bewährt hat. 9. Es lag nahe, das empfindliche Chloratom durch organische Reste zu ersetzen.
• 1 b ti n g 2. Sagen Sie deutsch.
а) все электроны, рыхло связанные электроны, четная ва- И'нтность, ограниченное число, склонность к образованию •■мета, с точки зрения органической химии.
б) 1. О чем идет речь в тексте? 2. Речь идет о понятии ипЛентности. 3. О чем шла речь выше? 4. Речь шла о струк- Iурпых формулах. 5. О чем пойдет речь ниже (дальше)? 0. Речь пойдет о химической связи.
в) 1. Мы пытаемся дополнить схему. 2. Я пытаюсь связать оба представления. 3. Пытались сохранить этот способ написания. 4. Пытаются оправдать вывод. 5. Они пытались выразить структуру формулами. 6. Какой метод Вы пытаетесь применить?
GRUNDTEXT 6.
DIE GESTALT DER SCHMELZKURVE
Im Gegensatz zur Dampfspannungskurve, über deren Verlauf und Eigenschaften man sich auf experimentellem Wege Gewißheit verschaffen konnte, ist man bei der Erforschung der Schmelzkurven durch die begrenzten Festigkeitseigenschaften der zum Bau von druckfesten Gefäßen in Frage kommenden Stoffe, zumal bei hohen Temperaturen, auf die Untersuchung niedrigschmelzender Stoffe und auch bei diesen auf ein Druckgebiet beschränkt, welches, gemessen an den Drucken, denen die Stoffe im Innern der Weltkörper ausgesetzt sein können, verschwindend klein ist.
Für kleine Drucke bis zu 3000 Atm. kann die Gleichung der Schmelzkurve nach G. Tammann in der Form
![]()
geschrieben werden, da in diesem Gebiet QP, die Schmelzwärme bei konstantem Druck, sich praktisch nicht ändert und TAv linear vom Druck abhängt.
G. Tammann hat Vorstellungen über den weiteren Verlauf und die Gestalt der Schmelzkurve entwickelt. Es ergibt sich in gekürzter Darstellung derselben folgendes Bild.
Wenn man die Frage erörtern will, ob die Schmelzkurve ähnlich wie die Dampfspannungskurve der Flüssigkeit einen kritischen Endpunkt besitzt, so könnte hierüber entschieden werden, wenn es gelingt, nachzuweisen, daß die Volumenänderung beim Schmelzen und die Schmelzwärme in ein und demselben Punkt der Schmelzkurve Null werden. Die experimentellen Befunde sind aber dahin zu deuten, daß dies nicht der Fall ist, denn, wie schon erwähnt, und wie aus den Daten der Tabelle zu entnehmen ist, ändert sich mit steigendem Druck die Schmelzwärme nur sehr wenig, die Volumendifferenz zwischen Schmelze und Kristall nimmt erst schneller, dann langsamer ab und wenn sie Null wird, während die Schmelzwärme einen endlichen Wert besitzt, so muß die Tangente an die Schmelzkurve parallel der Druckachse gerichtet sein, die Schmelzkurve muß ein Temperaturmaximum, der Stoff also bei diesem Druck einen maximalen Schmelzpunkt besitzen.
Ein Beispiel für den experimentell gelungenen Nachweis des
Temperaturmaximums der Schmelzkurve ist das Glaubersalz (vgl. jedoch weiter unten).
Kommt man in das Druckgebiet oberhalb des Temperaturmaximums der Schmelzkurve, wo die Volumenänderung das umgekehrte Vorzeichen hat, so erhält man die Verhältnisse, wie sie beim Eis und beim Wismut schon bei gewöhnlichem Druck vorliegen, die Kurve hat die in der Abbildung mit 2 bezeichnete Richtung, und die Steigerung des Druckes bewirkt jetzt eine Erniedrigung der Schmelztemperatur.
Wird unter diesen Verhältnissen die Schmelzwärme nach tiefen Temperaturen zu kleiner und schließlich Null, während die Volumendifferenz einen endlichen negativen Wert behält, so wird dadurch auch noch ein — allerdings noch nicht realisiertes— Druckmaximum möglich und die Schmelzkurve wird ohne kritischen Endpunkt schließlich dem absoluten Nullpunkt zustreben. Das nach G. Tammann sich so ergebende Bild der Schmelzkurve ist in der Abbildung wiedergegeben.
Texterläuterung
... wie sie . . . — которые
... dahin . . . daß — в том смысле, что ...; так, что ...
Übungen zum Wortschatz Übung 1. Übersetzen Sie.
1. Das Gefäß ist dem Druck ausgesetzt. 2. Das Volumen nimmt ab. 3. Es werden die experimentellen Befunde erörtert. 4. Bewirkt die Steigerung des Druckes eine Erniedrigung der Schmelztemperatur? 5. Man stellt fest, daß es Lösungen von Elektrolyten gibt, bei denen z. B. die Leitfähigkeit proportional der Ionenzahl ist und andere Lösungen, bei denen dies nicht der Fall ist. 6. Der Verlauf der Kurve wurde von mehreren Forschern gedeutet.
О b u n g 2. Sagen Sie deutsch.
Мы ограничимся небольшим давлением. 2. Кривую упругости пара можно получить экспериментальным путем. 3. Для пиита нам нужны сосуды, выдерживающие давление (прочные на сжатие). 4. Он измеряет давление. 5. От чего зависит давление? 6. Здесь следует упомянуть исследования Таммана. 7, Получается следующее уравнение.
GRUNDTEXT 7.
MESOMERIE DER ANIONEN TAUTOMERER STOFFE
Wie man auch im einzelnen den Vorgang bei der Umsetzung einer Metallverbindung auffaßt, eins ist sicher: Bei der Reaktion wird das Metall zum Kation. Dieses Kation ist je nach der Elektronenaffinität des mit dem Metall verbundenen organischen Restes und der Natur des Metalls mehr oder weniger genau in der festen Metallverbindung vorgebildet. Es kann sich einmal in dem bei der Reaktion verwendeten Lösungsmittel vor der Reaktion bilden; dann liegt der Fall der elektrolytischen Dissoziation vor, und was reagiert, ist dann nicht die Metallverbindung, sondern ihr Anion — das Metallkation spielt dabei ebensowenig eine Rolle wie beispielsweise das Natriumion bei der Neutralisation der Natronlauge. Oder aber es kann sich, falls das Lösungsmittel eine elektrolytische Dissoziation nicht zu bewirken vermag, das Metallkation aus der nicht dissoziierten Metallverbindung, sei es, daß diese gelöst oder in fester Phase vorliegt, mit Halogen oder einem Säurerest zusammen als festes heteropolares Salz aus der Lösung ausscheiden. Wie dem auch sein mag, irgendwie tritt das nach Ablösung des Metalls hinterbleibende organische Anion in Erscheinung, und dessen Umsetzung führt zum organischen Reaktionsprodukt. Worüber man noch streiten kann, ist die Frage, ob, den eben skizzierten beiden Möglichkeiten entsprechend, das freie Anion durch das Lösungsmittel oder erst durch Angriff des mit der Metallverbindung reagierenden Stoffes geschaffen wird. Auf diese Frage soll hier nicht näher eingegangen werden, weil Versuche, die darüber zu entscheiden gestatten würden, nicht vorliegen.
Das Anion ist dasselbe, welches nach Ablösung des Protons aus der entsprechenden Wasserstoffverbindung übrig bleibt. Da es nun zwei Wasserstoffverbindungen gibt, und das Anion genau so wie das Metallkation in der festen Metallverbindung mehr oder weniger streng vorgebildet ist, so ist es das Nächstliegende, für das Anion dieseble Tautomerie wie bei der Wasserstoffverbindung anzunehmen und damit, wenn schon keine tautomeren Formen bei der Metallverbindung zu fassen sind, wenigstens solche beim Anion als möglich anzusehen. Beim Anion des Natrium-acetessigesters würde dann bei der einen Form des Anions die negative Ladung am Sauerstoff, bei der andern am Kohlenstoff sitzen:

Wie man ohne weiteres sieht, ist die Reihenfolge der Atome in beiden Formeln genau die gleiche, nur die Bindestriche und die elektrische Ladung, das heißt also, die Verteilung der Elektronen ist eine andere. Durch diese Formeln würde mithin ein viel feinerer Unterschied zum Ausdruck gebracht werden als durch die gewöhnlichen Strukturformeln.
Texterläuterung
wie dem auch sein mag — как бы (там) ни было
Übungen zum Wortschatz
llbung 1. Übersetzen Sie.
ansehen als, bewirken, eingehen auf etwas, entscheiden über rtwas, zum Ausdruck bringen, in Erscheinung treten; ein feinerer I Interschied, ein stärkerer Angriff, eine nähere Besprechung; ohne weiteres, je nach, eben, oben, im einzelnen, wenigstens.
b u n g 2. Sagen Sie deutsch.
1. Процесс рассматривают как электролитическую диссоциацию. 2. Катион металла может выделиться из раствора в миле соли. 3. О чем спорят? — Спорят о формулах. 4. Здесь имеется различие.
GRUNDTEXT 8.
ELEMENTARE BERECHNUNG DES Я-KOEFFIZIENTEN
Der Koeffizient B, der in erster Linie die Abweichungen im thermischen Verhalten des realen Gases von dem eines idealen (Itises beschreibt, wird in nicht recht glücklicher Weise als zwei- ior Virialkoeffizient bezeichnet. Diese Bezeichnung ist historisch dadurch bedingt, daß die erste theoretische Ableitung der Tempel nturabhängigkeit des Koeffizienten В durch eine Verbindung df* Moltzmannschen e-Satzes und des Gleichverteilungssatzes mit dem Virialsatz der Mechanik gelang. Während aber die tfltcn beiden Sätze in dieser, bzw. in einer entsprechenden ande eu l'orm der statistischen Mechanik oder der kinetischen Gas- lllrorie einen wesentlichen Bestandteil dieser Ableitung darstellen. erweist sich die Verwendung des Virialsatzes nur als eine Min vielen Möglichkeiten zur Gewinnung der thermischen Zu- «limilsglcichung für reale Gase.
Zwei von diesen Möglichkeiten sollen im folgenden ausführliche! besprechen werden, zumal sie in der hier gebrachten Form мин Teil neue Gesichtspunkte und Überlegungen enthalten. (Jlelclizeitig soll gezeigt werden, wie man bei diesen zunächst Imi Kähmen der klassischen Physik durchzuführenden Betrachtungen allenfalls erforderliche Quantenkorrekturen berücksichtigen kann. Und schließlich sollen die so gewonnenen ß-Formeln illnkutlert und kurz mit experimentellen Ergebnissen verglichen werden.
Als erste Methode zur Berechnung des ß-Koeffizienten (ohne Mniul/.ung des Virialsatzes) soll ein Verfahren angegeben wer- Я1Н1, welches unter Vermeidung diffiziler statistischer oder kine- II-" Ihm Betrachtungen an eine von Boltzmann entwickelte Vor-
Stellung anknüpft und, hinausgehend über die in der Literatur enthaltenen, fast stets im Qualitativen endenden sogenannten elementaren Begründungen der van-der-Waals-Korrekturen, in durchaus elementarer Weise bis zu einer quantitativ gültigen Schlußformel führt.
Die für ein ideales Gas wohlbekannte Beziehung p—nwkT muß auch für ein reales Gas gelten, da weder die Bernoullische1Ableitung noch der Gleichverteilungssatz durch die Existenz von van der Waalsschen Kräften beeinflußt werden. Zu einem Unterschied in der Zustandsgieichung zwischen einem idealen und einem realen Gas kommt man somit nur durch die Annahme, daß bei letzterem die Gasdichte unmittelbar an der Gefäßwand von der im Gasinnern mehr oder minder stark abweicht. Die Aufgabe besteht daher in der rechnerischen Ermittlung dieses Dichteunterschiedes.
Anschaulich ist dieser Unterschied unmittelbar verständlich, sofern zwischen den einzelnen Gasteilchen Anziehungskräfte wirksam sind. Während sich nämlich diese Kräfte im Gasinnern aus Symmetriegründen im Mittel gegenseitig aufheben, bleibt in der Randzone eine resultierende Kraft übrig, welche die dort befindlichen Gasteilchen ins Innere zu ziehen sucht und dadurch die Randdichte verringert. Umgekehrt bewirken Abstoßungskräfte eine Erhöhung der Randdichte. Zu einer solchen Erhöhung kommt es aber auch beim Fehlen von Kräften endlicher Reichweite allein durch die Ausdehnung der Gasteilchen, indem nach Boltzmann dem einzelnen Gasteilchen am Rande etwas mehr Platz zur Verfügung steht als im Innern. Man denke sich, um sich dies klarzumachen, im Gasinnern eine ebene Fläche gelegt und vergleiche nun den Einfluß dieser Fläche auf die Lagemöglichkeiten der ganz links von ihr befindlichen Teilchen, wenn man einmal zuläßt, daß die weiter rechts liegenden Teilchen die Wand durchdringen können, und wenn man zum anderen Male diese Fläche als völlig undurchdringlich ansieht. Formal kann man diesen Fall von Gasteilchen endlicher Größe ohne sonstige Wechselwirkung aber auch aus der Vorstellung gewinnen, daß zwischen den Teilchen eine sehr starke Abstoßungskraft wirksam wird, sobald sie sich einander bis auf einen bestimmten Minimalabstand annähern. Im folgenden soll daher der Kürze halber der Fall endlich
großer Gasteilchen ohne sonstige Kraftwirkung aufeinander stets nur in diesem letzteren Sinn zusammen mit dem Fall der Existenz weiterreichender van-der-Waals-Krafte behandelt werden.
Um nun den Dichteunterschied im Gasinnern und unmittelbar an der Wand zu ermitteln, sei an den Boltzmannschen e-Satz erinnert, nach welchem die Teilchendichte an irgendeiner Stelle proportional ist der Exponentialfunktion mit der negativen, dort
Iifltohenden potentiellen Energie, noch geteilt durch kT als Expo- iH ilten. Nun kommt es aber bloß auf die mittlere Teilchendichte iin, wobei die Mittelung über Bereiche zu erstrecken ist, die *olbst noch viele Teilchen enthalten. Da die van-der-Waals-Kräfte «Wischen zwei Teilchen, beschrieben durch potentielle Energie iln Funktion des Abstandes der beiden Teilchen, im allgemeinen mit zunehmendem Abstand sehr rasch abfallen, wird sich bei nicht zu dichten Gasen ein herausgegriffenes Teilchen vorwie- upnd im feldfreien Raum befinden, wo die Exponentialfunktion
den Wert I besitzt.
Die Diskussion der Formel möge auf später verschoben werden. Hier sei nur noch erwähnt, daß bei der hier gegebenen Ableitung die Fälle vernachlässigt wurden, bei denen das herausgegriffene Teilchen gleichzeitig in die Wirkungssphäre von zwei ОПТ mehreren Teilchen gerät; die Berücksichtigung dieser Fälle würde dann zu den höheren Korrekturgliedern in der Reihenentwicklung führen. Ebenfalls ohne Beweis sei erwähnt, daß eine allfalige Anziehungskraft der Wand auf die Gasteilchen, welche zweifelsohne die Randdichte erhöht, keinerlei Einfluß auf die (irftüe des ß-Koeffizienten besitzt.
Übungen zum Wortschatz
Übung 1. Übersetzen Sie.
ableiten, entwickeln, sich annähern, vernachlässigen, sich denken, ermitteln, sich erweisen, sich gegenseitig aufheben, anknüpfen an etwas, einen Fall behandeln, zur Verfügung stehen, niclien + zu+Infinitiv; die Abweichung, der Satz, die Existenz, die Zunahme, der Wert, die Reichweite, ebene Fläche," das eben < iesagte; oben, durchaus möglich, gültig, recht ausführlich, vor- u legend, aus Symmetriegründen, halber, sofern.
вычислять, обусловливать, избегать, существовать, отыскивать, принимать (предполагать), делить на . .. (матем.), I равнивать; уменьшение, результат; наглядно, в первую очередь, ради краткости, в общем, слишком трудно; соответство- иить, соответствующее правило, соответственно рисунку.
1. Es kommt zu einer starken Abstoßung der Teilchen.
Vor einer quantitativen Behandlung des Absorptionsvorganges sind noch zwei wichtige Punkte zu klären, nämlich erstens die I läge nach den Besetzungszahlen der durch das Magnetfeld aufgespaltenen Energieniveaus und zweitens die Relaxationser- »eheinungen beim Ubergang der Kerne in ihre stationären Zutände. 3. Bei den Leuchtstofflampen ist die Innenwand mit einem Leuchtstoff bestrichen, der die unsichtbaren ultravioletten Strahlen des angeregten Quecksilberdampfes in sichtbares Licht umsetzt. Nach dem Stokesschen Gesetz über die Fluoreszenz ist nämlich die Wellenlänge des ausgesandten Lichts größer als die des eingestrahlten. 4. Es kommt bei der Bestimmung der Zersetzungsspannung weniger darauf an, den Absolutwert von i zu kennen, als vielmehr seine Änderung mit steigender polarisierenden EMK. 5. Wenn es nur auf die positiven Sauerstoffatomionen ankäme, so dürfte mit der "Gaskathode" überhaupt keine Carosche Säure in der Flüssigkeit auftreten. 6. Die magnetische Kernresonanzmethode wird aus zwei Gründen besonders zur Ermittlung von Protonenabständen in Kristallgittern herangezogen. Einmal ist hier die Empfindlichkeit der Methode maximal, und zum anderen kann gerade bei Protonen wegen der geringen Beugung von Röntgenstrahlen nur schwierig die Lage dieser leichten Kerne im Gitter mit der klassischen Röntgenmethode bestimmt werden.
Ü b u n g 2. Sagen Sie deutsch.
1. Это отношение действительно только для идеального газа. 2. Поведение газа термически обусловлено. 3. Выведение формулы весьма сложно. 4. Был разработан новый метод.
На частицы газа оказывают влияние силы притяжения.
Сила притяжения стенки влияет на величину коэффициента.
Расстояние между частицами влияет на силу отталкивания.
Мы должны установить разницу плотностей. 9. Частицы могут проникать через стенку. 10. Газ проникает через поверхность? 11. По каким причинам силы притяжения взаимно уничтожаются? 12. Какие силы вызывают повышение плотности по краям? 13. Ради простоты мы пренебрегаем этой разницей.
GRUNDTEXT 9.
DER BINDUNGSZUSTAND IN KONJUGIERTEN SYSTEMEN
Es fragt sich nun, ob man für den besonderen Bindungszu- stand, den man im allgemeinen nur als vorübergehenden bei Reaktionen annehmen kann, eine besondere Schreibweise einführen soll oder nicht. Eine Notwendigkeit zur Einführung neuer Symbole wäre erst gegeben, wenn in irgendeinem Falle der neuartige Bindungszustand stabilisiert erschiene.
Von dieser Notwendigkeit war Thiele nach seinen ersten umfangreichen Untersuchungen über die Additionen an konjugierten Systemen überzeugt. Denn für ihn galt damals die 1,4-Addi- tion als Gesetz; es schien ihm daher der besondere Bindungszustand im konjugierten System sich in allen Reaktionen auszudrücken, von verschwindend seltenen Ausnahmen bei unsymmetrisch gebauten Systemen abgesehen. Er mußte daher für diesen, von ihm als normal betrachteten Zustand nach einer Schreibweise suchen. Nur aus dem Glauben Thieles an die Allgemeingültigkeit der 1,4-Addition heraus läßt sich sein Schritt, diese Schreibweise mit dem Versuch einer umfassenden Theorie zu verbinden, verstehen. Nach dem damals vorliegenden Material »chlen tatsächlich die Allgemeinheit der 1,4-Addition beim konjugierten System für fast alle Reaktionen gesichert, die unterzieht worden waren — besonders für die Addition von nascieren- ilrin Wasserstoff und für die Addition von Brom; daß die Kon- itltutlon der ungesättigten Dibromide wegen der Allylumlage- ГШ1В nicht richtig ermittelt worden war, hat sich erst viel später herausgestellt. Fälle, die sich auf den ersten Blick anscheinend Dicht einordneten, wie die Reaktion a, ß-ungesättigter Ketone, llrlien sich mühelos deuten, wenn man eine sehr einleuchtende Unilagerung der 1,4-Additionsprodukte und damit einen Reaktionsverlauf annahm, der sich bei der Reduktion des Benzils Hatte experimentell beweisen lassen. Einige Ausnahmen, die tfolzdcm bestehen blieben, zeigten freilich immerhin schon so Viel, daß gelegentlich auch Additionen im Sinne der gebräuchlichen Formeln erfolgen können; doch beschränken sie sich, wie »chon erwähnt, auf das unsymmetrisch gebaute System C~C—C = 0. Thiele glaubte sich berechtigt, sie mit einem kurzen Hinweis auf die verschiedene spezifische Verwandtschaft (Irr sich addierenden Atome zu Kohlenstoff und Sauerstoff vorläufig beiseite lassen zu dürfen, um erst einmal eine Anschauung über 1,4-Addition von allgemeinen Gesichtspunkten aus gewinnen zu können.
Ohne zunächst auf die theoretischen Betrachtungen Thieles, mit deren Hilfe er eine Erklärung für die 1,4-Addition geben zu kftnnen meinte, Rücksicht zu nehmen, soll dem heutigen Stande (Irr Kenntnisse entsprechend die von Thiele eingeführte Schreibweise, möglichst vom hypothetischen Beiwerk befreit, betrachtet werden.
Übungen zum Wortschatz
Ü b u n g 1. Übersetzen Sie, indem Sie die partizipiale Wendung
"abgesehen von..." gebrauchen.
1. Если не говорить о введении новых символов ... 2. Не говоря об исследованиях реакций присоединения ... 3. Если in бросить несимметрично построенные системы ... 4. Если не говорить о немногих исключениях . ..
Ü b u n g 2. Bilden Sie von den gegebenen Verben Substantive
und übersetzen Sie diese. i ischeinen, überzeugen, ausdrücken, vorliegen, ermitteln, deuten, beweisen, meinen, sättigen, verlaufen, erwähnen, gewinnen, annehmen, ausnehmen.
Ü b u n g 3. Übersetzen Sie.
1. Er meinte den Reaktionsverlauf richtig gedeutet zu haben. 2. Sie behaupteten, die Atomverwandtschaft nachgewiesen zu haben. 3. Er glaubt, einen besonderen Bindungszustand zu untersuchen.
GRUNDTEXT 10.
ALLGEMEINES UBER WALDENSCHE UMKEHRUNG
Die sterischen Umlagerungen, soweit sie durch thermische Einflüsse hervorgerufen werden oder als Folge von chemischen Reaktionen auftreten, die sich fern vom die räumliche Anordnung festlegenden Zentrum abzuspielen scheinen, vollziehen sich, soweit sichere Erfahrungen reichen, nicht durch unmittelbares Umklappen der Substituenten an diesem Zentrum in eine andere räumliche Lage. Ausnahmen erscheinen nicht ausgeschlossen, sind aber sicher sehr selten. Eine genaue Untersuchung der Umlagerungsbedingungen und des Verlaufs der Um- lagerungsreaktionen führt vielmehr zu dem Schluß, daß bei den Konfigurationsänderungen das betreffende Asymetriezentrum bzw. die Doppelbindung durch unmittelbaren Angriff auf die damit verbundenen Atome, sei es durch Substitution, sei es infolge der Möglichkeit einer tautomeren — also strukturellen — Umlagerung, in Mitleidenschaft gezogen wird, selbst wenn sich dieser unmittelbare Angriff aus dem Vergleich der Konstitution des Ausgangs- und Endproduktes nicht entnehmen läßt. Nach diesen Erfahrungen erscheint die Prüfung der Frage besonders wichtig, ob sich die räumliche Anordnung der Atome bei einem Angriff erhalten wird, der sich schon nach der formelmäßigen Darstellung auf das Zentrum der Stereoisomerie richtet, also bei Substitutionen an einem Asymmetriezentrum und bei Additionen an eine Doppelbindung. Das Prinzip der möglichst geringen Strukturänderung bei chemischen Reaktionen, auf diese Fälle übertragen, würde besagen, daß bei Substitutionen der Substi- tuent an den Platz seines Vorgängers tritt; das ist die wörtliche Auffassung des Begriffs "Substitution". Bei der Addition an mehrfache Bindungen müßten sich, wenn man das van't Hoffsche Modell den Betrachtungen zugrunde legt, die Atome in ds-Stel- lung anlagern, wenn man bei der Anlagerung eine der beiden Bindungen unberührt läßt:
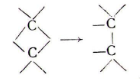
Wenn diese einfachen mechanischen Bilder für den Vorgang der Substitution und der Anlagerung zutreffen würden, wäre es möglich, Konfigurationsbestimmungen auf dieser Grundlage durchzuführen. In den Entwicklungsjahren der Stereochemie hat man dies unbedenklich tun zu dürfen geglaubt in Anbetracht der großen Leistungsfähigkeit, welche die mechanischen Modelle bei der Erklärung der Zahl von Isomeren zeigten, ohne zu bedenken, daß es sich bei der Erklärung des räumlichen Verlaufs * ' i Reaktionen um eine Anwendung der Modelle auf einem Ürblele handelte, für das sie ursprünglich nicht geschaffen wann, da sie nur die Lage der Atome im fertigen, ungestörten Molekül wiedergeben sollten. Doch hätte schon damals ange- ii Iiis der verschiedenen, bereits bekannten strukturellen Um- 1 (In ningen, die zur Vorsicht sogar bei Strukturbestimmungen malmten, eine kritische Einstellung angezeigt erscheinen können. Drt aber — wie man heute weiß, durch Zufall — einige besonders yi lindlich studierte Fälle sich widerspruchsfrei in diese Art der KiHifignrationsbestimmung fügten, nämlich die Permanganat- "ivdation der Fumarsäure zur Traubensäure und der Malein- •Wiirc zur Mesoweinsäure, wurde eine dahin gerichtete systema- Unchc Untersuchung nicht in Angriff genommen, und es blieb in Zufall überlassen, daß schließlich im Jahre 1895 Unter- »ucliungen von Waiden die Nichtanwendbarkeit des genannten Prinzips bei Substitutionsreaktionen erkennen ließen. Die Uraiichbarkeit des Prinzips war zwar schon vorher anläßlich von l'.lii/.elfällen in Zweifel gezogen worden; dies hatte bereits Baeyer IK8H in aller Klarheit zum Ausdruck gebracht. Das erste Beispiel «Infiir, daß ein Substituent nicht, dem Sinne des Wortes "Substi- llltlon" entsprechend, an die Stelle seines Vorgängers zu treten braucht, ist freilich schon im Jahre 1879 von Zincke aufgefunden •forden. Daß auch bei Additionsreaktionen an Doppelbindungen ilnri Prinzip der möglichst geringen Struktur—hier also Kon- llgurationsänderung— nicht anwendbar ist, ergaben umfassende I iiitorsnchungen von Michael, der in vielen Fällen neben Anlage- ■ nngcn in c/s-Stellung auch ganz oder teilweise in frans-Stellung i rfolgcndc Anlagerungen nachwies.
Texterläuterung
in Mitleidenschaft ziehen — зд. затрагивать
Übungen zum Wortschatz
Ü b u n g 1. Übersetzen Sie.
reiche Erfahrungen, das betreffende Atom, eine unberühr- li Bindung; die Umlagerungen vollziehen sich ...; der Vergleich iler Ausgangs- und Endprodukte ergab ...; das Modell trifft nicht 'ii. den Betrachtungen wurde ein anderes Prinzip zugrunde uelegt. sie glaubte eine widerspruchsfreie Erklärung gegeben zu Iiiihcn, die Umlagerungen brauchen nicht durch thermische Ein- Hnsso hervorgerufen zu werden; brauchen Sie einen Beweis dafür?
fonnelmäßig, zweckmäßig, beispielmäßig, planmäßig, mengenmäßig, zahlenmäßig, erfahrungsmäßig, regelmäßig;
33
пространственное расположение, общие исследования, непосредственное воздействие, известное понятие, кратная связь;1. Закон гласит ... 2. Сама реакция протекает ... 3. Даже простое исследование показывает ... 4. Даже исключения подтверждают ... 5. Сама возможность перегруппировки приводит к выводу, что ...
1. Перегруппировка происходит (совершается) у асимметрического центра. 2. Первоначальное положение атомов сохраняется. 3. Речь идет об исключении. 4. Он доказал непригодность принципа. 5. Нам нужна механическая модель.
GRUNDTEXT 11.
DIE GRENZFLÄCHE VON FLÜSSIGKEITEN UND FESTKÖRPERN
GEGEN GASE
Die bisherigen Betrachtungen galten Oberflächen, d. h. Grenzflächen gegen den stoffleeren Raum. Es war dabei aber stets bewußt, daß es solche Oberflächen als Gleichgewichtsformen der Stoffe grundsätzlich bei endlichen Temperaturen nicht gibt. \Y.:< an chemisch einheitlichen flüssigen und festen Stoffen als Grenzfläche beobachtet wird, ist vielmehr stets die Grenzfläche gegen den eigenen Dampf. Unter Vorwegnahme der Erkenntnis, gs!5 die Grenzflächenenergie gegen den leeren Raum sich von derjenigen gegen den eigenen Dampf, wenigstens solange der Dampfdruck nicht abnorm groß ist, und von derjenigen gegen— in bezug auf den betrachteten Stoff chemisch indifferente — Gase, wenigstens bei Drucken bis zur Größenordnung der Atmosphäre, nur unmerklich unterscheidet, konnten wir die Grenzflächenspannung gegen den eigenen Dampf bzw. gegen Luft und ähnliche Gase kurzweg als Oberflächenspannung ansehen.
Daß aber die Grenzflächenspannung gegen angrenzende Gase und Dämpfe grundsätzlich von der Oberflächenspannung im strengen Sinne zu unterscheiden, und zwar stets kleiner als diese anzusehen ist, lehrt schon die einfache Fortführung der Überlegung, die uns eingangs unserer Betrachtung das Wesen der die Grenzflächenspannung verursachenden Kräfte verstehen lehrte: Ein Molekül, das aus dem Innern einer Flüssigkeit oder eines Festkörpers an die Oberfläche kommt, wird dem Einf.uß eines Teils der ihm artgleichen, mit ihm durch zwischenmolekulare Anziehungskräfte verbundenen Nachbarn entzogen; seine Uberführung in die Oberfläche ist also mit einer Potentialerhöhung, d. h. mit Aufwand von Arbeit verbunden, die, auf die Flächeneinheit bezogen, das Maß der Oberflächenspannung gibt. Sind nun aber jenseits der die Flüssigkeit oder den Festkörper begrenzenden Fläche ebenfalls Moleküle vorhanden, sei es des eigenen Dampfes, sei es eines artfremden Gases, so wird ein Molekül beim Ubergang in die Grenzfläche zwar der Einwirkung der Nachbarn im gleichen Maße entzogen wie beim Ubergang llt dir Oborfläche gegen den stoifleeren Raum, tritt aber dort mit Molekülen des angrenzenden Raumes in neue Wechselwirkung, die entsprechend einer zwischenmolekularen Anziehung einen It'il des mit dem Austritt aus dem Innern der Flüssigkeit МИГ des Festkörpers verbundenen Potentialgewinnes wieder iMfnpcnKiert. Die zur Überführung in die Grenzfläche aufzuwendente Arbeit, d. h. aber die Grenzflächenspannung ist also not- Mndlg KU iner als die auf Vakuum als Grenzilächenpartner Имоц. п.- С er flächen Spannung.
Im Versuch läßt sich das mit der bereits früher angegebenen AnordtuiTiL; zum Nachweis des Krümmungsdruckes unmittelbar hostatiger: In dem am Boden mit einem feinen Loch versehenen Reagenzglas habe sich die Wassersäule auf die durch die Ober- Hachenpannung des Wassers bestimmte Gleichgewichtshöhe Bringen wir nun unter das Reagenzglas ein Schälchen mit Äther, so daß der an der Öffnung hängende Halbtropfen en eine mit Ätherdampf gesättigte Atmosphäre grenzt, so beginnt das Wnsser alsbald von neuem abzutropfen, bis die dem neuen, tlncr verringerten Grenzflächenspannung entsprechenden Gleichgewicht zugehörige Höhe der Flüssigkeitssäule erreicht ist. Bei Eintauchen des unteren Reagenzglasendes in den flüssigen Äther wiederholt sich das gleiche Spiel; die sich nunmehr einstellende, abermals geringere Höhe der Wassersäule zeigt die gegenüber der Grenzfläche Wasser-Ather-Dampf abermals geringere Grenz- Hachenpannung Wasser-fliissiger Äther an. Auch dieser Befund tffscheint im Sinne unserer Überlegung verständlich. Die Kon- IWtrittlon des Äthers in der mit seinem Dampf gesättigten AlBIOiphi'ire ist verhältnismäßig gering. Die durch Wechsehvir- Mlltu der in der Grenze befindlichen Wassermoleküle mit Ather- HNlirMlIeii des Dampfraumes bedingte Verminderung des Ober- IIIHleiipolcntials ist also nur klein. Grenzt das Wasser dagegen an WUnluen Äther, so tritt jedes Wassermolekül an der Grenze «Mit Allierrnolekülen in Wechselwirkung; die Potentialverminde- ншц diireli den flüssigen Äther ist dementsprechend größer als ilvJPMlU1' durch den Dampf.
So einfach dieser Versuch erscheint, so komplex erweisen «Ii Ii Inden die in ihm zutage tretenden Erscheinungen gegenüber llnir (inantitativen Auswertung. Der Äther wird, wenn er mit dem Wasser in Berührung kommt, in diesem bis zur Sättigung baw, bis zu der durch den Druck des Dampfes bestimmten Lös- HcliKell irolöst. Was gemessen wird, ist also nicht mehr die Grenzflachenpannung von Wasser gegen Äther bzw. flüssigen AlltH, mindern die Grenzflächenspannung einer wäßrigen Lösung tili! Alliei gegen den Dampf oder gegen den flüssigen Äther. Hinzu Kommt, und das zeigt die im Vergleich zu derjenigen »tniili den flüssigen Äther relativ hohe Erniedrigung der Ober- llwhrnipimnung durch den Dampf, daß an der Grenzfläche Wasser-Äther-Dampf Äther adsorptiv angereichert wird. Damit führt unser Versuch, die Grenzflächenspannung chemisch einheitlicher Stoffe gegeneinander zu bestimmen, bereits hier in den Bereich der Lösungen und der Adsorption.
Echte Grenzflächenspannungen chemisch einheitlicher Stoffe gegeneinander werden nur in den seltenen Fällen praktisch völlig fehlender Löslichkeit und Adsorption beobachtet. Reine Werte dieser Art gegen Gase und Dämpfe sind am ehesten bei Quecksilber zu erwarten, das nichtmetallische Gase und Dämpfe im allgemeinen sehr wenig löst. Seine Oberflächenspannung gegen den stoffleeren Raum erweist sich, wenn Oxydation und die oben erwähnten, durch Verunreinigungen aus Glasgefäßen bedingten Fehler ausgeschlossen werden, von der Grenzflächenspannung gegen indifferente Gase wie Luft oder Stickstoff unter nicht zu großen Drucken als nur unmerklich verschieden, soweit Unterschiede überhaupt nachweisbar sind, gehen sie in die erwartete I Richtung, indem die Oberflächenspannung gegen den stoffarmen f Raum größer ist als die Grenzflächenspannungen. Ebenso im Sinne der theoretischen Erwartung nimmt die Grenzflächenspannung von Quecksilber gegen Luft und gegen Wasserstoff mit steigendem Gasdruck ab. Steigender COo-Gehalt der Luft bewirkt zunächst eine Abnahme, oberhalb eines COo-Gehaltes von 3% aber ein Ansteigen der Grenzflächenspannung; die starke Wirkung von C02 tritt deutlich dadurh hervor, daß in Edelgas-C02- I Gemischen fallende Quecksilbertropfen das CO? in Bruchteilen einer Sekunde selektiv in monomolekularer Schicht aufnehmen. Versuche mit organischen Dämpfen ergeben, obwohl auch sie vom Quecksilber nicht gelöst werden, insofern nicht die Grenzflächenspannung im einfachen Verstände, als diese im allgemeinen an der Grenzfläche adsorptiv angereichert werden.
Texterläuterung
Es war ... bewußt... — Было ясно ...
Übungen zum Wortschatz
Übung 1. Übersetzen Sie.
wenigstens, in bezug auf etwas, und zwar, insofern ... als;
die aufzuwendende Arbeit; die die Grenzflächenspannung verursachenden Kräfte; ein grundsätzlicher Unterschied, die eigene Oberfläche; die auf Flächeneinheit bezogene Arbeit; die zutage tretende Wechselwirkung; das mit einem Thermometer versehene Reagenzglas, die verhältnismäßig geringere Konzentration; das mit dem Äther in Berührung kommende Wasser; eine quantitative Auswertung des Befundes;
1. Das Molekül wird der Einwirkung seiner Nachbarn entzoger.. 2. Es fehlten immer noch die Elemente mit den Ordnungs-
Millen 4.4. öl, 85 und 87, die sich offenbar allen Nachstellungen Iii entziehen verstanden (Nachstellung—преследование). I, Dem Verlangen, einen Beitrag zu der Kenntnis allgemeiner iNMtxmäQIgkeiten zu liefern, nach denen sich das Verhalten der MMchlcdenen Metalle bei ihrer Verwendung als Kathode bei ■jrtrlschen Reduktionen regelt, ist die vorliegende Arbeit ent- Mf un Ren. 4. Hinzu kommt die Abnahme der Grenzflächenspan- Йпв Г). Die Untersuchungen von al-Razi galten nicht nur der QOhThei Stellung, sondern auch der Fertigung von Arzneimitteln. ■ Die oben erwähnte Überlegung gilt für einen einheitlichen Mplf, 7. Die gemachte Voraussetzung darf als zutreffend gelten. IpOblge Konstanten gelten für Beobachtungen in freier, mäßig MWegter Luft. 9. Als Nullpunkt gilt die Temperatur des schmel- itmrirn Eises.
c) Ii ii n g 2. Sagen Sie deutsch.
i. Наблюдения проводились на жидких и твердых вещест- |«Х, 2. Давление не сильно отличалось от атмосферного. 3. Мы ■ССМатриваем оба газа как индифферентные. 4. Равновесие ■рстмгнуто. 5. Пробирку погружают в жидкий эфир. 6. Уста- ИйМ.'Шнается равная высота водяного столба. 7. Вода граничит О Жидким эфиром. 8. Ошибка исключена.
о illing 3. Drücken Sie den Vorgang durch Verben aus; iiber- wtzen Sie.
S\ u * t e r. Bestimmung der Größen — die Größen werden bestimmt; Entstehung einer neuen Struktur — eine neue Struktur entsteht oder es entlieht eine neue Struktur.
Beobachtung der Oberfläche, Anziehung der Moleküle, Erhöhung des Potentials, Überführung eines Moleküls in die Oberfläche, Übergang eines Moleküls in die Oberfläche, Entzug der Elektronen, Hervortreten der starken Wirkung von C02, Aufnahme des Stoffes durch die Flüssigkeit, Nachweis des Druckes, Messung der Grenzflächenspannung.
GRUNDTEXT 12.
OBERFLÄCHENSPANNUNG UND OBERFLÄCHENKONZENTRATION
Bei der Betrachtung der Oberflächenfilme war vorausgesetzt, duli der filmbildende Stoff, wohl an der Oberfläche, nicht aber Im Innern der Flüssigkeit gelöst werde. Das ist z. B. in bezug ни! Wasser dann der Fall, wenn die Moleküle des filmbildenden Stoffes zwar eine mit dem Wasser in starke zwischenmolekulare Wechselwirkung tretende, exponierte, d. h. sterisch nicht abgeschirmte hydrophile Gruppe enthalten, mit ihren übrigen Teilen •her nur so schwache Kräfte auf es ausüben, daß, dränge das
fanze Molekül in das Innere des Wassers ein, diese trotz der die ftslichkeit befördernden Wirkung der hydrophilen Gruppe nicht ausreichen, die gegen die relativ starken zwischenmoleku Kräfte, welche die Wassermoleküle aufeinander aussüben, laren zuwendende Lückenbildungsarbeit zu leisten. Alle diese Vo au!* Setzungen treffen bei den oben eingehend behandelten Fettsi*?"aus" bis herab zur Dodecylsäure zu. Bei dieser beginnt — mit kürauren Kohlenwasserstoffkette zunehmend — die Löslichkeit unter "zerer jetzt überwiegenden Einfluß der hydrophilen Carboxilgi dem merklich zu warden Aber auch Dodecylsäure bildet, trotz r|>PPe wenn auch geringen, so doch deutlichen Löslichkeit, auf Wy"lrer' einen normalen Film aus, dessen mit der Oberflächen\vaa< asser messender Oberflächendruck pr sich gegen Änderungen der?e zu Film eingenommenen Fläche F ebenso verhält wie derjenig' vom praktisch unlöslichen höheren Glieder der homologen ti? c'er Dabei ist die zur Ausbildung des Filmes erforderliche ,Vlen^e''ie- Säure so gering, daß ohne weiteres zu erkennen ist, daft?e an Konzentration der Säure in der Oberfläche wesentlich g^ d'c ist, als diejenige im Innern der nunmehr als Lösung zu be:?r"®cr! nenden Trägerflüssigkeit. Das wird noch unmittelbarer det'ze'.cM wenn der Film nicht durch Spreitung der auf die OberM].'011' gebrachten Säure hergestellt, sondern wenn seine Ausbi |'ac'ie auf der Oberfläche einer, bei Dodecylsäure wegen deren geT, 1 c'unS Löslichkeit in Wasser, immer sehr verdünnten Lösung r>nger gewiesen wird. nach-
Es ist ilso, wenn nunmehr das Verhalten löslicher Sto der Oberfläche von Flüssigkeit behandelt werden soll, zur^[e 'n zu fragen, unter welchen Voraussetzungen und in welchem hächst die Konzentration eines in einer Flüssigkeit gelösten Stof! Maße deren Oberfläche (bzw. Grenzfläche) eine andere ist als i,.'65 'n Masse der Lösung oder, da der Oberflächendruck durc'11 der Oberflächenspannung der Trägerflüssigkeit mitbestimmt is0'1 die die Oberflächenspannung von Lösungen und die Konzent^- хУ'е оn des gelösten Stoffes in der Oberfläche von dessen Konz"3*'011 tion iti im Inneren der Lösung abhängen. Dabei ist es für-011*1"3' Betrachtung grundsätzlich gleichgültig, ob von einer fe" diese Lösung ausgegangen wird oder ob die Anreicherung des F;rtlSen stoffes von außen, etwa aus dem Dampfraum erfolgt. "remd-
Bei der Beantwortung dieser Frage kann allgemein ang, men werden, die Konzentration des löslichen Stoffes sei цепот- Masse der Flüssigkeit eine andere als in deren Oberfläche. der wenn die freie Öberflächenenergie n\F einer chemisch ei1. Denn liehen Flüssigkeit dem Minimum zustrebt, so kann sie dies-'n"e^~ ihre auf eine ganz bestimmte Lagerung der Moleküle jn;es. da Oberfläche gegründete Oberflächenspannung ai bei gege*1 der Temperatur konstant ist, nur dadurch erreichen, daß die ebener fläche F ein Minimum wird; bei einer Lösung ist aber die flächenspannung selbst mit der Konzentration des ge 9 er" Stoffes in der Oberfläche veränderlich, und so besteht b<^'.os*e_n sungen immer die Möglichkeit, durch Änderung der Копг'е* Lö.
WIEDERHOLUNGSÜBUNGEN
Gute Homogenität des Magneten erreicht wird. 2. Zur direkten Bestimmung der Anreicherung eignet sich das schon oben genannte Verfahren, bei dem durch die Lösung aufsteigende oder fallende Tropfen des anderen in dieser nichtlöslichen Grenzflächenpartners gesammelt und die von diesen mitgenommene I Menge des gelösten Stoffes bestimmt wird. 3. Die vor und nach I dem Aufschließen des beim Lösen hinterbleibenden Rückstandes I gewonnenen Lösungen werden in einem Erlenmeyerkolben von 1,5 bis 2 Liter Inhalt vereinigt, auf 3U bis 1 Liter verdünnt und durch allmählichen Zusatz von Natriumkarbonatlösung so weit neutralisiert, wie es angeht, ohne daß ein bei längerem Umschütteln bleibender Niederschlag entsteht. 4. Dämpfe können 1 ohne Tropfenbildung über Taupunkt hinaus abgekühlt, Flüssigkeiten ohne Blasenbildung über den Siedepunkt hinaus erhitzt werden. 5. Alle Volumina müssen genau bekannt sein, durch Verschiebungen im Manometer eintretende Volumänderungen in Rechnung gesetzt werden. 6. Notfalls muß man dann etwas kühlen, hat dabei aber darauf zu achten, daß die Reaktion nicht zum Stillstand kommt. 7. Die Moleküle auf der flüssigen Oberfläche müssen zwar auch Potentialmulden überwinden, doch sind diese infolge der stärkeren thermischen Schwankungen in der Flüssigkeit von dauernd veränderlicher Tiefe und unregelmäßiger verteilt als auf dem Festkörper.
Übersetzen Sie; berücksichtigen Sie die Rektion des Verbs.
1. Zur Identifizierung dieser stellungsisomeren Porphyrine
hat die Aufnahme der Absorptionsspektren wesentlich beigetragen. 2. Von der Reinheit der Titersubstanz hat man sich vor dem Gebrauch zu überzeugen. 3. Auf eine Ausschaltung der Fehlerquelle, die einen größeren apparativen Aufwand erfordert hätte, wurde im Rahmen dieser Arbeit verzichtet.
Übersetzen Sie; unterscheiden Sie Adjektive und Adverbien.
1. Es gelingt so, die relative Anzahl unterschiedlich gebundener Protonen mit guter Genauigkeit zu bestimmen. 2. Hier überlagert sich dem Unterschied der Oberflächenspannung der je nach Größe der Dielektrizitätskonstanten verschieden starke Dissoziationsgrad in Ionen und damit ein verschieden starker Einfluß dissoziierter und undissoziierter Moleküle auf die Oberfläche. 3. Im folgenden sollen Längenänderungen an Glasproben bei verschieden schnellen negativen und positiven Änderungen der Temperatur betrachtet werden. 4. Eine allgemeiner anwendbare Apparatur wird von einer anderen Firma angeboten.
Übersetzen Sie; beachten Sie die erweiterten Attribute. ^A) Es erscheint angebracht, einige Bemerkungen über die nach der geschilderten Theorie aüfretenden Temperaturen zu machen. 2. Die kurzkettigste der verzeichneten Säuren behält den gasanalogen Zustand bis zu den größten Drucken beiVls. Auf eine weitere für das Verständnis der organischen Molekülverbindungen
nichtige Tatsache muß noch hingewiesen werden. AJ Leitet man Itetylcn durch ein 650 °C heißes, mit Holzkohlestuckchen gefüll- |рн stählernes Rohr, so läßt sich in den teerig^erdichteten Reak- lloHprurlukten tatsächlich Benzol nachweisen.(5^ Bei Zimmertemperatur feste Substanzen müssen im gelösten Zustand untersucht Werden.Im Stoß sich treffende Flüssigkeitsblasen vereinigen •Ich im allgemeinen nicht, sondern gehen nach erfolgter Begeg- Mutig wie elastische Kugeln auseinander. 7. Im Destillierrohr kondensierendes Acetamid wird vorsichtig hcrausgeschmolzen. Й, Beim Abkühlen fest werdende Chlorierungsprodukte können direkt durch Absaugen und Umkristallisieren gereinigt werden, fc Normann beschreibt den Apparat als ein weites, mit den Katalysator tragenden Bimssteinstücken gefülltes Rohr, durch welches die Dämpfe der zu hydrierenden Substanz mit Wasserstoff mischt geleitet werden./"9, Die oben erwähnte, durch zu hohe _pnnnung hervorgerufeneSjasentwicklung an der Anode würde Ntich bei zu hoher Temperatur auftreten, ^fö) Die in der durch die Kohlenstoffatome ausgezeichneten Eberfe liegenden äquatorialen Wasserstoffatome unterscheiden sich von den axialen Wasserstoffatomen, deren С—H-Bindungen im wesentlichen senk- irdit zu der genannten Ebene stehen.
Übersetzen Sie; achten Sie darauf, daß ein Substantiv ausgelassen ist.
I. Es bleibt nun die Frage, was den flüssig-ausgedehnten Vom flüssig-kondensierten Zustand unterscheidet. 2. Es ist zu beachten, daß die pn-Zahlen in der Grenzfläche sehr wohl andere lein können als die in der Masse des Wassers gemessenen. 3 Durch geeignete Wahl der beiden möglichen Winkellagen der Protonenverbindungslinien im Gitter, die durch die Röntgen- Itruktur bereits nahegelegt war, konnte eine ausgezeichnete Übereinstimmung der gemessenen Spektren mit den nach der Gleichung berechneten erzielt werden.
Übersetzen Sie; beachten Sie die Partizipialgruppen.
Es existiert eine Mischungslücke, beginnend mit einem Silbergehalt von 8,0% bis hinüber zu einem solchen von.91,2% (Mischungslücke — разрыв растворимости). v1!.' Das Perioden-
[csetz wurde, wenn auch noch nicht aus dem Atombau abgeteilt, bereits 1869 von Mendelejew erkannt und als gesetzmäßige Grundlage für die .Svßtematisierung der damals bekannten Elemente angewendet. ) Wir müssen uns, damit die Betrachtung der Überformung von Flüssigkeitsoberflächen im Schwerefeld ibschließend, mit dem Hinweis auf das Phänomen begnügen. Aj Bei einfachen Molekeln, die Doppelbindungen enthalten, kann TnaIi eine Bindungsänderung, verbunden mit einer chemischen Reaktion, schon bei mäßigen Drücken beobachten. Von einem Metallkamm werden feste Inseln in ihrer Bewegung aufgehalten, während flüssige, sich spaltend und nachher wieder zusammenschließend, durch den Kamm hindurchgehen. 6. Die magnetische Kernresonanzmethode stellt eine Spektroskopie bei — verglichen mit der optischen Spektroskopie — sehr langen Wellen dar. 7. Alle Untersuchungen über Keimbildung und Keimbildungsgeschwindigkeit werden dadurch außerordentlich erschwert, daß Verunreinigungen durch heterogene, oft mikroskopisch nicht mehr wahrnehmbare Körperchen, als latente Keimstellen wirkend, die Keimbildungsgeschwindigkeit erheblich erhöhen können.
h) Übersetzen Sie.
1. So müssen wir, soll unsere Betrachtung das Phänomen der Reibung in seinen wesentlichen Zügen erfassen, noch, wenn auch oft nur andeutend, auf die Frage des Materialverschleißes und seiner Beeinflussung durch grenzflächenaktive Stoffe eingehen. 2. Da aber, wie unten gezeigt wird, für Moleküle о die Differenz vergleichbarer Effekte ist, die nur einigermaßen theoretisch beherrscht werden, soll auf eine quantitative Darstellung verzichtet werden, und es sollen nur qualitativ die für die Praxis brauchbaren Gesichtspunkte diskutiert werden. 3. Die Frage, ob der Oberflächenschicht eine besondere von der makroskopisch bestimmten Viskosität im Inneren der Flüssigkeit verschiedene Viskosität eigen sei, wurde zunächst von Plateau 1 auf Grund von Beobachtungen über die Dämpfung einer in der Oberfläche schwingenden Magnetnadel dahingehend beantwortet, daß allgemein, also etwa bei reinem Wasser, in der äußersten Oberflächenschicht eine erhöhte Viskosität bestehe. 4. Vollständigkeit wurde auch bezüglich der Literaturzitate nicht angestrebt. Hierauf konnte um so leichter verzichtet werden, als in chemischen Zeitschriften der letzten Jahre eine ziemlich vollständige Literaturzusammenstellung geboten wird. 5. Sieht man von diesen Schwiergkeiten ab, so kann man davon ausgehen, daß für die endgültige Einordnung eines zu absorbierenden Moleküls eine Aktivierungsenergie nötig ist, die aus der Temperaturabhängigkeit der Adsorptionsgeschwindigkeit zu ermitteln wäre. 6. So wird bei Verwendung des niedrig schmelzenden Galliums dessen Schmelztemperatur von 30° gerade erreicht; bei der Kombination von Konstantan und Stahl steigt die Temperatur, ohne den Schmelzpunkt eines der beiden Metalle zu erreichen, auf über 1000 °C. 7. Die Molekulargewichte der Gase und Dämpfe ergeDen sich aus ihren Litergewichten, die der gelösten Stoffe aus den durch sie hervorgerufenen Gefrierpunktserniedrigungen. 8. Eine weitere Möglichkeit zur Messung schneller Reaktionen ist der paramagnetischen Pulsmethode eng verwandt. 9. Die Alkylmag- nesiumverbindungen werden bevorzugt dann zu Synthesen verwandt, wenn es auf einheitliche Produkte ankommt. 10. Noch aktiver als Fettsäuren sind an der Grenzfläche Wasser-Öl die Seifen, vor allem wohl deshalb, weil diese in Öl schlecht, jene 4ngegen gut löslich sind. 11. Das Absorptionsspektrum der wäs- wigen Promethiumsalzlösungen ist dem der Neodymsalzlösungen sehr ähnlich, nur daß bei jenem die einzelnen Banden ge Senkung des Flüssigkeitsspiegels an den Wänden des eintauchenden Körpers bedingten zusätzlichen hydrostatischen Effektes tritt. Iii. Es bleibt die Frage, warum aufeinander im Zustand der Haftreibung ruhende Körper, wenn die Haftkräfte vollwirksame Adhäsionskräfte von nicht geringerer Stärke als im Innern der Körper sind, doch noch relativ leicht auseinandergebrochen werden können, leichter auch, als man bei der Kenntnis der wahren Kontaktfläche erwarten würde. Der Grund dafür dürfte darin zu suchen sein, daß ein wirklich senkrecht zu den Flächen erfolgendes Abreißen kaum möglich ist; bestehen auch nur geringe Neigungen, so können die Kontaktbrücken einzeln hintereinander ;:breißen, so daß die aufzuwendende Kraft jeweils nur die zum Bruch kleinster Haftstellen erforderliche ist (Haftreibung — тре- mie сцепления). 17. Recht einfach ercheint es, Mikrokugeln bekannter Größe und Zahl adsorbieren zu lassen. Dieser Weg ist aber wohl nur bei Glas und eventuell gewissen Metallen gangbar, bei denen hinreichend kleine Kugeln glatter Oberfläche zu erhalten sind. In anderen Fällen kann er dadurch erzwungen werden, daß der als fester Grenzflächenpartner vorgesehene Stoff geschmolzen in Form von Tröpfchen vorzugebender Größe In den unterhalb der Schmelztemperatur gehaltenen Adsorptionsraum gebracht wird und, indem er diesen durchfällt, erstarrt.
Ubung 2. Übersetzen Sie; beachten Sie die Nebensätze.
1. Reibung verzehrt Energie, indem sie mechanische Arbeit xorzüglich in Wärme verwandelt. 2. Untersucht man, indem man die drahtförmige Luftelektrode in beiden Horizontalrichtungen iber den Film führt, die Potentiale, so erhält man in Übergangs- pebieten von Stelle zu Stelle wechselnde Werte. 3. Eine chemische
Kompensation ist möglich, indem man der Reagenzlösung eine Komponente in geeigneter Menge zusetzt, die mit der Analysen- lösung eine Reaktion mit entgegengesetzter Wärmetönung liefert, so daß sich beide Effekte aufheben. 4. Welches auch die Zahi der Phasen, der Komponenten und der chemischen Reaktionen sei, die Gleichgewichtszustände eines geschlossenen Systerr.5. dessen Ausgangsmassen gegeben sind, sind vollständig bestimmt durch zwei unabhängige Variable. 5. Wo immer zwei Phasen aufeinandertreffen, ein äußeres elektrisches Feld übt a'_T die einander berührenden Körper eine ponderomotorische Kra:t aus, welche sie gegeneinander in Bewegung zu setzen stre5::. 6. So alltäglich das Auftreten von Tropfen etwa im Tau oder irr. Regen ist, so blieb doch die Problematik der Tropfengesta'.t offenbar lange unbeachtet. 7. Anorganische Salze verhalten sich in Wasser als Lösungsmittel, wenn der Grenzflächenpartner eine sie nicht lösende Flüssigkeit ist, insofern ähnlich wie in Wasser gegen Luft, als die Grenzflächenspannung sich nur schwach und angenähert linear mit der Konzentration ändert. 8. Es kann hier auf die rein physikalischen Untersuchungen nicht näher eingegangen werden; über dieselben schlage man ein Lehrbuch der Physik nach. Erwähnt sei nur, daß es hauptsächlich das Studium der Kathodenstrahlen in Verbindung mit den weiter unten mitgeteilten Untersuchungen über radioaktive Elemente war, das- zu dieser Hypothese geführt hat.
Übung 3. Ubersetzen Sie; beachten Sie das Passiv.
1. So kommt schon in der Systematik zum Ausdruck, daß der lebende Organismus von der Kunst des Chemikers an Mannigfaltigkeit der Verbindungen übertroffen wird. 2. In Gasen kar.n wegen der geringen Konzentration aus Intensitätsgründen nur bei erhöhtem Druck gemessen werden. 3. Strukturfragen der organischen und anorganischen Chemie können aus den Kernresonanzspektren beantwortet werden. 4. Aus praktischen Gründen wird fast immer bei konstanter Frequenz mit variablen? Magnetfeld gearbeitet.
Übung 4. Übersetzen Sie; beachten Sie die Formen des Konjunktivs bzw. des Konditionalis.
1. Als wesentliches Kriterium für die "Festigkeit" der Elektronen in organischen Molekülen sei die elektrische Leitfähigkeit betrachtet. 2. Die Thixotropie des verbleibenden Gemenges ist die gleiche, als ob dieses unmittelbar in der vorliegenden Zusammensetzung bereitet worden wäre. 3. Als Beispiel für eine Abhängigkeit von der Molekülgröße seien Beobachtungen an einem stark entwässerten Kalknatriumaluminiumsilicat genannt. 4. Die mit Sicherheit von Äthan zum Heptan und Benzol zunehmen le Stärke der zwischenmolekularen Kräfte ließe eine in der angegebenen Reihenfolge zunehmende Adsorption erwarten. 5. Als Bei- fpici für Adsorptionskonkurrenz diene das Verhalten von Gemi- » hen von Benzol mit anderen Flüssigkeiten an festen Grenzflächen. 6. Ein anderslautendes Ergebnis von Laplace, nach dem bei Verschiedenheit des Randwinkels auf beiden Seiten der F.atte Anziehung oder Abstoßung stattfände, haben bereits Young 1 und Poisson2 widerlegt, so u. a. mit dem Hinweis darauf, daß, falls bei gleich hohen Niveaubereichen endlicher Breite in beiden Kammern in der ja als allein möglich vorausgesetzten horizontalen Richtung Bewegung einträte, Beschleuningung in < uer Richtung bestünde, in der keine Kraft wirke. 7. Wollte man d.e Erscheinungen, welche mit der Ausbildung und mit Ände- iungen von Potentialdifferenzen an Grenzflächen verbunden find, mit in eine Betrachtung der physikalischen und chemischen Erscheinungen an Grenzflächen einbeziehen, so müßte diese fast das Gesamt der elektrischen und elektro-chemischen Erscheinungen mit umfassen. 8. Ausgang einer Betrachtung der Adsorption an festen Körpern könnte grundsätzlich ebenso wie bei Flüssigkeiten die Gibbssche Adsorptionsgleichung sein. 9. Auch bei starker Oberflächenaktivität bleiben die absoluten Mengen adsorbierten Stoffes so außerordentlich klein, daß zu ihrem quantitativen Nachweis, sei es im Schaum oder über die Bestimmung der durch die Adsorption bedingten Konzentrationsverminderungen im Innern der Lösung, die Erzeugung sehr großer Flüssigkeitsoberflächen notwendig wäre. 10. Die Anzahl der vorgeschlagenen Methoden ist so groß, daß eine erschöpfende Behandlung aller in der Literatur behandelten Verfahren weit über den Rahmen dieser Arbeit hinausgehen würde. Außerdem sind viele dieser Methoden so wenig exakt, man denke z. B. an die früher gebräuchliche Trennung des Nickels und Kobalts von den übrigen Elementen der Gruppe durch Behandeln der Sulfide mit verdünnter Salzsäure, daß ein näheres Eingehen auf diese überflüssig erscheint. 11. Im Sinne der Gleichungen entspräche jedem Maximum der Grenzflächenspannung die gleiche Zusammensetzung der Oberfläche wie im Innern der Lösung bei ganz verschiedenen Werten der Oberflächenenergie. 12. Auf das Auftreten von Mischfilmen im lebenden Organismus und ihre hohe Bedeutung für diesen sei hingewiesen. 13. Die einfachste molekulardisperse Durchmischung zweier Stoffe im Filmzustand läge dann vor, wenn zwei unpolare Stoffe, die untereinander nur Dispersionskräfte betätigen, im Mischfilm beobachtet würden. Das wäre auf Quecksilberunterlage sehr wohl möglich. 14. Die Einzelheiten zeige man am Beispiel der Filme von Myristinsäure auf schwach salzsaurer wäßriger Lösung zwischen den Grenztemperaturen von 2° und 34 °C. 15. Nun ist es keineswegs so, als bestünden zwischen den lyophoben Molekülresten und der unterliegenden Flüssigkeit überhaupt keine Anziehungskräfte.
! 1 Lies: [']лт;]-Янг
