
- •Часть II
- •Содержание.
- •Лабораторный практикум:
- •Формулы для приближенных вычислений
- •Тригонометрические формулы
- •Определение абсолютной и относительной влажности воздуха
- •§1. Основные представления о водяном паре и влажности воздуха
- •§2. Диаграмма состояний в системе жидкость-пар и зависимость давления, насыщенного пара от температуры
- •§3. Определение влажности воздуха конденсационным гигрометром Ламбрехта (по точке росы)
- •§4. Измерение относительной влажности с помощью психрометров
- •Как пользоваться психрометрическим графиком (номограммой).
- •Контрольные вопросы и задания.
- •§1. Качественный анализ особого состояния поверхностного слоя
- •§ 2. Динамический анализ особого состояния поверхностного слоя
- •§ 3. Энергетический анализ особого состояния поверхностного слоя
- •§ 4. Связь между динамическим и энергетическим коэффициентами поверхностного натяжения
- •§ 5. Давление Лапласа
- •II. Экспериментальное определение коэффициента поверхностного натяжения жидкостей
- •По высоте подъема в капиллярных трубках.
- •2 . По методу отрыва капель
- •3. По методу выдувания пузыря из мыльной пленки
- •Порядок выполнения.
- •4. По методу отрыва рамки.
- •Контрольные вопросы:
- •Литература:
- •Зависимость температуры кипения жидкости от давления
- •§1. Пузырьковое кипение.
- •§2. Дифференциальная и интегральная зависимость температуры кипения от внешнего давления (или: давления насыщенного пара от температуры).
- •§3. Диаграмма состояний однокомпонентной системы.
- •§4. Экспериментальное изучение зависимости Ткип(р).
- •Порядок выполнения работы.
- •Расчеты и выводы: Контрольные вопросы:
- •Литература:
- •Зависимость вязкости жидкостей от температуры.
- •Теоретическое введение.
- •§1.Объяснение некоторых свойств систем с учетом особенностей взаимодействия двух молекул.
- •§ 2. Согласованное поле периодической структуры.
- •§3. Использование представлений о согласованном потенциальном поле для объяснения некоторых физических свойств конденсированных сред.
- •§4. Дефекты в кристаллах и температурная зависимость вязкости в жидкостях.
- •Эксперимент и обработка его результатов.
- •Расчеты и выводы: Контрольные вопросы:
- •Литература:
§4. Экспериментальное изучение зависимости Ткип(р).
Приборы и материалы.
1. Установка, состоящая из колбы с водой, холодильника (конденсора), термометра и электроплитки.
2. Манометр.
3. Барометр.
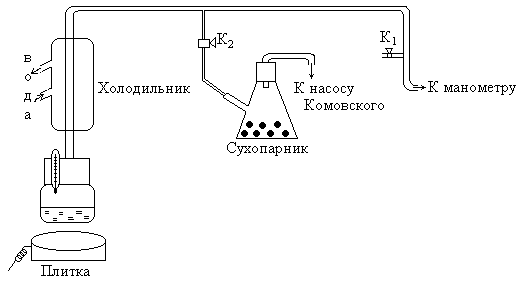
Рис. 5.
Приступая к выполнению работы, следует уяснить себе назначение каждой части установки, схема которой представлена на рис. 5., разобраться в соединительных трубках.
Порядок выполнения работы.
1. Отрегулируйте струю воды, поступающей в холодильник.
2. Откройте кран К1, соединяющий систему с атмосферой, включите электрическую плитку. Определите температуру кипения воды tкоС при атмосферном давлении.
3. Закройте кран К1, откройте кран К2, присоедините насос к трубке, произведите с его помощью разрежение, определите температуру кипения воды.
Постепенно уменьшая давление в системе, произведите не менее 12 измерений (качаний насосом делайте столько, чтоб температура кипения изменялась на (23)0 С).
4. После того как разрежение будет произведено до максимума, который определяет доступность для измерения температуры, произведите опыт в обратном порядке. С помощью крана в систему осторожно впускайте небольшие порции воздуха, постепенно увеличивая давление до атмосферного и определяя при этом соответствующие температуры кипения.
5. Давление определяется по графику цифровых показаний манометра.
Результаты измерений занести в таблицу:
Атмосферное давление po (измеряется по барометру): po= 133·N Па
где N – давление по барометру в мм. рт. ст.
№ п/п |
Показания манометра деления |
Р·104 Па |
ln P |
tк, С |
Tк, К |
1/Тк |
1. |
|
|
|
|
|
|
2. |
|
|
|
|
|
|
……… |
|
|
|
|
|
|
12. |
|
|
|
|
|
|
6. Оценив погрешности измерений p и t, постройте график зависимости p(tк) или tк(p), выбрав масштаб так, чтоб график занимал все поле рисунка (чертежа).
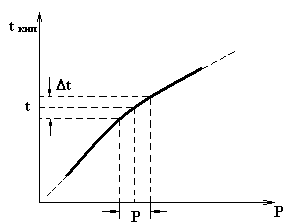
7. По графику в координатах ln p от 1/Тк оцените соответствие полученных результатов зависимости (9).
8. Воспользовавшись экспериментальной зависимостью tкип(T) и уравнением (5) в приближении, что насыщенный пар при температурах далеких от критической можно считать идеальным газом и что н.п.>>ж (н.п.>>ж), найдите удельную теплоту этого фазового перехода для 3-5 точек.
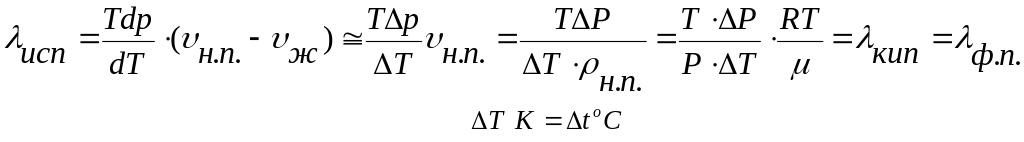
= 18,0·10-3 кг/моль
![]()
В СИ:
Расчеты и выводы: Контрольные вопросы:
1. Назовите виды кипения и условия, при которых они реализуются.
2. Чем кипение отличается от простого испарения? Расскажите о процессах, происходящих при пузырьковом кипении.
3. Изобразите примерный вид диаграммы состояний для однокомпонентной системы и объясните физический смысл линий на ней. О тройной и критической точках.
4. Что произойдет с жидкостью (например, водой), выброшенной из космического корабля в плохо герметичном сосуде?
5. Что такое удельная теплота фазового перехода? Первое начало термодинамики и молекулярно-кинетические представления к анализу плавления и испарения. В чем сходство и отличие этих фазовых переходов?
6. Получите уравнение Клапейрона-Клаузиуса для фазовых переходов. Как с его помощью оценить удельную теплоту фазового перехода? Дома эту процедуру постарайтесь выполнить, пользуясь таблицей Рн.п.(Т).
