
- •Часть I
- •Содержание.
- •Лабораторный практикум:
- •Измерения, их погрешности и обработка результатов измерений.
- •Обработка результатов прямых измерений.
- •II. Значащие и запасные цифры в числах и вычислительные операции с этими числами.
- •III. Обработка и представление результатов косвенных измерений.
- •Некоторые числа и физические константы, используемые при расчетах:
- •Формулы для приближенных вычислений
- •Некоторые математические формулы и соотношения:
- •Тригонометрические формулы
- •Формулы дифференциального и интегрального исчислений
- •Определение удельной теплоты плавления льда калориметрическим методом
- •§1. Характеристики процессов теплообмена.
- •§2. Энергетика фазовых переходов при плавлении и кристаллизации.
- •§3. Экспериментальные закономерности для процессов плавления.
- •§4. Общие принципы калориметрических измерений.
- •§5. Определение удельной теплоты плавления льда при атмосферном давлении (определяется по барометру и пересчитывается в Па с учетом 3х значащих цифр).
- •Расчеты.
- •Контрольные вопросы:
- •Литература:
- •Теоретическая часть:
- •§1. Основные понятия.
- •§2. Законы изопроцессов и уравнение Клапейрона (уравнение для любых реальных идеальных газов).
- •§3. Уравнение состояния однокомпонентного идеального газа – уравнение Клапейрона-Менделеева.
- •§4. Физический смысл универсальной газовой постоянной.
- •§5. Давление. Разность давлений. Измерение давления и разности давлений.
- •I. Экспериментальное определение r методом откачивание воздуха из сосуда определенного объема.
- •II. Определение r методом впрыскивания в сосуд с воздухом легко испаряющейся жидкости.
- •Результаты эксперимента и обработки данных представлены в таблице №2.
- •Контрольные вопросы:
- •Теоретическое введение
- •§1. Внутренняя энергия идеального газа
- •§3. О воздухе.
- •§4. Адиабатный и политропический процессы.
- •§4А. Постройте графики изопроцессов, включая адиабатный, в различных координатах:
- •§4Б. Политропические процессы при различных “n” и их графическое представление.
- •§6. Экспериментальное определение для воздуха.
- •1. Описание метода Клемана и Дезорма (приближение Клемана-Дезорма).
- •2. Измерения и обработка результатов.
- •Контрольные вопросы:
- •Литература:
- •Определение коэффициента внутреннего трения воздуха.
- •Явления переноса
- •§ 1. Феноменологическое описание явлений переноса
- •§2. Модель явления внутреннего трения в идеальном газе.
- •Экспериментальное определение коэффициента внутреннего трения η в газовых средах (в воздухе)
- •§3. Вывод рабочей формулы (формулы Пуазейля) для определения коэффициента вязкости .
- •§4. Методы экспериментального определения и обработка результатов измерений.
- •4.1. По методу натекания воздуха из атмосферы через капилляр в разряженную среду.
- •4.2. По выталкиванию воздуха через капилляр в атмосферу.
- •Измерения и обработка данных для первого и второго предлагаемых методов.
- •4.3. По натеканию воздуха через капилляр в разреженную среду.
- •§5. Расчёт средней длины свободного пробега ( ) и эффективного диаметра молекулы воздуха
- •Контрольные вопросы:
§5. Определение удельной теплоты плавления льда при атмосферном давлении (определяется по барометру и пересчитывается в Па с учетом 3х значащих цифр).
Пусть в калориметре массы mк находится вода массы mв при tо и лед массы mл при tпл.(tпл при p = 760 мм. рт. ст. равна 0 °C). Тогда в системе (вода, внутренний сосуд калориметра, лед, термометр) происходит тепловой процесс, в результате которого лед плавится и устанавливается для всех тел системы общая температура tк.
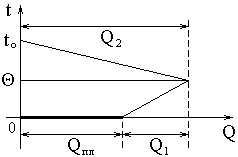
Qпл + Q1 = Q2 (10)
Qпл – теплота плавления льда;
Q1 – количество теплоты, пошедшей на нагревание воды, полученной из льда;
Рис.
4.
mл + cвmл( – 0º) = свmв(to - ) + скmк(to - ) + w(to - ) (11)
Откуда
 (12)
(12)
Таким образом, для определения данным методом необходимо знать:
mл – массу льда (расплавившегося),
mв – массу воды в калориметре (первоначально),
mк – массу калориметра (внутреннего сосуда) с мешалкой,
tо – начальная температура воды, калориметра и термометра (к моменту загрузки льда),
– установившаяся температура,
cв, ск, – удельные теплоемкости воды и калориметра (алюминиевого) -табличные значения,
w – теплоемкость термометра (его водяной эквивалент). В данной работе этой величиной можно пренебречь, т.е. w 0.
Замечание 1.
Предположение о том, что W 0 легко проверяется. Достаточно до проведения экспериментов со льдом в калориметр опустить такой же второй термометр, имеющий заметно меньшую температуру, и если показания основного термометра не изменяются, то, действительно, в нашем опыте теплоемкость его можно считать равной нулю.
К определению величин, входящих в (12) и сводится практическая задача по определению удельной теплоты плавления льда данным методом.
Замечание 2.
! Это замечание важно с двух точек зрения:
Сколько налить в калориметр воды и сколько добавить туда льда?
Важно знать, что удельная теплота плавления льда численно почти в 80 раз превышает удельную теплоемкость остывающей воды (числа сравниваются в одной системе единиц). А это значит, что для того, чтоб расплавить 1 г льда, вода массой 1 г должна остыть почти на 80оС (точнее 79оС). Теперь ясно, что воды следует взять чуть больше, чем половину внутреннего сосуда калориметра при температуре близкой к (5060)оС (если позволяет термометр). Лед надо добавлять сухой (без влаги). Желательно, чтоб конечная температура воды в калориметре стала примерно на 10оС ниже комнатной, - это уменьшит фактор теплообмена.
2) О сухом льде! Если лед будет содержать жидкость, то результат эксперимента будет существенно занижен. Промокайте-просушивайте лед хорошо! Не доводите его до фазы активного плавления. Пусть его температура будет даже на (0,20,3)%. Самостоятельно сделайте эту оценку.
Приборы и материалы:
1. Калориметр. 2. Вода. 3. Термометр. 4. Лед.
|
5. Фильтровальная бумага. 6. Весы. 7. Электрическая плитка или кипятильник с нагреваемой водой.
|
Замечания:
1. Обратите внимание:
а) при взвешивании пустой калориметр должен быть сухим;
б) при опускании льда в воду лед должен быть сухим (просушите фильтровальной бумагой и сразу же опустите). Количество льда, которое необходимо опустить в калориметр, определяется с учетом ранее оговоренных условий, (это может быть несколько кусочков).
3. Масса расплавленного льда определяется как разность масс калориметра с водой после опыта и калориметра с водой до опыта.
4. Удельные теплоемкости воды, внутреннего сосуда калориметра и мешалки в данном опыте не определяются, (числовые данные приведены: проверьте, сравнив со справочными).
5. Во время опыта термометр из калориметра вынимать не рекомендуется, т.к. при этом можно вынести и капли жидкости, что ведет к занижению mл и завышению .
6. Окончательная (установившаяся) температура определяется как самое наименьшее показание термометра во время опыта (почему?) .
7. Первоначальное количество воды в калориметре должно быть, возможно, большим (почему?).
Таблица 1. cв= 4,18·103 ; ск= 0,896·103 .
mк, г |
(mк+ mв), г
|
mв, г |
(mк+mв+mл), г |
mл, г |
m (весов), г |
tо, °С |
, °С |
tо, , °С |
к = m/mк |
в
=
|
л
=
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
