
IV уровень.
Гипоталамус получает блок информации по вегетативной нервной системе.
Часто III и IV уровень не разрывают и говорят о гипоталамо-гипофизарной регуляции. Гипоталамус при помощи собственных гормонов управляет нижестоящими уровнями в эндокринной нервной системе.
V уровень.
Осуществляется путём изменения активности различных зон коры головного мозга. Эти зоны связаны ассоциативными связями с гипоталамусом и меняют активность клеток гипоталамуса.
Биологические эффекты любого гормона, который производится в организме человека, всегда опосредованы рецепторами, т.е. чтобы проявился биологический эффект нужно чтобы гормон соединился со своим специфическим рецептором. После образования гормон-рецепторного комплекса начинается реализация биологических эффектов данного гормона. Рецепторы разнообразны и делятся на 2 группы в зависимости от локализации в клетке:
На поверхности клетки. На поверхность выходит часть рецептора, которая предназначена для контакта с гормоном. Рецептор пронизывает всю толщу мембраны и его часть обращена в цитоплазму.
Внутриклеточные, располагающиеся в цитоплазме – предназначены для гормонов, которые проходят через мембрану клетки.
Взаимодействие рецептор-гормон осуществляется при помощи нековалентных сил взаимодействия (ион-ионные и т.д.). Часто взаимодействие обратимо. Гормон-рецепторный комплекс существует какой-то интервал времени. Пока пролонгировано существует этот комплекс идёт реализация биологического эффекта. Клетки организма как саморегулирующая система обладают способностью менять свою чувствительность на действие гормональных сигналов. Таких способов существует много. Вот некоторые из них:
Количественный механизм. Распространён широко. Клетки изменяют свою чувствительность по отношению к конкретному гормону, изменяя количество рецепторов, чувствительных к данному гормону. Такая регуляция бывает либо позитивной, либо негативной. Если ↑ количество рецептора, то ↑ чувствительность клетки. Если ↓ количество рецепторов, то ↓ чувствительность. Это медленный механизм регуляции.
Качественный механизм. Клетки не изменяют количество рецепторов, но изменяют их чувствительность. Они «включают» и «выключают» рецепторы. Такое явление видим, когда в зону, окружающую клетку, поступают гормоны-антагонисты по биологическому эффекту. Тот гормон, который первый соединяется с клеткой, изменяет чувствительность клетки таким образом, что клетка становится невосприимчивой к гормону-антагонисту клетки (т.е. «выключается» рецептор). Например, если на клетку подействовал адреналин, то действие инсулина невозможно (т.е. однонаправленный механизм).
Эффект «плато». Клетки ограничивают действие гормональных сигналов при помощи эффекта насыщения или эффекта доз (эффект «плато»). Клетка может продуцировать максимально строго определённое количест
во рецепторов, чувствительных к данному гормону.

Действие абсолютно любого гормона основано на связывании гормона с рецептором. Если в межклеточной жидкости непрерывно растёт количество гормона, то клетка вначале отвечает по нарастающей, а затем по максимуму, по одному и тому же уровню. Это потому, что количество рецепторов к одному и тому же виду клеток ограничено (лимитировано). Это нужно, чтобы клетка не погибла.
Общая реакция тканей-мишеней на действие гормона определяется прежде всего локальной концентрацией гормона вблизи тканей-мишеней, которая зависит от:
скорости синтеза и секреции гормона;
анатомической близости тканей-мишеней к источнику гормона;
константы ассоциации-диссоциации гормона со специфическим белком-переносчиком, если такой существует для данного конкретного гормона. Переносчики нужны для стероидов, не растворимых в воде;
скорости превращения неактивной или малоактивной формы гормона в активную;
скорости удаления гормона из крови либо в результате работы системы выведения (почки, печень) либо в результате распада или уничтожения гормона (гормон-рецепторный комплекс→в цитоплазму→выброс лизосомальных ферментов→распад гормонов).
Рецепторы, которые предназначены для действия гормонов-антагонистов, не изменяют свою чувствительность, но в цитоплазму клетки попадают соединения (ферменты), которые блокируют реализацию эффектов гормонов-антагонистов.
Гормоны осуществляют регуляцию внутриклеточных процессов следующими путями:
Путём активации синтеза вторичных мессенджеров (посредников).
Путём рецептор-зависимой активации ионных каналов плазматических мембран.
Путём изменения активности рецептора-фермента, т.к. некоторые рецепторы проявляют ферментные свойства. Такие рецепторы расположены на поверхности клеток, а активные центры обращены в сторону цитоплазмы, они предназначены для контакта с фактором роста клеток или, например, рецепторы, чувствительные к натрий-уретическому гормону предсердия. Ферментативную активность рецепторы проявляют, как правило, в момент образования гормон-рецепторного комплекса.
Гормоны влияют на внутриклеточные процессы путём переноса связанного с рецептором гормона в цитоплазму клетки, где он находится в неизменённом виде определённый интервал времени. Либо за счёт образования внутриклеточного гормон-рецепторного комплекса (типично для стероидов).
Если рассматривать механизмы работы гормонов, то в организме человека можно выделить 3 механизма воздействия гормона на клетку:
I мембранный (реализуется практически мгновенно, самый быстрый механизм).
II мембранно-внутриклеточный – быстрый, но реализуется через 5-10 минут.
III внутриклеточный (прямой, цитозольный) – типичен для гормонов стероидной природы, а также для гормонов, которые взаимодействуют с рецепторами на поверхности клетки, а далее гормон-рецепторный комплекс при погружении в цитоплазму там относительно длительно не разрушается. Это длительный механизм (несколько часов, суток).
Таблица 4. Основные этапы передачи гормональных сигналов.
Через мембранные рецепторы (пептидные гормоны, адреналин) |
Через внутриклеточные рецепторы (Стероидные гормоны, тироксин) |
Г ↓ Рецептор (в мембране)
G-белок аутофосфори-
рецептора ↓ Фермент каскад (аденилатциклаза, фосфорилирования Гуанилатциклаза, белков
Ф ↓ 2-й посредник активация (ц-АМФ, ц-ГМФ, ферментов и Са2+ИФ3, ДАГ, факторов NO) транскрипции ↓ ↓ Протеинкиназы ↓ изменение Фосфорилирование количества белков белков ↓ (ферментов)
И Функциональной активности
изменение скорости метаболизма |
Г ↓ Рецептор (внутри клетки) ↓ Комплекс гормон-рецептор ↓ Транспорт комплекса гормон-рецептор в ядро ↓ Взаимодействие с ДНК (энхансер, сайленсер) ↓ Индукция или репрессия синтеза белков ↓ Изменение количества белков (ферментов)
|
Практически реализация биологических эффектов идёт по одному механизму, ещё реже по двум, ещё реже по трём механизмам (инсулин).
Мембранный механизм типичен, главным образом, для гормонов белково-пептидной природы. Мембранный механизм в чистом виде существует редко, как правило, сочетается с мембранно-внутриклеточным. Рецепторы располагаются на поверхности клетки. В момент образования гормон-рецепторного комплекса рецептор начинает менять свою конформацию, изгибается в толще мембраны, изменяет форму мембраны. Он начинает выталкивать из мембраны в цитоплазму мембранные белки, которые до этого в цитоплазме не были. Эти белки очень часто ведут себя как ферменты, разрушающие вторичные мессенджеры, предназначенные для реализации биологических эффектов гормонов-антагонистов. В этот момент времени невозможно действие гормонов-антагонистов. В этот участок мембраны встраиваются цитоплазматические белки, выполняющие роль транспортных белков, при помощи которых внутрь клетки поступают различные соединения – глюкоза. GLUT-2 – это белок-транспортёр для глюкозы.
В момент образования гормон-рецепторного комплекса в зоне мембраны клетки активируются непосредственно прилегающие к рецептору различные транспортные системы и по такому механизму могут поступать свободные аминокислоты, глюкоза, Са2+, другие катионы.
Например, инсулин вызывает мгновенное гипогликемическое действие.
Или фермент фосфодиэстераза гидролизует ц-АМФ.
Мембранно-внутриклеточный механизм.
Очень широко распространён в организме человека. Мы регулируем обмен веществ при помощи изменения активности регуляторных ферментов. Этот механизм типичен для гормонов белково-пептидной природы, а также для гормонов, производных аминокислот.
Суть его сводится к следующему: в момент образования гормон-рецепторного комплекса внутри клетки начинает значительно увеличиваться количество молекул (вторичные мессенджеры, вторичные посредники) либо за счёт активации их синтеза, либо вследствии их поступления извне (Са2+). Это молекулы, которые могут запускать, как правило, каскад систем активации ферментов или изменять активность регуляторных ферментов. В конечном итоге мы наблюдаем изменение активности регуляторных ферментов, контролирующих строго определённую ветвь метаболизма.
Адреналин взаимодействует с рецептором, вследствие чего рецептор изгибается и часть рецептора, обращённая к цитоплазме, приближается G-белку (имеющего α, β, γ полипептидные цепи). G-белки могут быть позитивными (активируют ферменты) и негативными (тормозят ферменты). К α-цепи G-белка присоединяется молекула ГТФ (это возможно, когда существует гормон-рецепторный комплекс) и гидролизует его до ГДФ. Гидролиз только при приближении аденилатциклазы. При присоединении ГТФ к α-цепи происходит диссоциация трёх субъединиц G-белка (α, β, γ) и α-цепь G-белка присоединяется к ферменту аденилатциклазе, находящейся в неактивной форме. В ассоциированном виде этот фермент не работает. α-цепь выталкивает из аденилатциклазы

 ГДФ+Фн
ГДФ+Фн
ГТФ
Рисунок 2. Мембранно-внутриклеточный механизм (активация аденилатциклазы)
ингибирующую цепь, приводя к диссоциации самого фермента и активность аденилатциклазы увеличивается. ГТФ соединяется с α-цепью некоторый интервал времени, в тече ние которого аденилатциклаза активно работает . Затем идёт гидролиз ГТФ и G-белок вновь ассоциирует друг с другом и активность аденилатциклазы уменьшается. Но за это время внутри клетки образуется большое количество ц-3,5-АМФ. В этот момент времени наблюдаем усиление химического сигнала. 1 молекула гормона во временном интервале приводит к наработке сотни и тысячи молекул нуклеотидов (ц-3,5-АМФ, ц-3,5-ГМФ), следовательно, одновременно сотни и тысячи молекулы ферментов активируются, активируется протеинкиназная система, идёт модификация регуляторных ферментов (ковалентная модификация, например, гликоген).
Вторичные посредники существуют следующей разновидности:
- ц-3,5-АМФ и ц-ГМФ;
- кальциевая система;
- соединения белково-пептидной природы (белок IRS при действии на клетку инсулина).
Кроме того, в момент образования гормон-рецепторного комплекса внутриклеточно может быть активирована система кальция как вторичного посредника. Внутри клетки начинает расти концентрация Са2+. Причины увеличения его концентрации:
За счёт поступления Са2+ извне (рецептор-зависимая активация ионных каналов в момент образования гормон-рецепторного комплекса);
За счёт торможения выведения Са2+ из клетки;
За счёт выброса Са2+ из внутриклеточных депо (эндоплазматический ретикулум).
Очень часто в момент действия гормона на рецептор или образования гормон-рецепторного комплекса внутри клетки активируется фермент фосфолипаза С. Этот фермент начинает гидролизовать мембранные фосфолипиды, а конкретно инозитфосфатиды и в цитоплазму клетки начинают поступать ДАГи и инозитол-3-фосфат.
Поэтому часто считают, что система Са2+ как вторичного мессенджера включает 3 компонента:
относительно высокая концентрация Са2+;
ДАГи;
инозитол-3-фосфат.
Са2+ связывается с кальций-связывающим белком (кальмодулин), а комплекс кальций-кальмодулин обладает 2 действиями:
- непосредственно изменяет аткивность регуляторных ферментов;
- активирует каскад систем регуляции ключевых регуляторных ферментов.
ДАГи увеличивают сродство Са2+ к ферментам. Инозитол-3-фосфат повышает выброс Са2+ из внутриклеточных депо.
Цитозольный (прямой механизм) – типичен для стероидов, гормонов, которые легко проходят через клеточную мембрану или гормонов, гормон-рецепторные комплексы которых могут быть погружены через клеточные мембраны. Липофильные молекулы этой группы гормонов легко диффундируют сквозь плазматическую мембрану любых клеток, но только в клетках-мишенях они находят свой специфический рецептор, имеющий высокую степень сродства к гормону.
Гормон-рецепторные комплексы образуются в цитоплазме, рецепторы – внутри клетки. После образования гормон-рецепторного комплекса он движется в сторону ядра, затем довольно сложный механизм изменения активности генетического аппарата клетки. Как правило, активируется несколько генов, ответственных за синтез строго определённых регуляторных белков.
Известно, что активация образовавшегося гормон-рецепторного комплекса зависит от температуры и присутствия солей, при этом меняется величина, конформация и поверхностный заряд комплекса, и он приобретает способность связываться с хроматином. Гормон-рецепторный комплекс связывается со специфической областью ДНК и активирует либо инактивирует специфические гены. В результете избирательного воздействия на транскрипцию генов и синтез соответствующих мРНК происходит изменение содержания определённых белков, что сказывается на активности тех или иных процессов метаболизма. Далее начинается синтез белка и концентрация этого регуляторного фермента начинает плавно нарастать внутри клетки. Таким образом можно изменять активность метаболического пути (повышать синтез жирных кислот). Этот механизм реализуется медленно, через несколько часов, иногда – даже суток.
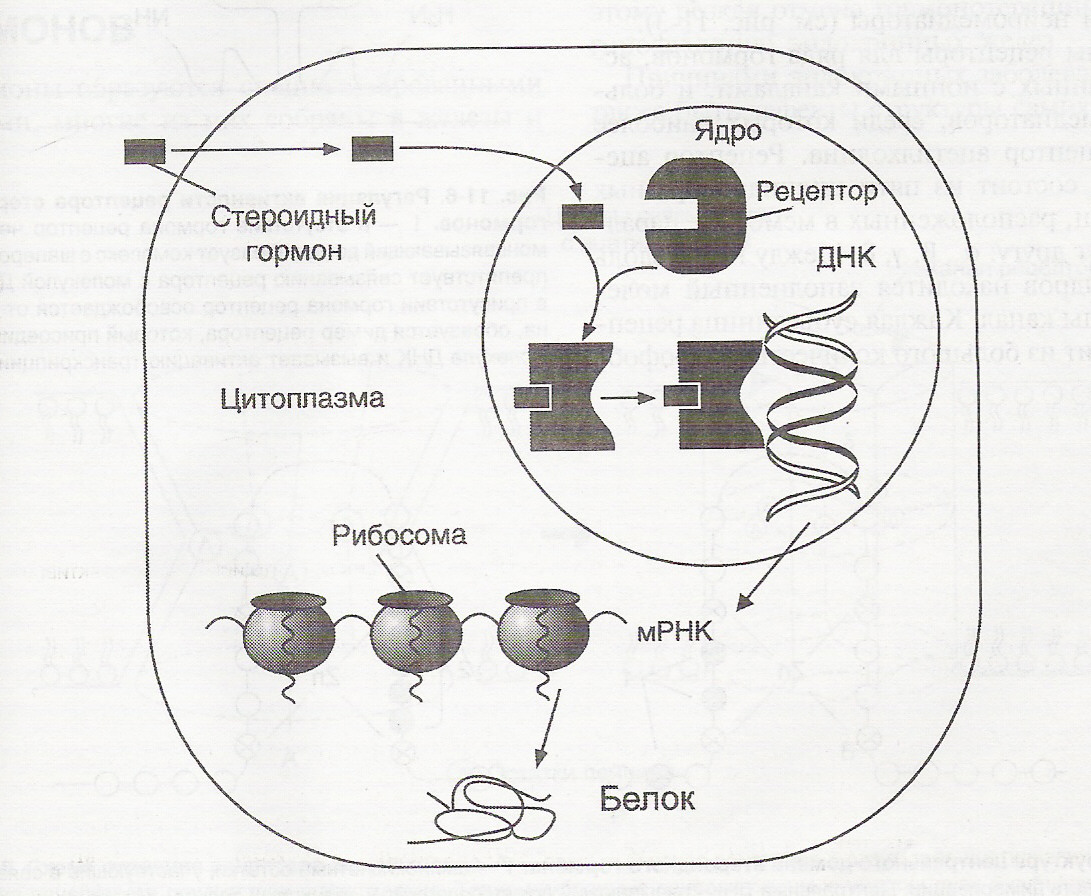
Рис. 3. Передача гормональных сигналов через внутриклеточные рецепторы (рецепторы стероидных гормонов могут находиться в цитоплазме и ядре).


 ормон
ормон
 лирование
лирование осфолипаза
С)
осфолипаза
С) зменение
зменение

 ормон
ормон