
- •Вопрос 1 Сырье для производства синтетического аммиака. Способы получения водорода и азота
- •Двухступенчатая организация конверсии природного газа.
- •Вопрос 2 Паровая конверсия природного газа: реакции и равновесие процесса.
- •Вопрос 3 Паровая конверсия природного газа: катализаторы.
- •Паровая конверсия природного газа: кинетика.
- •Параметры первой ступени конверсии природного газа.
- •Оборудование конверсии природного газа 1 ступени. Многорядная трубчатая печь.
- •Вопрос 4 Методика расчета материального баланса радиантной зоны трубчатой печи
- •Вопрос 5 Методика расчета теплового баланса радиантной зоны трубчатой печи
- •Вопрос 6 Двухступенчатая организация процесса конверсии природного газа.
- •Особенности второй ступени конверсии.
- •Реакции и равновесие процесса
- •Вопрос 7 Паровоздушная конверсия метана: кинетика, катализаторы и параметры процесса.
- •Вопрос 8 Оборудование стадии паровоздушной конверсии природного газа
- •9. 10. Двухступенчатая организация конверсии монооксида углерода. Конверсия монооксида углерода: реакции и равновесие процесса.
- •Методика расчета материального баланса процесса конверсии со.
- •Методика расчета теплового баланса конвертора со .
- •Очистка конвертированного газа от диоксида углерода. Требования, предъявляемые к хемосорбенту и массообменной аппаратуре.
- •Моноэтаноламиновая очистка: реакции, равновесие, кинетика и параметры процесса.
- •15. Оборудование стадии очистки конвертированного газа от диоксида углерода и регенерации раствора
- •Технологическая схема мэа-очистки.
- •Очистка конвертерного газа от со2 по методу «карсол».
- •18.Физико-химические свойства nн3.Требования к качеству nн3.Синтез nн3 :реакция,равновесие процесса
- •Требования к качеству продукционного nн3 по гост 6221 – 90.
- •19.Синтез аммиака: кинетика, механизм реакции, катализаторы и параметры процесса.
- •20. Оборудование стадии синтеза nн3.Технологические особенности производств
- •23.Производство нак. Сырье. Требования к качеству продукционной кислоты. Стадии производства.Балансовая реакция получения hno3 и расчет расходных коэффициентов. Стадия контактного окисления аммиака…
- •25.Гомогенное окисление монооксида азота: реакции, равновесие, кинетика и параметры процесса.
- •27. Переработка оксидов азота в азотную кислоту: реакции, равновесие, кинетика и параметры процесса.
- •28. Оборудование стадии абсорбции нитрозных газов.
- •30.Методика расчета материального баланса первой тарелки абсорбционной колонны в производстве азотной кислоты.
- •31. Методика расчета теплового баланса первой тарелки абсорбционной колонны в производстве азотной кислоты.
- •33. Сырье и требования к качеству продукционного карбамида. Физико-химические свойства карбамида. Синтез карбамида: реакции и равновесие процесса.
- •34. Синтез карбамида: кинетика и параметры процесса. Диаграмма состояния системы.
- •35. Оборудование стадии синтеза карбамида. Расходные коэффициенты на 1 т карбамида. Технологические особенности производства карбамида.
- •36. Технологические схемы получения карбамида.
- •Вопрсо№39: Методика расчета материального баланса аппарата итн
- •Способы получения элементарной серы. Добыча серы. Требования к качеству серы.
- •Сырье для производства h2so4. Серный колчедан и др. Сернистые соединения металлов, газы цветной металлургии, сульфаты Ca, k, Fe.
- •Газы цветной металлургии
- •Физико-химические основы процесса горения серы. Печи для сжигания жидкой серы. Утилизация теплоты горения серы.
- •Методика расчета материального баланса циклонной печи.
- •Методика расчета теплового баланса циклонной печи.
- •47. Равновесие и кинетика процесса окисления диоксида серы
- •48. Катализаторы для окисления диоксида серы. Контактные аппараты для окисления диоксида серы.
- •49. Методика расчета материального баланса контактного аппарата
- •50. Методика расчета теплового баланса контактного аппарата
- •51.Равновесие и кинетика процесса абсорбции триоксида серы.
- •Аппаратурное оформление стадии абсорбции. Моногидратный абсорбер. Олеумный абсорбер, сушильная башня.
- •53.Методика расчета материального баланса моногидратного абсорбера.
- •55. Технологическая схема печного отделения.
- •56. Технологическая схема контактно-компрессорного отделения.
- •57. Технологическая схема сушильно-абсорбционного отделения.
- •58.Способы производства и применение фосфорной кислоты. Сырье и требования к качеству продукционной фосфорной кислоты. Стадии технологического процесса.
- •Разложение апатитового концентрата смесью серной и фосфорной кислот
- •Фильтрация фосфополугидрата на вакуумных фильтрах, гидроудаление
- •Упаривание (концентрирование) фосфорной кислоты
- •Абсорбция газов
- •59.Химизм процесса взаимодействия фосфатов с кислотами. Кинетика процесса разложения фосфатов.
- •Скорость процесса разложения фосфатов (Кинетика)
- •60.Кристаллизация сульфата кальция и условия образования крупнокристаллического осадка.
- •61.Режимы экстракции фосфорной кислоты. Оборудование для экстракции фосфорной кислоты.
- •62.Выделение и улавливание фтора при получении и переработке эфк. Оборудование стадии.
- •63.Методика расчета материального баланса отделения экстракции в производстве дигидратной эфк.
- •64.Методика расчета теплового баланса отделения экстракции в производстве дигидратной эфк.
- •65. Производство сложных удобрений на основе эфк. Свойства фосфатов аммония. Физико-химические особенности производства аммофоса и фосфатов аммония.
- •Физико-химические особенности н а рисунке показаны изотермы растворимости в системе аммиак – фосфорная кислота – вода при 25 и 75 ºС. Взаимодействие эфк с nh3 происходит по реак-ям (1)-(3).
- •66 Вопрос. Основное оборудование стадий нейтрализации, гранулирования и сушки при получении фосфатов аммония: струйный реактор, саи, аг, сб, бгс.
- •68. Производство диаммонийфосфата, особенности технологии. Требования на даф
- •1. Привести расчет величин δн и δg для I ступени паровой конверсии природного газа.
- •8. Дать полную характеристику колонне синтеза, как реактору для получения карбамида. Материал колонны синтеза.
- •9. Основные стадии процесса окисления аммиака до оксида азота(2), как гетерогенно-каталитического хтп.
- •12 Дать полную характеристику абсорбционной колонне , как реактору получения нак. Материал абсорбционноц колонны.
- •13. Уравнение адиабаты. Зависимость степени превращения оксидов азота в азот для необратимой экзотерм. Реакции (графическая и аналитическая зависимости)
- •14. Дать полную характеристику аппарата типа “кипящий слой”, рассчитать критическую скорость псевдоожижения.
- •15. Интенсификация работы оборудования и пути ее увеличения.
- •17.Охт. Дать полную характеристику экстрактору, как реактру для получения эфк.
64.Методика расчета теплового баланса отделения экстракции в производстве дигидратной эфк.
Цель расчета: определение теплоты, вносимой поступающей в экстрактор циркулирующей пульпой.
Исходные данные.
1. Исходные данные, таблица материального баланса и расчеты.
2. Удельные теплоемкости веществ, кДж/(кг×К): апатитовый концентрат – 0,783 [3]; 93 %-ная серная кислота при 40 °С – 1,275 [6]; воздух при 20 °С – 1,004 [3]; фосфогипс – 1,072 [3].
3. Температуры потоков, °С: апатит – средняя температура в самом жарком месяце; 93 %-ная серная кислота – 40; оборотная фосфорная кислота (27,62 % Н3РО4) – 70; воздух на входе – 20; газы на выходе – 60; пульпа на фильтрацию и циркулирующая пульпа – 80.
4. Кратность циркуляции пульпы КЦ = 8.
5. Относительная влажность воздуха – 0,8.
6. Потери теплоты в окружающую среду – 2 % от прихода теплоты.
7. Теплотами испарения воды и HF в виде SiF4 пренебрегаем вследствие их малости.
8. Отношение Ж/Т в пульпе – 3:1.
9. Массовая доля твердой фазы в пульпе Т=25 %, жидкой Ж=75 %.
10. Гипсовое число Г = 1,6.
11. Расчёты выполнить в МДж
Расчет
1. Составить расчетную схему тепловых потоков экстрактора. На схеме указать все входящие и выходящие тепловые потоки, температуры потоков, искомые величины. Записать химическую реакцию, протекающую в экстракторе, с численным значением теплового эффекта.
2. Записать условие и уравнение теплового баланса. Уравнение теплового баланса имеет вид: Q1 + Q2 + Q3 + Q4 + Q5 + Q6 + Q7 = Q8 + Q9 + Q10 + Q11,
где Q1 – физическая теплота апатитового концентрата, подаваемого на экстракцию; Q2 – физическая теплота 93 % серной кислоты; Q3 – физическая теплота раствора разбавления (ОФК); Q4 – теплота, выделяемая при протекании экзотермической реакции разложения апатитового концентрата; Q5 – теплота, выделяющаяся при разбавлении 93 % серной кислоты в экстракторе; Q6 – физическая теплота циркулирующей пульпы; Q7 – физическая теплота воздуха, поступающего в экстрактор; Q8 – физическая теплота пульпы, идущей на фильтрацию; Q9 – физическая теплота газов, покидающих экстрактор; Q10 – физическая теплота циркулирующей пульпы, поступающей из экстрактора в вакуум-испаритель для охлаждения; Q11 – потери теплоты в окружающую среду.
3. Рассчитать физическую теплоту апатитового концентрата Q1, подаваемого на экстракцию. Принять среднюю температуру в районе г. Череповца в июле, т.е. в период наиболее напряженного теплового режима цеха, t = 17,6 °С
4. Рассчитать физическую теплоту Q2 93 % серной кислоты.
5. Рассчитать физическую теплоту Q3 раствора разбавления (ОФК).
Удельную теплоемкость раствора разбавления определить по формуле; кДж/(кг×К):
с = 4,2324 – 0,02969×х (14),
где х – концентрация Н3РО4, % мас.
6. Рассчитать теплоту Q4, выделяющуюся при протекании экзотермической реакции разложения апатитового концентрата по формуле:
Q4 = (mап/Mап)×Kизв×hап×q,
где mап – масса фторапатита; Мап – молярная масса фторапатита; Кизв –коэффициент извлечения; hап = 1 – содержание фторапатита в апатитовом концентрате; q – тепловой эффект реакции взаимодействия серной кислоты с апатитовым концентратом, определяемый по уравнению реакции
Ca5F(PO4)3 (тв) + 5H2SO4 (р) + 10H2O (ж) = 5CaSO4×2H2O (тв) + 3H3PO4 (р) + HF (г), DH<0.
7. Рассчитать теплоту Q5, выделяющуюся при разбавлении 93 % серной кислоты в экстракторе по формуле:
Q5 = GK×q/98,
где GK – часовое количество 100 % серной кислоты, поступающей в экстрактор; q – удельная теплота разбавления серной кислоты, кДж/кмоль:
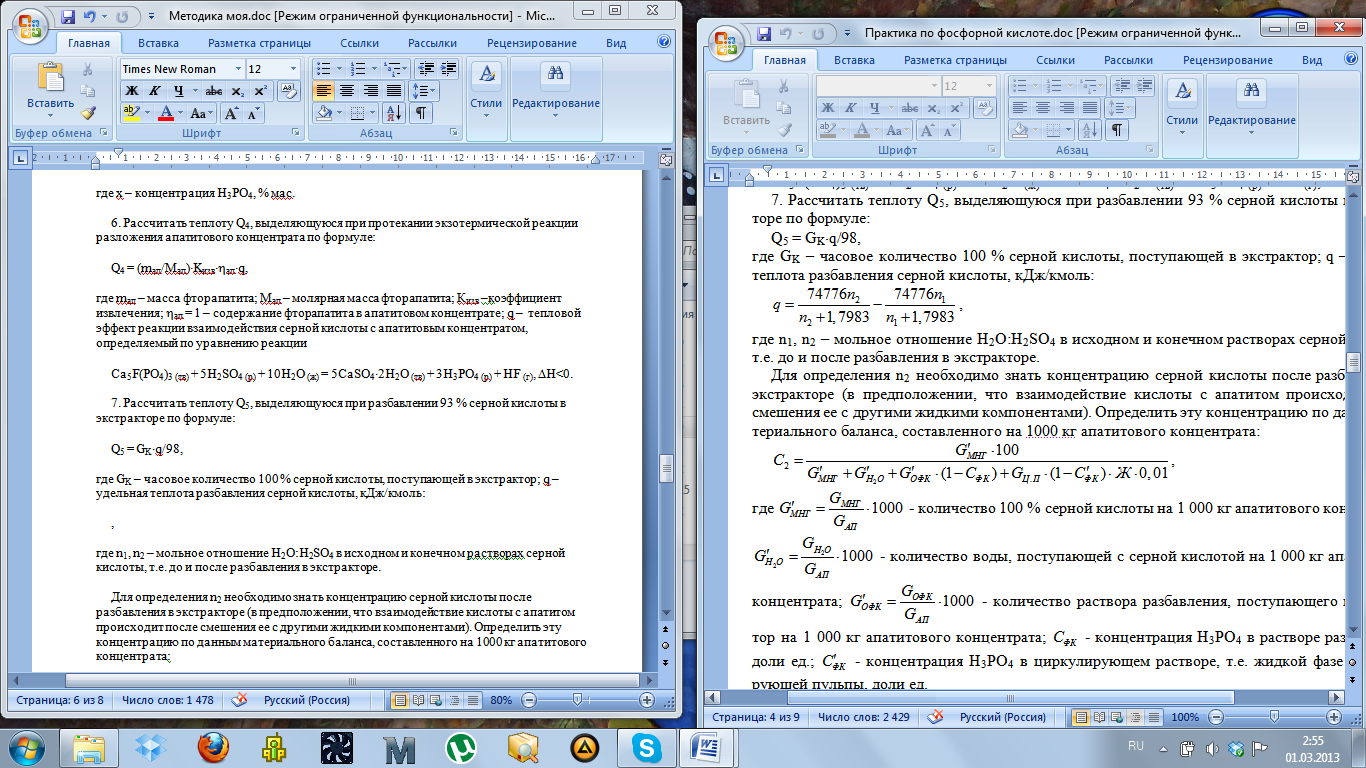
где n1, n2 – мольное отношение H2O:H2SO4 в исходном и конечном растворах серной кислоты, т.е. до и после разбавления в экстракторе.
Для определения n2 необходимо знать концентрацию серной кислоты после разбавления в экстракторе (в предположении, что взаимодействие кислоты с апатитом происходит после смешения ее с другими жидкими компонентами). Определить эту концентрацию по данным материального баланса, составленного на 1000 кг апатитового концентрата:
где - количество 100 % серной кислоты на 1 000 кг апатитового концентрата; - количество воды, поступающей с серной кислотой на 1 000 кг апатитового концентрата; - количество раствора разбавления, поступающего в экстрактор на 1 000 кг апатитового концентрата; СФК - концентрация H3PO4 в растворе разбавления, доли ед.; С’ФК - концентрация H3PO4 в циркулирующем растворе, т.е. жидкой фазе циркулирующей пульпы, доли ед.
Рассчитать количество пульпы на 1 000 кг фосфата, поступающей на фильтрацию равно:
GП=1000Г(n+1)
где Г – гипсовое число; n – отношение Ж/Т.
Рассчитать количество циркулирующей пульпы на 1000 кг фосфата, поступающей на фильтрацию по формуле:
GЦ.П.= КЦ* GП
8. Обозначить физическую теплоту циркулирующей пульпы Q6 за х (МДж).
9. Рассчитать физическую теплоту воздуха, поступающего в экстрактор по формуле:
![]() (15)
(15)
где VВОЗД = 235 000 м3/ч – объем воздуха, поступающий в экстрактор (по практическим данным); Свозд - теплоемкость воздуха, кДж/(кг×К); rВОЗД – плотность воздуха, кг/м3; tвозд - температура воздуха; Рt – парциальное давление водяных паров в насыщенном воздухе (из приложения табл. 7); МН2О - молярная масса воды, кг/кмоль; j - относительная влажность воздуха, доли ед.;Ht В.П. – энтальпия водяных паров, кДж/кг (из приложения табл. 7); РАТМ – атмосферное давление.
10. Рассчитать общий приход теплоты.
11. Рассчитать физическую теплоту пульпы Q8, идущей на фильтрацию по формуле:
Q8 = GП×GАП×cП×tП,
где GАП – расход апатита, кг/ч; cП – теплоемкость пульпы, кДж/(кг×К); tП – температура пульпы, идущей на фильтрацию, °С.
Рассчитать удельную теплоемкость пульпы по формуле, кДж/(кг×К):
CП = сЖ×хЖ + сТВ×хТВ,
где сЖ – теплоемкость жидкой фазы в пульпе; хЖ - массовая доля жидкой фазы в пульпе; сТВ – теплоемкость фосфогипса; хТВ - массовая доля твердой фазы в пульпе. Условно принять, что жидкая фаза представляет собой раствор фосфорной кислоты, а твердая – фосфогипс, тогда сЖ можно определить по формуле (14).
12. Рассчитать физическую теплоту Q9 газов, покидающих экстрактор. Газы, покидающие экстрактор, содержат (без учета испарения водяных паров) HF и воздух. Физическая теплота газов, покидающих экстрактор, рассчитывается по формуле (15).
13. Рассчитать физическую теплоту циркулирующей пульпы Q10, поступающей из экстрактора в вакуум-испаритель для охлаждения по формуле:
Q10 = GЦ.П×cЦ.П×tЦ.П.
14. Рассчитать потери теплоты в окружающую среду Q11.
15. Рассчитать общий расход теплоты: QРАСХ = Q8 + Q9 + Q10 + Q11.
16. Найти из условия теплового баланса х. Пересчитать Q6, Q11, QРАСХ.
17. Составить таблицу теплового баланса экстрактора на часовую производительность.
18. Сделать выводы.
