
Материальный баланс колонны
Таблица №1
Компоненты
|
Молярная масса, кг/кмоль |
Сырье |
Дистиллят |
Кубовый остаток |
|||||||||
Массовый расход GiF кг/ч |
Массовая доля хiF |
Мольный расход NiF кмоль/ч |
Мольная доля хiF |
Массовый расход Gi Р кг/ч |
Массовая доля хiР |
Мольный расход Ni Р кмоль/ч |
Мольная доля хiР |
Массовый расход Gi W кг/ч |
Массовая доля хiW |
Мольный расход Ni W кмоль/ч |
Мольная доля хiW |
||
хл.форм |
119,4 |
2200 |
0,48 |
18,4 |
0,42 |
2176,8 |
0,96 |
18,2 |
0,95 |
23,2 |
0,01 |
0,20 |
0,01 |
Толуол |
92,1 |
2383,3 |
0,52 |
25,9 |
0,58 |
90,7 |
0,04 |
1,0 |
0,05 |
2292,6 |
0,99 |
24,9 |
0,99 |
Сумма |
- |
4583,3 |
1,0 |
44,3 |
1,0 |
2267,5 |
1,0 |
19,2 |
1,0 |
2315,8 |
1,0 |
25,1 |
1,0 |
Определение температурного режима в колонне
Для построения кривых изобар нам необходимо знать зависимость между температурой t и давлением насыщенных паров компонента Рi. Зависимость между температурой t и давлением насыщенных паров компонента Рi, описывается эмпирическим уравнением Антуана:
![]()
Коэффициенты уравнения Антуана
Хлороформ: А = 15,9732; В = 2696,79; С = -46,16; t кип = 61,2оС [6]
Толуол: А = 16,0137; В = 3096,52; С = -53,67; t кип = 110,8оС [6]
В большинстве справочной литературы давления паров приведены в миллиметрах ртутного столба. В этой же единице получается давление и при использовании уравнения Антуана. В промежуточных расчётах использовать эту единицу вполне допустимо. Для упрощения целесообразно перевести в миллиметры ртутного столба также заданное общее давление:
Р = 0,9760 = 684 мм рт. ст.
![]()
Для вычисления равновесных фаз воспользуемся уравнениями:
![]()
![]()
Здесь х и у – мольные доли хлороформа в жидкости и в равновесном с ней паром.
Равновесный состав жидкости (х) и пара(y) температуры кипения (t) бинарной смеси хл.Форм-толуол
Таблица №2.
t, 0С |
Рнкк |
Рвкк |
X, % |
Y, % |
61,2 |
684 |
142,7 |
1 |
1 |
64,7 |
814,5 |
163,4 |
0,80 |
0,95 |
68,2 |
908,6 |
186,5 |
0,69 |
0,92 |
71,7 |
1011,1 |
212,2 |
0,59 |
0,87 |
75,2 |
1122,3 |
240,7 |
0,50 |
0,83 |
78,7 |
1242,8 |
272,2 |
0,42 |
0,77 |
82,2 |
1373 |
307,0 |
0,35 |
0,71 |
85,7 |
1513,5 |
345,3 |
0,29 |
0,64 |
89,2 |
1664,8 |
387,3 |
0,23 |
0,57 |
92,7 |
1827,3 |
433,3 |
0,18 |
0,48 |
96,2 |
2001,7 |
483,5 |
0,13 |
0,39 |
99,7 |
2188,5 |
538,3 |
0,09 |
0,28 |
103,2 |
2388,2 |
597,9 |
0,05 |
0,17 |
106,7 |
2601,3 |
662,6 |
0,01 |
0,04 |
110,8 |
2828,4 |
684 |
0 |
0 |
По данным таблицы № 2 строим диаграммы фазового равновесия в координатах у – х (рис. 2) и t - х, у(рис. 3)
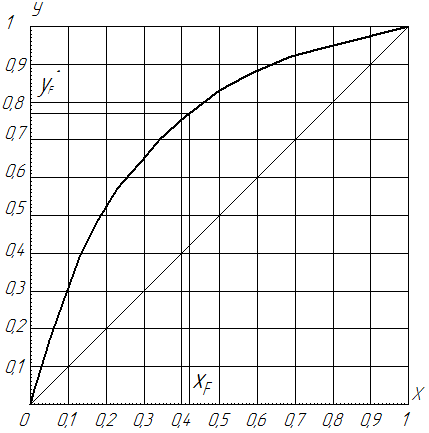
Рис. 2. Диаграмма равновесия между паром и жидкостью в координатах Y – X.
Построение кривых изобар проводится в следующих координатах: по оси абсцисс откладываются мольные составы фаз по НКК, а по оси ординат - температуры кипения НКК и ВКК. По данным таблицы №2 строим график кривых изобар пара и жидкости.
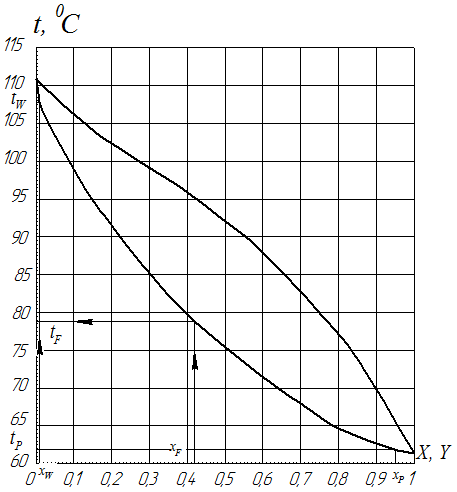
Рис.3 Диаграмма равновесия между паром и жидкостью в координатах t-x,y
Давление вверху и внизу колонны отличается от давления в зоне питания незначительно, поэтому по изобарным температурным кривым кипения и конденсации с достаточной точностью можно определить температуры в зоне питания t F, на верху tD и в кубе t W колонны см. рис 3
Так как сырье поступает в колонну с долей отгона e = 0, для нахождения t F достаточно из точки с абсциссой х F=0,42, соответствующей мольной доле низкокипящего компонента в сырье, восстановить перпендикуляр до пересечения с изобарной температурной кривой кипения. Температура в зоне кипения составляет t F = 78,60С; аналогично определяем температуру в кубе колонны t W = 107,80С; для определения температуры паров на верху колонны t Р из точки с абсциссой х Р = 0,95 восстанавливаем перпендикуляр до пересечения с изобарной температурной кривой конденсации. Температура на верху колонны равна t Р = 61,90С.
Определение оптимального флегмового числа
По графику 2 определяем значение уF* = 0,77
Минимальное флегмовое число Rmin , рассчитываем по уравнению:
Rmin
=![]()
Для проведения ректификации необходимо чтобы оптимальное флегмовое число Rопт было больше Rmin.
Оптимальное флегмовое число Rопт, рассчитываем по уравнению:
Rопт = 1,3 ∙ Rmin + 0,3 = 1,3 ∙ 0,51 + 0,3 = 0,963
Построение рабочих линий процесса
Уравнение рабочей линии верхней части колонны для Rопт имеет вид:
у = (Rопт / (Rопт + 1)) ∙ х + (х нккР / (Rопт + 1))
у = (0,963/(0,963 + 1)) ∙ х + (0,95 / (0,963 + 1)) = 0,4906∙х + 0,4840
Уравнение рабочей линии нижней части колонны для Rопт имеет вид:
у = ((f + Rопт ) / (Rопт + 1)) ∙ х - ((f – 1) / (Rопт + 1)) ∙ хнккW
f = (хнкк Р – хнккW) / (хнккF - хнккW) = (0,95 – 0,01) / (0,42 – 0,01) = 2,2927
у = ((2,2927 +0,963)/(0,963 +1)) ∙х - ((2,2927–1)/(0,963+1))∙ 0,01 = 1,6585∙х - 0,0066
На рисунке 2 изображаем рабочие линии процесса верха и низа колонны.
Верх. Рабочая линия всегда проходит через точку А, лежащую на диагонали диаграммы у-х. Абсцисса точки А равна хнккР= 0,95. Отрезок ОВ, отсекаемый рабочей линией на оси ординат составляет величину
хнккР / (Rопт+ 1) = 0,95 /(0,963 + 1) = 0,48
Рабочая линия верха и низа пересекаются в точке D, абсцисса точки D равна хнккF = 0,42 АD-рабочая линия верха.
Низ. Рабочая линия проходит через точку С, абсцисса которой равна хнккW = 0,02. Соединяем точки С и D получаем рабочую линию низа СD.
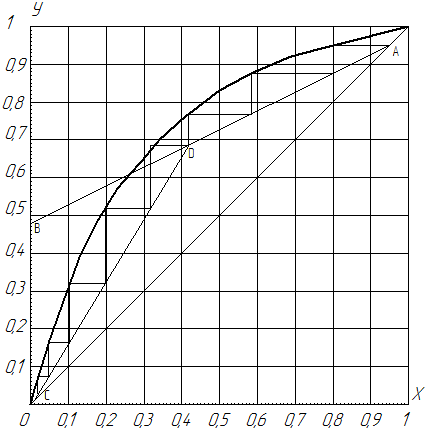
Определение числа теоретических тарелок
Число теоретических тарелок в верхней части колонны nв равно числу ступеней изменения концентрации, вписанных между линией равновесия и прямой АD. Число теоретических тарелок в нижней части колонны mв равно числу ступеней изменения концентрации, вписанных между линией равновесия и прямой СD. Ступень, огибающую т. D отнесем к числу тарелок в верхней части колонны. Число теоретических тарелок в верхней части колонны nв = 3, в нижней части колонны mв = 5
Общее число тарелок nm = 8
Определение расходов пара и флегмы в колонне
Сырье поступает в колонну с долей отгона e = 0, поэтому
qо = GF∙(1-е) = 4583,3 кг/ч.
Массовый расход пара в верхней части колонны находим из уравнения:
GВ = G Р ∙ (Rопт + 1) = 2267,5 ∙ (0,963 + 1) = 4451,1 кг/ч
Так как сырье поступает в жидкой фазе, то в соответствии с уравнениями:
GО = GF ∙ e GО = 0
Gm = G = GВ = 4451,1 кг/ч
Массовый расход флегмы qn, поступающей в зону питания, рассчитываем по уравнению:
qn = Rопт ∙ G Р = 0,963 ∙ 2267,5 = 2183,6 кг/ч
Массовый расход флегмы q, поступающей в нижнюю часть колонны, рассчитываем по уравнению:
q = qо + qn = 4583,3 + 2183,6 = 6766,9 кг/ч
Массовую концентрацию низкокипящего компонента хсм во флегме, поступающей на последнюю тарелку нижней части колонны, определяем из соотношения:
см = (qn ∙ n + qо∙ нк.к F ) / (qо + qn)
n = 1,05 ∙ нк.к F = 1,05 ∙ 0,48 = 0,504
см = (2183,6 ∙ 0,504 + 4583,3 ∙ 0,48) / (6766,9) = 0,49
Массовая концентрация низкокипящего компонента уm в паровом потоке Gm, поднимающемся с последней тарелки нижней части колонны в зону питания составляет:
![]() m
= (q
∙
см
- GW
∙
нк.к W)
/ Gm
m
= (q
∙
см
- GW
∙
нк.к W)
/ Gm
m = (6766,9 ∙ 0,49 – 2315,8 ∙ 0,01) / 4451,5 = 0,74
Массовая концентрация низкокипящего компонента усм в паровом потоке G,в покидающем зону питания определяем из уравнения:
см = (qn ∙ n + G Р∙ нккР ) / G
см = (2183,6∙ 0,504 + 2267,5 ∙0,96) / 4451,5 = 0,74
Проверка: n > см > нк.к F m = см
0,504 > 0,49 > 0,48 0,74 = 0,74
