
Фазові рівноваги та фазові переходи.
Фазою називається сукупність однорідних, однакових за своїми властивостями частин системи. В термодинаміці розглядаються твкрта, рідка та газоподібна фази. За певних умов різні фази однієї речовини можуть знаходитися в рівновазі, контактуючи одна з одною. Перехід з однієї фази в іншу супроводжується поглинанням або виділенням деякої кількості теплоти. Такі фазові переходи називаються фазовими переходами першого роду. Переходи, не пов’язані з поглинанням чи виділенням тепла називаються фазовими переходами другого роду.
Розглянемо фазові переходи першого роду.
 При
нагріванні кристалічної речовини
збільшується амплітуда коливань
її молекул, зростає хаотичність їх
руху, і при досить високій температурі
зникає дальній порядок (речовина
плавиться). Хімічно
прості кристали плавляться
при цілком певній температурі (точка
плавлення).
При
нагріванні кристалічної речовини
збільшується амплітуда коливань
її молекул, зростає хаотичність їх
руху, і при досить високій температурі
зникає дальній порядок (речовина
плавиться). Хімічно
прості кристали плавляться
при цілком певній температурі (точка
плавлення).
аЬ — нагрівання кристала
bс — плавлення
сd — нагрівання рідини (розплаву)
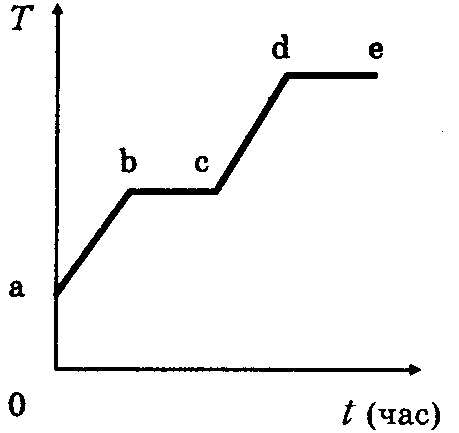 dе
— кипіння
dе
— кипіння
У сплавів існує інтервал температур, у якому відбувається плавлення. Аморфні тіла не плавляться, а розм'якшуються (зменшується їх в'язкість).
Теплофізичні характеристики речовини
1. Питома теплоємність
Чим більшу кількість речовини нагрівають і чим більшої зміни температур Ткінц- Тпоч = dТ треба досягти, тим більше потрібно часу, і тим більший потрібен теплопідвід до речовини:
Для різних речовин однакової m для досягнення однакових dT потрібне різне dQ:
![]()
Коефіцієнт С (від "сарасitу" — ємність) — питома теплоємність.
![]()
Ця величина чисельно дорівнює кількості теплоти, яку одержує чи віддає 1 кг речовини при зміні його температури на 1 К.
2. Питома теплота плавлення
Чим більша маса речовини, яку розплавляють, тим більша потрібна кількість теплоти:
![]()
Питома теплота плавлення λ чисельно дорівнює кількості теплоти, яку необхідно передати одному кілограму кристалічної речовини, нагрітої до температури плавлення, щоб перетворити її в рідину тієї ж температури.
Для процесу кристалізації
![]()
у
цьому випадку ![]() — питома теплота кристалізації.
— питома теплота кристалізації.
3. Питома теплота пароутворення
Як і в попередньому випадку: dQ~т (чим рідини більше, тим довше її випаровувати, тим більше потрібне Q).
![]()
Питома теплота пароутворення r чисельно дорівнює кількості теплоти, необхідній, щоб при незмінній температурі 1 кг рідини перетворити у пару.
(У таблицях значення L наводиться при температурах кипіння рідин.)
Для процесу конденсації
у цьому випадку r— питома теплота конденсації.
4. Питома теплота згорання (теплотворна здатність)
Чем більше згорає палива, тим більше тепловиділення: Q~m. Різні речовини виділяють різні Q:
![]()
Питома теплота згорання q чисельно дорівнює кількості теплоти, яка виділяється при згоранні 1 кг речовини.
Рівняння теплового балансу
Воно виражає закон збереження енергії у процесах теплообміну. Для n тіл, що знаходяться у тепловому контакті:
![]()
