
- •Розділ 3 Ізомерія, класифікація органічних сполук та реакцій Ізомерія
- •Структурна ізомерія
- •Просторова ізомерія (стереоізомерія)
- •Геометричну
- •Оптичну
- •Конформаційну
- •Оптична ізомерія (дзеркальна енантіомерія)
- •Конформаційна (поворотна) ізомерія
- •Класифікація органічних сполук
- •Ациклічні (аліфатичні),
- •Карбоциклічні (аліциклічні та ароматичні),
- •Гетероциклічні.
- •Деякі функціональні групи та відповідні їм класи органічних сполук
- •Класифікація органічних реакцій
- •Основні шляхи утворення вільних радикалів:
- •Поняття про атакуючі реагенти в хімічних реакціях
Розділ 3 Ізомерія, класифікація органічних сполук та реакцій Ізомерія
Органічні сполуки, які мають однакову брутто-формулу, але проявляють різні хімічні властивості, називаються ізомерами, а явище їх існування – ізомерією.
Сполуки, з різною хімічною будовою молекули, створюють тип ізомерії, який називається структурною ізомерією.
Сполуки з однаковою будовою, які проявляють різні властивості, що пов’язано з різним розташуванням фрагментів їх молекул у просторі створюють тип ізомерії, який називається просторовою ізомерією або стереоізомерією.
Структурна ізомерія
Цей різновид ізомерії може бути зумовлений наступними причинами:
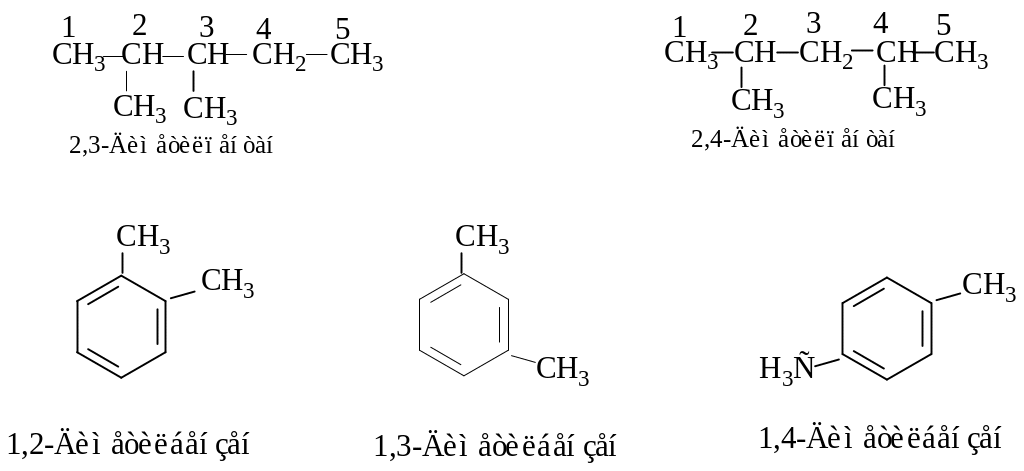
Різною будовою вуглецевого скелета молекули (ізомерія вуглецевого скелета), наприклад:

Різним положенням замісників або кратних зв’язків у ланцюгу (ізомерія положення), наприклад:

Різним взаємним розташуванням атомів або груп атомів у молекулі (ізомерія взаємного положення), наприклад:
Існують й інші різновиди структурної ізомерії, наприклад, метамерія, яка пов’язана з різним розташуванням у вуглецевому ланцюгу гетероатомів, наприклад:

Просторова ізомерія (стереоізомерія)
Стереоізомерія поділяється на такі різновиди:
Геометричну
Оптичну
Конформаційну
Геометрична ізомерія (цис-, транс-ізомерія або π-діастереоізомерія) характерна для алкенів і зумовлена неможливістю вільного обертання груп атомів довкола подвійного зв'язку. Якщо обидва атоми вуглецю при подвійному зв’язку сполучені з різними замісниками, як, наприклад у 2-бутені, то така молекула може існувати у вигляді двох геометричних ізомерів. Той ізомер, у якого два однакових замісника (Н або СН3) розташовані по один бік від площини π-зв'язку, називається цис- а другий, той у якого однакові замісники розташовані по різні боки від площини π-зв'язку — відповідно транс-ізомером


цис-2-Бутен транс-2-Бутен
Геометрична ізомерія властива також аліциклічним сполукам при наявності в одному циклі двох замісників біля різних атомів вуглецю.

цис-1,З-Диметилциклобутан транс-1,3-Диметилциклобутан
Цис- і транс- позначення можна використовувати у випадку наявності двох однакових замісників при обох атомах карбону. При наявності чотирьох різних замісників, згідно з правилами IUPAC, застосовують Z,E-систему позначень. Для цього спочатку визначають старшого замісника при кожному атомі вуглецю. Старшість атома визначається його порядковим номером в періодичній системі елементів. Так, наймолодший замісник водень, за ним ідуть Lі, Ве, С, N, О, F і так далі. У випадку функціональних груп старшість визначається природою першого атому (—SО3Н > —ОН > —NН2 > —СН3), а у випадку їх рівності — природою другого (—СН2—СН3 < —СН2—NН2 < —СН2—OH < —CH2—F) і так далі. При наявності груп з різними типами зв'язків старшість зростає в ряді:
![]() .
.
Якщо
обидва
старших замісники при
обох атомах вуглецю
розміщені
по
один
бік
від
подвійного зв'язку,
то
такий
ізомер позначається Z
(від німецького zusammen
— разом).
Якщо
ж старші замісники розміщені по різні
боки подвійного зв'язку, ізомер
позначається Е
(від німецького entgegen
— навпроти). Символи Z
і Е
не потрібно змішувати з цис-
і транс-.
Z-1-Бромо-2-хлоропропен Е-1-Бромо-2-хлоропропен
