
- •Введение предмет цитологии
- •Краткая история изучения клетки, методы цитологии
- •Общая характеристика и эволюция клеток
- •Поверхностный аппарат клеток Плазматическая мембрана
- •Функции плазматической мембраны
- •Цитоплазма клетки
- •Вакуолярная система цитоплазмы
- •Эндоплазматическая сеть
- •Шероховатая эндоплазматическая сеть
- •Гладкая эндоплазматическая сеть
- •Комплекс Гольджи
- •Лизосомы
- •Вакуоли растительных клеток
- •Пероксисомы
- •Двумембранные органеллы цитоплазмы
- •Митохондрии
- •Пластиды
- •Опорно-двигательная система клетки
- •Микрофиламенты
- •Микротрубочки
- •Промежуточные филаменты
- •Литература
- •Оглавление
Митохондрии
Митохондрии – это окруженные двойной мембраной органеллы, выполняющие роль энергетической станции клетки. Они встречаются в большинстве эукариотических клеток (рис. 19). Исключение составляют зрелые эритроциты млекопитающих и некоторые паразитические простейшие. Основная функция митохондрий заключается в окислении органических молекул и использовании освобождающейся энергии для синтеза АТФ.
Впервые митохондрии были описаны в 1850 году Келликером в мышцах насекомых, в 1890 году Альтманом был разработан метод их окраски фуксином. Однако функциональное назначение митохондрий было выяснено значительно позже. Хотя еще в 20-х годах 20 века Варбургом было показано, что с цитоплазматическими гранулами связано клеточное дыхание, только в 40-х годах, благодаря использованию метода дифференциального центрифугирования, Кеннеди и Ленинджер установили, что дыхание и окислительное фосфорилирование осуществляется митохондриями.

Рис. 19. Схема строения (сверху) и электронная микрофотография митохондрии
Совокупность всех митохондрий одной клетки получила название хондриом. При этом в разных типах клеток хондриом может иметь существенные различия. Во многих клетках он представлен многочисленными разрозненными митохондриями, равномерно локализованными по всей цитоплазме, например, в мало - или недифференцированных клетках. В других клетках митохондрии сконцентрированы в зонах, наиболее интенсивно потребляющих энергию (в зонах эргастоплазмы в активно метаболизирующих и секретирующих клетках, в синапсах нервных клеток, у основания ресничек и т.д.).
Обычно митохондрии такого типа представляют собой зерновидные или нитевидные структуры, размеры и количество которых в разных клетках сильно варьирует. Чаще всего длина митохондрий составляет 1-10 мкм, а толщина 0,5 мкм. Количество митохондрий в клетках печени может достигать 1000, а в ооцитах – 300 000. В клетках зеленых растений их меньше, так как при фотосинтезе также синтезируется АТФ.
При другом типе хондриома в цитоплазме обнаруживается одна гигантская разветвленная митохондрия. Такого рода митохондриальный ретикулум присутствует в поперечно-полосатых мышечных волокнах (рис. 20) и в некоторых одноклеточных зеленых водорослях
Для мышечных волокон наличие единой ветвящейся митохондрии имеет весьма важное функциональное значение. В этом случае протонный градиент равномерно распределяется по всей поверхности внутренней мембраны органеллы, а, следовательно, синтез АТФ может идти в любом ее участке. Благодаря этому обеспечивается поступление макроэргических молекул в любую точку цитоплазмы для одновременного использования их миофибриллами в процессе мышечного сокращения.
Промежуточный тип хондриома представлен в мышце сердца. Здесь соседние митохондрии стыкуются друг с другом с помощью особых контактов, образующих трехмерную сеть. Как и скелетной поперечно-полосатой мышце таким путем осуществляется синхронность сокращения всех саркомеров кардиомиоцита.
В живых клетках митохондрии достаточно динамичны: они могут менять размеры и форму, двигаться, сливаться друг с другом и ветвиться. Например, у иглокожих в ходе онтогенеза происходит слияние митохондрий в одну гигантскую структуру и последующее ее фрагментация.

Рис. 20. Гигантская митохондрия
Реконструкция по серийным электронномикроскопическим фотографиям срезов мышечного волокна (по Ю. С. Ченцову)
Несмотря на большое морфологическое многообразие митохондрий, их ультраструктура в целом имеет единый план строения. Митохондрии окружены двойной мембраной, которые ограничивают две полости: межмембранное пространство и матрикс. Наружная мембрана, как уже отмечалось выше, отличается от внутренней по своим очертаниям, свойствам и химическому составу. В наружной мембране находятся поры, образованные белком порином. Через них в межмембранное пространство из цитозоля беспрепятственно проходят ионы, сахара, аминокислоты и другие вещества. Что касается белков, то их проникновение внутрь митохондрии обеспечивается благодаря присутствию на наружной мембране специфических рецепторов. Большая часть белков, предназначенных для митохондрий, синтезируется на рибосомах в цитозоле. Для взаимодействия с митохондриальным распознающим рецептором эти белки имеют на N-конце сигнальный пептид. В транспорте вновь синтезированных для митохондрий белковых молекул участвуют особые цитозольные белки, называющиеся шаперонами, которые способствуют определенной правильной укладке полипептидных цепей.
Внутренняя митохондриальная мембрана образует многочисленные складки – кристы, направленные внутрь матрикса. Форма и характер расположения крист в разных типах клеток широко варьируют, а их количество и степень развития, как правило, отражают функциональные нагрузки митохондрий в различных клетках и зависят от функциональной активности ткани. Внутренняя митохондриальная мембрана отличается высоким белок-липидным соотношением, что связано с локализацией здесь ферментов дыхательной цепи и АТФ-синтетазного комплекса. Липидный матрикс характеризуется присутствием больших количеств фосфолипида кардиолипина. В отличие от наружной мембраны внутренняя мембрана митохондрий практически непроницаема ни для каких частиц, даже для ионов и протонов.
Внутренняя полость митохондрий – матрикс содержит огромное количество ферментов, участвующих в окислении субстратов в цикле трикарбоновых кислот (цикле Кребса). Кроме того, в матриксе локализуется митохондриальный геном, представленный собственными митохондриальными ДНК и рибосомами, а также компонентами, необходимыми для репликации ДНК и экспрессии соответствующих генов.
Основная функция митохондрий заключается в преобразовании энергии реакций окисления органических субстратов в энергию АТФ, которая используется клеткой для выполнения самых различных функций. В отсутствие митохондрий животная клетка извлекает энергию для синтеза АТФ в результате анаэробного распада глюкозы – гликолиза, который протекает в цитозоле. Но при гликолизе освобождается лишь очень малая часть свободной энергии, заключенной в химических связях сахаров, поскольку имеет место неполное окисление субстрата. В то же время в митохондриях расщепление глюкозы (а также жирных кислот) в присутствии кислорода доводится до конца с образованием углекислого газа и воды. О более высокой эффективности аэробного окисления свидетельствует 18-ти кратное превышение количества молекул АТФ, в которых запасается энергия, при аэробном процессе по сравнению с анаэробным.
В качестве субстратов для окисления в митохондриях используются главным образом жирные кислоты и пировиноградная кислота (ПВК), которая образуется в цитозоле в ходе реакций бескислородного расщепления сахаров. Эти вещества проникают в митохондриальный матрикс, где подвергаются дальнейшему окислению. Здесь они сначала распадаются до двууглеродного соединения (ацетата), соединяющегося с коферментом А. Ацетилкоэнзим А связывается с четырехуглеродным соединением щавелевоуксусной кислотой (ЩУК) с образованием лимонной кислоты (шестиуглеродное соединение), которая далее окисляется в цикле трикарбоновых кислот. В ходе семи последовательных реакций снова образуется ЩУК, которая взаимодействует с новой молекулой ацетилкоэнзима А и цикл повторяется. В результате реакций цикла Кребса из субстратов выделяется две молекулы СО2, а также извлекаются высокоэнергетические электроны. Эти электроны связываются с акцепторными молекулами коферментов НАД (никотинамидадениндикуклеотид) и ФАД (флавинадениндинуклеотид) и быстро передаются в дыхательную цепь, локализованную во внутренней мембране митохондрий. Причем ФАД является непосредственным компонентом дегидрогеназы внутренней мембраны митохондрий, а НАД представляет собой растворимое в матриксе промежуточное соединение, которое переносит электроны на ферменты дыхательной цепи. В конечном счете, богатые энергией электроны, освободившиеся в процессе окисления в цикле трикарбоновых кислот, передаются на молекулярный кислород с помощью встроенных в мембрану переносчиков и образуются молекулы воды.
Дыхательная или электронно-транспортная цепь – это совокупность трех комплексов ферментов внутренней мембраны митохондрий, в которой каждый последующий комплекс обладает большим сродством к электронам, чем предыдущий. Благодаря этому электроны последовательно переходят с одного комплекса на другой, пока не попадут на кислород, обладающий наибольшим сродством к электрону. Иначе говоря, в дыхательной цепи переносчики электронов расположены в соответствии с окислительным потенциалом, который является наиболее высоким у О2. В результате при передаче электронов по цепи от одного переносчика на другой - на все более низкий энергетический уровень – значительная часть их свободной энергии освобождается и может быть использована для синтеза молекул АТФ. Поскольку в дыхательной цепи происходит поэтапное окисление и восстановление ее элементов, энергия электронов выделяется небольшими порциями. В трех точках электронно-транспортной цепи этой энергии выделяется достаточно для синтеза из АДФ и фосфата молекулы АТФ. Этот процесс получил название окислительного фосфорилирования, в котором внутренняя мембрана митохондрий выполняет роль энергопреобразующего устройства. Однако долгое время оставался неясным механизм сопряжения окисления субстратов с синтезом АТФ.
В 1961 году П. Митчелл предложил чисто умозрительную схему сопряжения окисления и фосфорилирования, выдвинув хемиосмотическую гипотезу. Но только через несколько лет были получены необходимые экспериментальные данные, и гипотеза Митчелла получила всеобщее признание. Согласно этой гипотезе, процесс сопряжения идет только в присутствии мембраны и промежуточных богатых энергией веществ, как это имеет место при субстратном фосфорилировании, не образуется. Вместо них существует прямая связь между химическими и транспортными (осмотическими) процессами: при прохождении высокоэнергетических электронов по дыхательной цепи внутренней митохондриальной мембраны от одного переносчика к другому освобождается энергия, которая используется для выведения протонов (Н+) из матрикса в межмембранное пространство. В результате выделяющаяся при транспорте электронов энергия запасается в виде градиента протонов на мембране, т.е. она консервируется не в форме химических связей, а в форме электрохимического градиента. Этот градиент является движущей силой образования АТФ.
Превращение энергии происходит, следовательно, за счет двух взаимосвязанных, но независимых процессов: создания мембранного потенциала вследствие выброса протонов из матрикса и работы протонного насоса, обращающего процесс, что сопровождается синтезом АТФ. Для их осуществления необходимо выполнение, по меньшей мере, двух условий. Во-первых, для обеспечения векторного протекания процессов переносчики в мембране должны быть ориентированы определенным образом и однонаправленно функционировать так, чтобы протоны транслоцировались исключительно в одном направлении. Во-вторых, создание мембранного потенциала возможно только в том случае, если внутренняя мембрана митохондрий непроницаема для протонов.
Ферментная система, которая осуществляет синтез АТФ (АТФ-синтетаза), выявляется на электронных микрофотографиях субмитохондриальных частиц в виде сферических выступов на поверхности внутренней мембраны, обращенной к матриксу. АТФ-синтетаза состоит из двух основных частей: сопрягающего фактора F1, образующего выступы, и протонного канала Fо (рис. 21). Физиологическая роль F1 состоит в том, чтобы катализировать синтез АТФ. Fо- гидрофобный компонент, состоящий из полипептидных цепей «заякоренных» на внутренней митохондриальной мембране – обеспечивает ток протонов через канал от цитоплазматической стороны мембраны к матриксу. Предполагается, что сопряжение переноса протонов через мембрану с синтезом АТФ осуществляется путем конформационных изменений, передаваемых через ферментный комплекс.
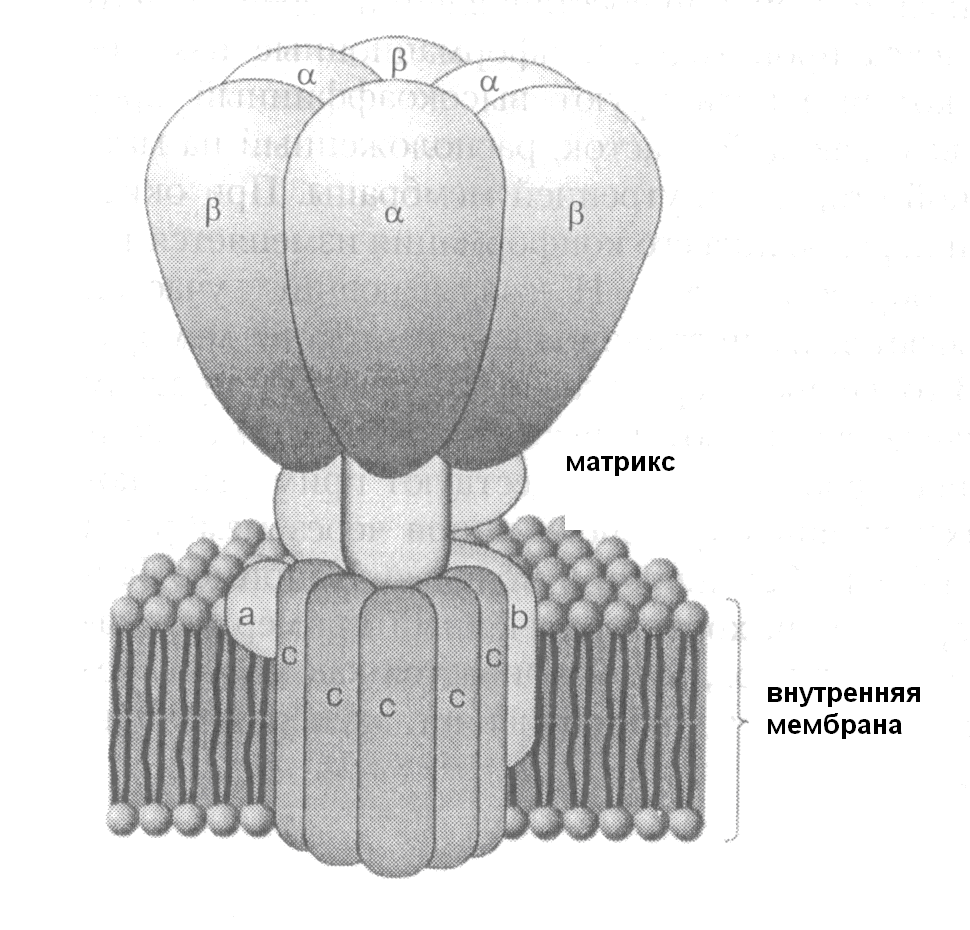
Рис. 21. Схема строения митохондриальной АТФ-синтетазы митохондрий
