
- •Лабораторна робота № 2 одержання піни та дослідження її стійкості
- •1. Піни – важливий клас колоїдних систем
- •2. Методи одержання пін та їх будова
- •3. Стійкість та властивості пін
- •5. Кінетика руйнування піни
- •4. Практичне значення ціноутворення та використання пін. Флотація.
- •Пуста порода
- •Обладнання та реактиви
- •Хід роботи
- •Контрольні запитання
- •Рекомендована література
Пуста порода
Рис. 3. Схема пінної флотації за Песковим і Прейс
Прикладом може служити флотаційне розділення сільвіну (KCl) від галіту (NaCl) в насичених розчинах за допомогою довго ланцюгових амінів, наприклад солі додециламонію. Дивно, що дві подібні між собою солі розділя-ються таким простим реагентом. Це можна пояснити тим, що розміри іону RNH3+ дозволяють входити йому у вакансію К+ , але не дозволяють витіснити іон Na+. Таким чином, міцну адсорбцію амінів на сільвіні можна розгляддати як свого роду ізоморфне поверхневе заміщення. Для відділення бариту BaSO4 від оксидів як колектор використовують олеїнову кислоту. Це ж відноситься і до кальциту CaF2. Дуже імовірно, що сильна адсорбція колектора на бариті і каль-циті зумовлена нерозчинністю солей лужноземельних металів і жирних кислот.
Флотація нерозчинних мінеральних оксидів краще всього пояснюється на основі теорії подвійного електричного шару.
В цьому випадку потенціал поверхні мінералу має таке ж важливе значення, як і специфічна хімічна взаємодія. Потенціалвизначаючим іоном для оксидів є іон водню, причому рН точки нульового заряду сильно залежить від природи поверхні самого оксиду.
Молекули колектора, адсорбованого на оксиді, очевидно, розташовують-ся в штернівському шарі, тобто адсорбція спричинює зменшення потенціа-лу. При високих ступенях заповнення поверхні колектора потенціал може на-віть перевертатись (змінювати знак на протилежний). Це може служити під-твердженням, що в таких системах хімічні сили по меншій мірі співмірні з електростатичними.
Адсорбцію колектора можна підсилювати або ослаблювати вводячи в систему багатозарядні іони, що сприяють адсорбції або пригнічують її.
Миюча дія мил і детергентів (плинів) була б неможливою без утворення піни. Цей процес базується на складному комплексі явищ змочування, відриву забруднення (твердих частинок, масляних плям) від тканини, утворення механічно стійких адсорбційних шарів у піні і утримування забруднень в піні.
Виключне значення мають піни в протипожежній справі, оскільки вони містять у виді дисперсної фази вуглекислий газ. Така піна при нанесенні на предмети, що горять запобігає доступу до них повітря і сприяє згасанню вогню.
Однак інколи виникає необхідність в руйнуванні пін, утворення яких часто небажаний процес. Способи піногасіння, природно базуються на заміщенні або руйнуванні структурних адсорбційних шарів, що стабілізують піну. Деякі піни руйнуються аліловим спиртом, який завдяки своїй високій поверхневій активності, як і при руйнуванні емульсій, здатний витісняти стабілізатор із поверхневого шару, але сам не дає механічно стійких шарів. Для руйнування пін використовують також різні механічні засоби, теплове „перепалювання” плівок та ін.
За допомогою спінювання і наступного видалення піни можна очищувати деякі рідини від вмісту в них ПАР, що при спінюванні переходять в піни. І навпаки, користуючись тим же прийомом, із розчинів можна витягувати наявні там цінні поверхнево-активні речовини.
Обладнання та реактиви
Установка для утворення піни (рис. 4). Мірний циліндр. Секундомір (годинник). Груша об’ємом 250 – 500 см3. Водний 2% розчин некалю.
1
3
5
4
9
6
10
12
10
7
8
11
11
11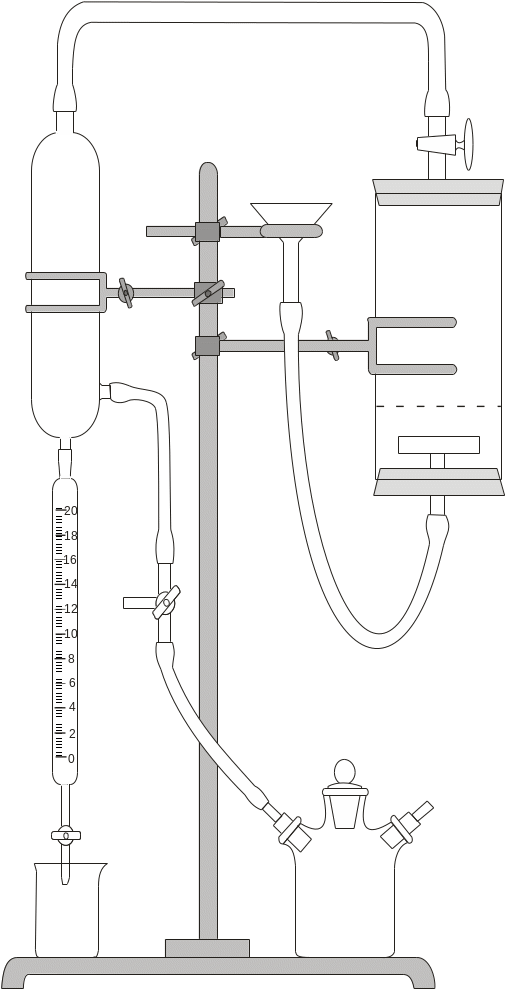



![]()

Рис. 4. Схема лабораторної установки для одержання і дослідження піни.
1 – штатив; 2 піноутворювач; 3 пінозбірник; 4 бюретка; 5 стакан для зливу розчину; 6 буфер; 7 розчин ПАР; 8 барботер; 9 воронка; 10 двоходові крани; 11 з’єднювальні гумові трубки; 12 триходовий кран
