
- •1) Объем газа вступившего в помещение в результате аварийной ситуации.
- •Исходные данные:
- •Xapaктepиcтики paвновесия - си
- •Xapaктepиcтики paвновесия - си
- •Xapaктepиcтики paвновесия - си
- •Xapaктepиcтики paвновесия - си
- •Xapaктepиcтики paвновесия - си
- •Xapaктepиcтики paвновесия - си
- •Xapaктepиcтики paвновесия - си
Министерство образования Российской Федерации
Уфимский Государственный Авиационный Технический Университет
Кафедра АТиТ
Расчетно-графическая работа
“ Метод расчета избыточного давления, развиваемого при сгорании газопаровоздушных смесей в помещении ”
Выполнил: ст.гр. ПБ-302
Худяков Ю.Ю.
Проверил: Лазунов Д.Л.
Уфа-2005
Задание на
расчетно-графическую работу![]()
Через помещение,
свободный объем которого
![]() проходит трубопровод с проходным
сечением диаметром d
проходит трубопровод с проходным
сечением диаметром d![]() ,
по которому транспортируется газ с
расходом
,
по которому транспортируется газ с
расходом
![]()
![]()
![]() при
нормальных условиях и с максимальным
давлением
при
нормальных условиях и с максимальным
давлением
![]() .
Трубопровод оснащен системой
автоматического отключения со временем
срабатывания
.
Трубопровод оснащен системой
автоматического отключения со временем
срабатывания
![]() и с обеспечением резервирования ее
элементов. Длина отсекаемого участка
трубопровода
и с обеспечением резервирования ее
элементов. Длина отсекаемого участка
трубопровода
![]() .
Максимальная возможная температура
для данной климатической зоны t
.
Максимальная возможная температура
для данной климатической зоны t![]() .
.
Рассчитать избыточное давление, температуру и состав продуктов сгорания при горении газовоздушной смеси, возникающем при аварийной разгерметизации трубопровода в производственном помещении.
Произвести оценку возможной степени поражения здания при необходимости обозначить меры по повышению безопасности сооружения.
Исходные данные:
Вариант№110
Газ пропан
![]()
-
Свободный объем помещения
 ;
; -
Диаметр трубопровода
 ;
; -
Расход газа по трубопроводу
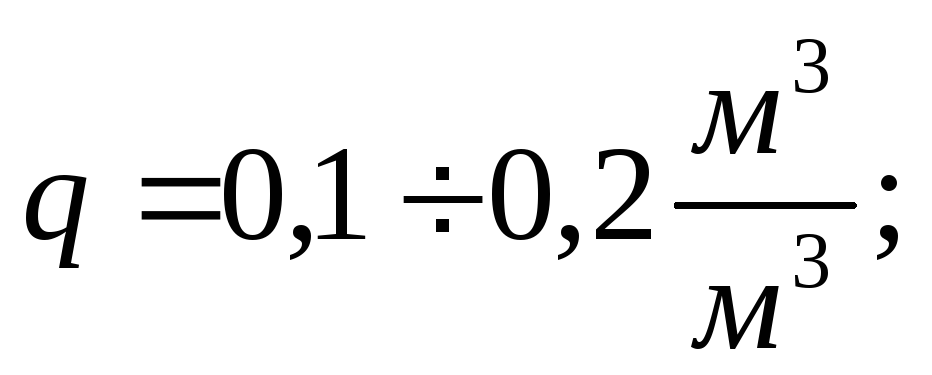
-
Максимальное давление в трубопроводе
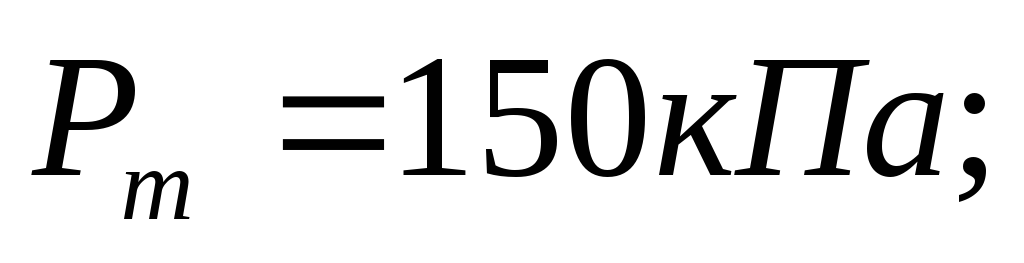
-
Время срабатывания системы автоматического отключения
 ;
; -
Длина отсекаемого участка трубопровода
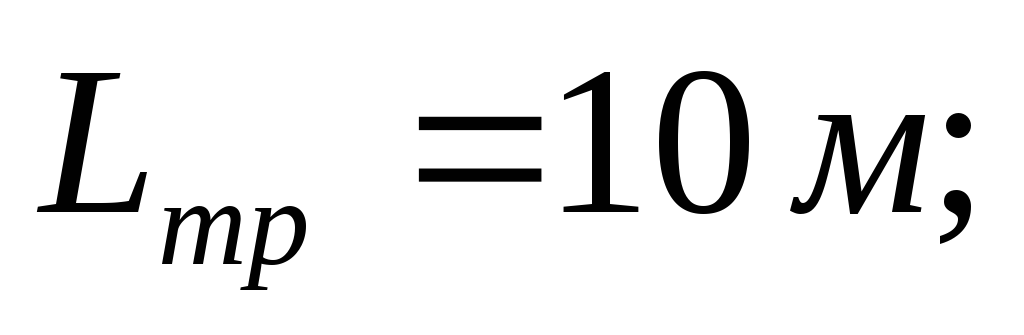
![]()
Последовательность расчета:
1. Теоретический
объем сухого воздуха (![]() )
необходимый для полного сгорания сухого
газообразного топлива
)
необходимый для полного сгорания сухого
газообразного топлива
![]() ;
;
![]()
2. Объем газа вступившего в помещение в результате аварийной ситуации
![]()
![]()
![]()
при
![]()
![]()
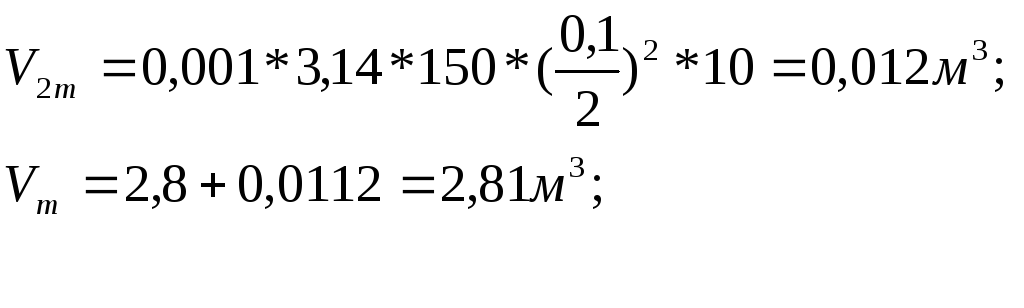
при
![]()
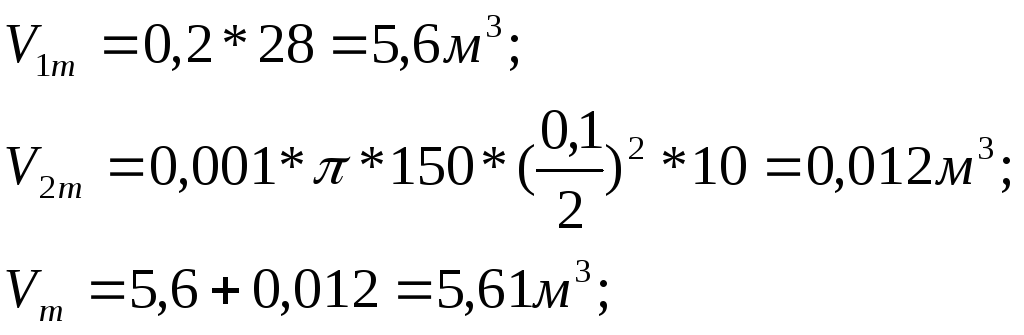
3. Cстехиометрический коэффициент пропана

Таким образом, для сжигания 44 кг пропана требуется 160кг кислорода, а для сжигания 1кг пропана 3,63 кислорода соответственно. Так как кислород составляет кислород 23,2% воздуха можно рассчитать стехиометрический коэффициент для пропана:
![]()
4. Коэффициент избытка воздуха образовавшейся в помещении газовоздушной смеси.
При
![]()
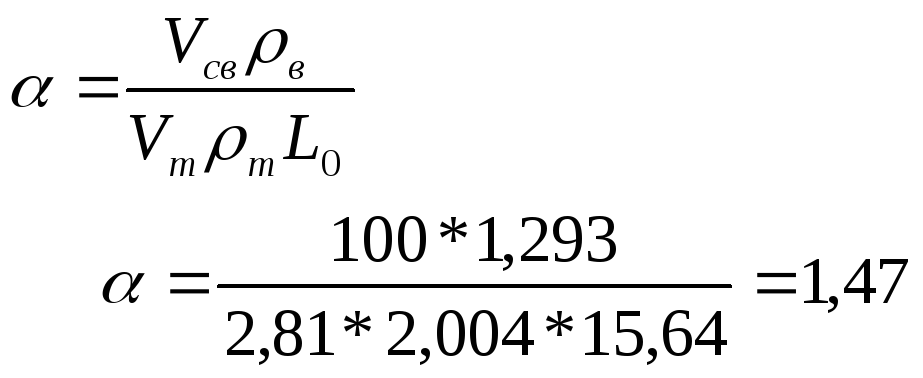
При
![]()
![]()
5. Объемная концентрация газа в помещении
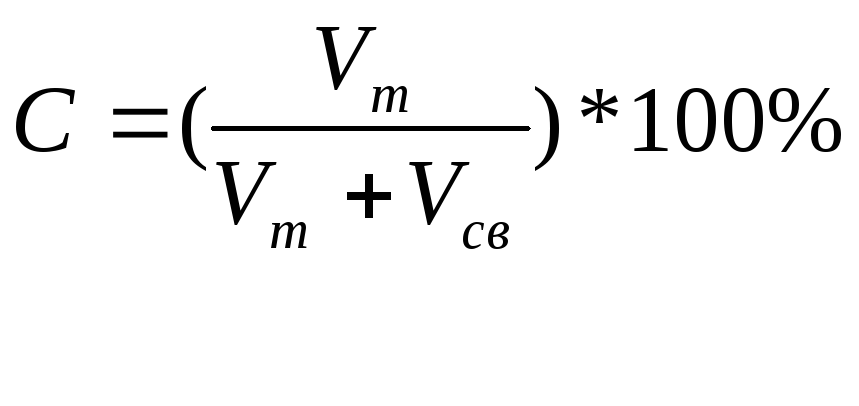 ;
;
при
![]()
![]()

при
![]()
![]()
Полученные концентрации сравниваем с пределами воспламенения и видим что пределы для пропана низший=2,54>2,4, а высший=5,31<9,5.
Так как полученные концентрации лежат в пределах, то смесь (взрывоопасная) воспламенится от случайной искры.
6.Объем газа в помещении при коэффициенте избытка воздуха равном 1.
![]()
7. Стехиометрическая концентрация газа

8. Масса газа
поступившая в помещение при
![]()
![]()
9. Избыточное давление в помещении
![]()
![]() (коэффициент
негермитичности)
(коэффициент
негермитичности)
![]() (
для пропана)
(
для пропана)
![]()
![]()
![]()
по данным таблице№4
степень поражения по
![]() составляет > 100кПа – полное разрушение
здания.
составляет > 100кПа – полное разрушение
здания.
Меры по повышению безопасности объекта: уменьшить время срабатывания автоматического отключения.
10. при помощи программы АСТРА выполняется расчет температуры горения и концентрации образовавшихся продуктов сгорания для полученного диапазона изменения коэффициента избытка воздуха с шагом 0,1. И потом строим зависимости температуры горения T, СO2 и СО от α.
12.Меры по организации безопасной работы объекта.
Я считаю надо понизить время срабатывания автоматики до 5 секунд. Увеличить проветриваемость помещений специальными вентиляторами.
Пересчет параметров с учетов измененного времени.
1) Объем газа вступившего в помещение в результате аварийной ситуации.
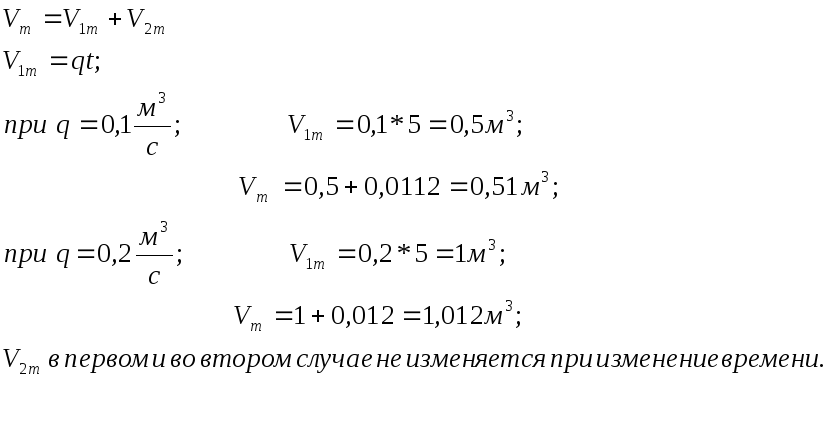
2) Коэффициент избытка воздуха образовавшейся в помещении газовоздушной смеси.
![]()
При
![]()
![]()
![]()
При
![]()
3) Объемная концентрация газа в помещении.

Полученные концентрации сравниваем с пределами воспламенения и видим, что пределы для пропана низший=0,507<2,4, а высший=1,002<9,5.
Видно, что концентрация при q = 0,1м3/с при t = 5с не входит в пределы. Следовательно она не взрывоопасна.
11.Выходные данные, полученные при помощи пакета “Астра”.
Исходные данные:
p = 150, I=0,
Fuel = (C3H8 [-103.85] ),
Ox = (N75.84 O23.2 Ar0.93 C1O2 0.03 ),
alpha = 0.74, 0.84, 0.94, 1.14, 1.24, 1.34, 1.44 ;
Xapaктepиcтики paвновесия - СИ
P= 15OOO+O3 T= 29512+O4 V= 63575-O2 S= 87589+O1 I= OOOOO-OO
U=-95363+O3 M= 38863+O2 Cp= 17O81+O1 k= 12333+O1 Cp"= 1874O+O1
k"= 12347+O1 A= 1O797+O4 Mu= 8O972-O4 Lt= 21892+OO Lt"= 25235+OO
MM= 25732+O2 Cp.г= 17O81+O1 k.г= 12333+O1 MM.г= 25732+O2 R.г= 32313+O3
Z= OOOOO-OO Пл= OOOOO-OO Bm= 14863+OO
Coдepжaниe кoмпoнeнтoв - мoль/кг
O 39335-O3 O2 65522-O3 H 32246-O1
H2 21769+O1 OH 432O3-O1 HO2 13668-O4
H2O 91992+O1 H2O2 23912-O4 Ar 45O84+OO
N 68836-O5 N2 17893+O2 NO 1197O-O1
NO2 252O4-O5 N2O 2O118-O4 NH 69939-O4
NH2 23585-O3 NH3 37227-O2 N2H2 3O817-O6
HN3 25143-O7 HNO 49384-O4 HNO2 42774-O5
NH3O 87735-O7 CO 54355+O1 CO2 31312+O1
C2O 14187-O7 CH2 43946-O7 CH3 174O8-O5
CH4 75356-O5 C2H2 28O41-O7 CHO 5442O-O3
CHO2 3992O-O3 CH2O 18848-O3 CH2O2 6538O-O3
CH3O 1288O-O7 CN 79828-O6 N2C 48169+OO
CN2 7O111-O7 NCO 13266-O5 HCN 61993-O3
HNC 12541-O5 -1*OH 1912O-O7 +1*H3O 3O69O-O7
эл.газ 11O86-O7
Xapaктepиcтики paвновесия - си
P= 15OOO+O3 T= 31159+O4 V= 64517-O2 S= 85887+O1 I= OOOOO-OO
U=-96776+O3 M= 37354+O2 Cp= 16734+O1 k= 12279+O1 Cp"= 19372+O1
k"= 12118+O1 A= 1O8O3+O4 Mu= 84181-O4 Lt= 21588+OO Lt"= 26133+OO
MM= 26771+O2 Cp.г= 16734+O1 k.г= 12279+O1 MM.г= 26771+O2 R.г= 31O58+O3
Z= OOOOO-OO Пл= OOOOO-OO Bm= 15942+OO
Coдepжaниe кoмпoнeнтoв - мoль/кг
O 22377-O2 O2 72979-O2 H 36479-O1
H2 1O764+O1 OH 1O948+OO HO2 11O66-O3
H2O 9OOO6+O1 H2O2 1O164-O3 Ar 458O5+OO
N 194O3-O4 N2 185O4+O2 N3 14264-O7
NO 49429-O1 NO2 31662-O4 N2O 8698O-O4
NH 1O4O4-O3 NH2 18145-O3 NH3 12249-O2
N2H2 26852-O6 HN3 3736O-O7 HNO 15233-O3
HNO2 3O537-O4 NH3O 11596-O6 CO 38O6O+O1
CO2 41531+O1 CH2 13651-O7 CH3 23O32-O6
CH4 45822-O6 CHO 38O13-O3 CHO2 5593O-O3
CH2O 6836O-O4 CH2O2 46732-O3 CN 56628-O6
N2C 14684+OO CN2 48942-O7 NCO 18512-O5
HCN 16385-O3 HNC 476O1-O6 -1*OH 57O51-O7
+1*H3O 75O5O-O7 эл.газ 21O52-O7
