
- •Студент пәнінің
- •«Пайдалы қазбалар кенорындарын іздеу және барлаудың
- •1.5 Пәннің мақсаттары мен міндеттері
- •Сабақтардың тізімі мен түрлері, оларды орындау графигі
- •1.7 Пайдаланылатын әдебиет
- •1.8 Білімді бақылау және бағалау
- •1.9 Курстың саясаты мен процедурасы
- •2 Таратылып берілетін материалдардың мазмұны
- •2.1 Курстың тақырыптық жоспары
- •2.2 Дәрістік сабақтардың конспектісі
- •Түпкі таужыныстарда жоғары концентрацияда орналасқан элементтер ассоциациясы
- •Әртүрлі типті кенорындардағы элементтердің ассоциациялары
- •Туынды шашырау ореолдары бойынша литохимиялық іздеулердің масштабтары
- •2.3 Зертханалық сабақтардың жоспары
- •2.4 Студенттердің оқытушының басшылығымен өздігінен жүргізетін жұмысы (соөж)
- •2.5 Студенттердің өздігінен жұмысы (сөж) ауқымындағы сабақтардың жоспары
- •2.6 Өзіндік бақылау үшін тест тапсырмалары
- •2.7 Өтілген курс бойынша емтихандық сұрақтар
- •Глоссарий
- •050706 – «Геология және пайдалы қазба кенорындарын барлау» мамандығы үшін
2.2 Дәрістік сабақтардың конспектісі
1-ші дәрістің тақырыбы. Жер қыртысындағы химиялық элементтердің концентрациясы және шашырау процесін зерттейтін гехимияның ғылым ретінде қалыптасуы.
Мазмұны: Геохимия – жер қыртысының химиялық құрамы жайлы және химиялық элементтердің миграциясы, шашырауы және концентрациясы жайлы ғылым. Ең алғаш біздің елімізде ХХ ғасырдың басында пайда болған.
Геохимияның ғылым ретінде құрылуында В.И. Вернадскийдің, А.Е.Ферсманның және В.Н.Гольдшмидтің еңбектері жетекші рольді атқарады.
Өзінің қысқа ғана даму уақыты аралығында екі ғылымның (геология және химия) негізінде дамитын геохимия үлкен жетістіктерге жетіп, геологиялық ғылымдар циклінде минералогия және петрография ғылымдары сияқты өзінің орнын тапты.
Өзіндік ғылым сияқты геохимияның өз пәні және зерттеу тапсырмалары, өзінің зерттеу әдістерімен әдістемелері бар.
Геохимиялық зерттеулердің нысаны болып, ең алдымен Жердегі элементтердің атомы болып келеді. Сонымен қатар, геохимия Жерден тысқары – космостық денелерде және жаралымдарда (космохимия) химиялық элементтердің атомдарын зерттейді.
1924 жылы В.И.Вернадский геохимия нені зерттейтінін анықтаған:
1) Жер қыртысының химиялық элементтерін, яғни атомдарын, олардың тарихын, таралуын және кеңістікте – уақытта қозғалуын және олардың генетикалық байланысын;
2) Кейбір элементтердің жер қыртысындағы және оның кейбір бөліктерінде сандық және сапалық таралуын;
3) Элементтердің орын ауыстыру (миграция), шашырау немесе жиналу заңдылықтарын;
4) Жер қыртысының әртүрлі жағдайындағы элементтердің өзара байланыс заңдылықтарын;
5) Тірі заттардың, таужыныстардың, топырақтың құрылысында элементтердің қатысу заңдылығын.
Геохимия атомды зерттеу негізінде пайда болған. Химиялық элемент, минералдардың және таужыныстардың химиялық құрамы, кендерді және пайдалы минералдарды іздеу түсініктері бұрыннан келе жатқан түсініктер. Бұл түсініктер б.э.д. 460-370 ж.ж. Демокриттің, Аристотельдің жұмыстарында және де Авиценнаның (985-1057), Бойлдың (1627-1691), Лавуазьенің (1743-1794) және т.б. жұмыстарында көрсетілген.
М.В. Ломоносовтың (1711-1765) жұмыстарында терең геохимиялық идеалар жатыр. Оның жұмыстарындағы ең негізгісі табиғаттың құбылыстарына химиялық бағытпен және тарихи тұрғыдан қарау. М.В. Ломоносовтың жұмыстарының негізінде заттың атомдық құрылысының гипотезасы жатыр. Ол жаратылыстанудың негізгі заңы болып келетін және геохимиялық құбылыстарға маңызды болатын, яғни табиғаттағы химиялық элементтердің миграция процесін түсіну үшін «Заттың және энергияның сақталуы» атты заңды шығарған. М.В.Ломоносовтың геохимиялық көзқарастарының негізінде біз өмір сүретін өмірдің өгергіштігі жайлы идеялар жатыр. М.В. Ломоносов қазіргі ғылымға да қажетті бірқатар геохимиялық идеяларды айтқан: минералдардың жаралуының жағдайы жайлы; минералдардың және элементтердің парагенезисі жайлы; геохимиялық іздеудің критерийі ретінде минералдардың типоморфтық қасиеттері жайлы; химиялық элементтердің миграциясы туралы; минералдар жаралудағы тірі организмдердің ролі жайлы және т.б.
М.В. Ломоносовтың геохимиялық идеяларын В.М. Севергин, В.И.Вернадский, А.Е.Ферсман және т.б. орыс және қазіргі ғалымдар дамытқан.
Геохимиялық зерттеулердің нысаны болып келетін химиялық элементтердің атомдары жайлы қазіргі көзқарастар тек қана Д.И.Менделеевтің периодтық заңы ашылғаннан кейін, радиоактивтіліктің және басқа да физикалық құбылыстардың ашылуы нәтижесінде және осының негізінде қазіргі атомдардың моделі құрастырылғаннан кейін мүмкіндікке ие болды. Д.И. Менделеевтің периодтық жүйесі химиялық элементтердің атомдары жайлы қазіргі зерттеулерге бастама болды және химиялық элементтердің табиғи жағдайда бірігу және таралу заңдылығын жүйелі түрде зерттеуге мүмкіндік берді.
1982 жылы Америкалық геологиялық комитеттің химигі Ф.У. Кларк үлкен фактілік материалдар негізінде жер қыртысындағы негізгі 30-40 химиялық элементтердің таралуы жайлы нақты сандық мәліметтер берді.
Ресейде геохимияның пайда болуы кездейсоқ жайт емес, ол хиимялық-генетикалық минералогияның (минералогияны «жер қыртысының химиясы» деп түсінген) негізінде пайда болды.
Геохимия бойынша ең алғаш дәрістер курсын А.Л.Шенявский атындағы Мәскеу университетінде 1912 жылы А.Е.Ферсман оқыған. Кейіннен осы дәрістер жинағы баспадан шығарылған.
Геохимияның дамуында норвегия ғалымы В.М.Гольдшмидт үлкен үлес қосқан болатын. Ол кристаллохимиялық бағыттарды дамытатын бірқатар геохимиялық сұрақтарды зерттеді. М.Лауе рентгендік сәулелерді кристалдық торларда атомдар мен иондардың тәртібін зерттеуде қолдануды енгізген. Осы мәселе геохимия ғылымының алдында жаңа перспективаларды ашты.
Егер ең алдымен В.И.Вернадский, содан кейін А.Е.Ферсман және В.М.Гольдшмид 1923 жылы геохимиялық сұрақтарды атом құрылысының сұрақтарымен байланыстырмаған болса және геохимияға өте маңызды ережені(химиялық элементтердің атомдарының құрылысы олардың табиғаттағы тәртібін анықтайды ) құрастырмаған болса, онда геохимия ғылымы тек қана қағаз жүзінде жазылған ғылым болып қалар еді.
Геохимия ғылым ретінде геологиялық, физикалық, химиялық және математикалық циклдардың пәндерімен тығыз байланысты қажет етеді. Геохимия геологиялық ғылымдар циклінің ішінде жинақтайтын ғылым болып келеді. Себебі оның негізінде химиялық элементтердің атомы жатыр.
Геохимия минералогиямен тығыс байланыста болады. Бұл ғылымдардың минералогиялық және геохимиялық процестерде ортақтығы өте көп. Бірақ сонымен қатар, жер қыртысындағы химиялық элементтердің атомын зерттейтін геохимия ғылымы зерттеу нысаны геохимия сияқты сол кеңістікте, Жер тарихының дәл сол уақытындағы атомдар молекулаларының қосылуын зерттейтін минералогиядан ғылымынан біршама өзгешеленеді.
Жер қыртысы – қалыңдығы 15-70 км болып клетін Жердің тасты қабығы (литосфера), жоғары жағында атмосферамен және гидросферамен, ал төменгі бөлігінде сейсмикалық Мохоровичич бөлімі деп аталатын қабатпен (сейсмикалық толқындардың көрсеткіші 6-7 ткм/с. 13-16 ткм/с. дейін өзгереді) шекараланады.
Негізгі әдебиет: [6], 450-454 б.
Қосымша әдебиет: [7], [8], [10]
Бақылау сұрақтары:
1) Геохимия қандай ғылымдармен тығыз байланысыты?
2) Геохимияда зерттеу нысанына не жатады?
3) Геохимияның құрылуында М.В.Ломоносовтың сіңірген еңбегі?
4) Геохимия үшін Д.И.Менделеев ашқан жаңалықтың мәні?
5) Геохимияның ғылым ретінде дамуына шет ел ғалымдарынан кім үлкен қосты?
2-ші дәрістің тақырыбы. Жер қыртысындағы элементтерді анықтаудың түрлері.
Мазмұны: Жер қыртысындағы химиялық элементтердің бөлінуі және орын ауыстыруы оның құрылысының ерекшеліктерімен, анықтау түрімен, сонымен қатар сол элементтер орналасқан сыртқы жағдайлардың кешенімен анықталады. Осы факторларды геохимиялық іздеу әдістерімен пайдалы қазба кенорындарын іздеу барысында ескеретін болса, онда қарастырылып отырған элементтердің миграция жолдарын және оның дамуын дәл анықтауға мүмкіндік береді.
Жер қыртысындағы элементтер тұрақты химиялық тепе-теңдік жүйесін құрайды. Осындай жүйелердің тобы химиялық элементтерді анықтаудың түрлері деген атға ие болды. Әр түрлі формада орналасқан элементтердің тәртібін білу іздеу болжамдарының сенімділігін арттыруға септігін тигізеді. Жер қыртысындағы элементтерді анықтаудың төмендегідей сегіз түрі бөлінеді:
1) Жеке минералдық түрлер (кристаллдық және коллоидтық жүйелер – молекулалар және олардың қосындылары). Химиялық элементтердің бұл түрі литосфераға өте маңызды болып келеді. Элементтер осындай түрде болып, әрдайым өзара тұрақты байланыста миграцияланады. Элементтердің мұндай түріне қатты дисперстік ортасы бар коллоидтық жүйелердің аз ғана мөлшері жатқызылады (кристаллозолдар және кристаллогелдер). Осыларды құрайтын элементтердің миграциясы тек қана минералды түрде және тек бірге өтеді. Бірақ, элементтердің өзара қатынасы әрбір жеке сынықта әр түрлі болуы мүмкін. Бұл ерекшелік коллоидтық минералдарды изоморфтық қосылыстарға жақындатады.
Қазіргі кезде 2400 жеке минералдық түрлер және 7000 астам түрлері бар. Олар өз кезегінде таралуына байланысты 5 топқа бөлінеді:
а) өте көп таралғандар, саны бойынша таужыныстардың біршама бөлігін қамтиды (дала шпаттары, кварц, слюдалар, кальцит және т.б.).
б) таралғандар, саны бойынша сирек таужыныстардың бөлігін қамтиды немесе көптеген таужыныстардың шағын ғана бөлігін қамтиды (апатит, нефелин, лейцит және т.б.).
в) орташа таралғандар, таужыныс құраушы емес, бірақ пайдалы қазба кенорындарының кендерінде көп мөлшерде кездеседі (пирит, халькопирит, галенит, ильменит).
г) сирек, кенорындарда аз мөлшерде кездесетіндер (саф алтын, сильвин, витерит, бериллий, тантал, ниобий минералдары және т.б.).
д) өте сирек, Жер шарының тек қана 10 немесе одан да аз нүктелерінде анықталған, өте аз мөлшерде кездеметіндер (криолит, германит, рейнерит және т.б.)
Жер қыртысындағы минералдардың әр түрлі кластарының
салмақтық мөлшері 1 - кесте
Минералдық класс |
Минералдардың минималды саны |
Жер қыртысында құрайтын салмағы, % |
Осы кластың жиі минералдық құрамына кіретін элементтер |
Таза (саф) элементтер |
90 |
0,1 |
Pt және оның тобы Au, Ag, Cu, Hg, Bi, C, S, As |
Cульфидтер және олардың аналогтары |
200 |
0,25 |
S, Se, Sb, Te, As, Fe, Cu, Pb, Zn, Co, Ni, Hg, Bi, Mo, Au |
Тотықтар |
200 |
17,0 |
O, Si, Fe, Al, H, Ti, Mn, Cr, Sn,Nb, Ta, TR |
Силикаттар |
800 |
80,0 |
O, Si, Fe, Al, Ca, Na, K, Mg, сирек Mn, Ti, B және т.б. |
Карбонаттар |
80 |
1,7 |
C, O, Ca, шамалы Fe, Na, Ba, Sr?, Cu, Pb, Zn |
Бораттар |
40 |
Шамалы мөлшерде |
B, O, Ca, Mg, H кейде S, Cl |
Фосфаттар,арсенаттар, ванадаттар |
350 |
0,7 |
P, AS, V, Ca, Mg, Fe, Mn, шамалы Al, H, сирек Pb, Cu, Zn, Cl, F, U |
Сульфаттар |
260 |
0,1 |
S, O, Na, K, Mg, Ca, Al, Fe, H, сирек Pb, Cu, Sn, Ba, Sr |
Хроматтар, молибдаттар, вольфраматтар |
15 |
Шамалы мөлшерде |
Sr, Mo, W, O, Fe, Mn, Pb, Cu, Ca, H |
Галогенидтер |
100 |
Шамалы мөлшерде |
F, Cl, Ca, Mg, Na, K, Al, кейде Li, H, O |
|
2135 |
99,85 |
|
Химиялық элементтердің жеке түрлерін жаратылуының әртүрлі қабілеттері бар. Кестеге қарайтын болсақ, жер қыртысының құрамындағы әртүрлі кластардың салмақтық мөлшері және жеке элементтердің минералдар түзудегі қатынасы әртүрлі.
Жер қыртысында негізгі минерал түзуші элементтер мыналар: O, Si, Al, Fe, Ca, Na, K, Mg, Ti, H, C, Mn, P, S ( яғни 14 элемент). Ал мына элементтерден басқалары Cu, Zn, Pb, TR, Nb, Ta, Be, As, Sb, U минералдардың аз ғана санын құрайды немесе мүлдем құрамайды ( Pb, Hf, Zn, инертті газдар, радиоактивтік элеменнтер қатары).
2) Минералдардағы изоморфты қосылыстар. Минералдардың химиялық құрамының мәліметтерін қарағанда қарапайым бинарлы қосылыстардың құрамы талдаулар нәтижесі бойынша біршама күрделі екені бұрыннан анықталған. Мысалы: қарапайым құрамды қосынды ZnS (сфалерит) бірқатар элементтердің қосылыстарынан тұруы мүмкін (Zn, Fe, Mn, Cd, Ga, Se, Sn, S, Sc). Сирек табиғи қосындылар – минералдар екі немесе үш қосындылардың қосылыстарынан тұрады. Мысалы: плагиоклаз екі анықталған қосындыдан тұрады – альбит (Na [Al Si3 O8]) және анортиттен (Ca [Al2Si2O8]).
Мұндай қосындыларды «аралас кристалдар» деп атайды. Ал осы аралас қосындыларды тұғызған құбылысты изомроф немесе изоморфизм деп атайды.
В.И.Вернадский (1909-1910) Жер қыртысының минералдарындағы химиялық элементтерінің орналасуы жайлы эмпирикалық мәліметтердің негізінде изоморфизмнің классикалық эмпирикалық қатарын ұсынды. Оның бір сіңірген еңбегі ол изоморфтық алмасулардағы термодинамикалық жағдайлардың ролін ең алғаш көрсетті, яғни изоморфты қатарлар температура мен қысымның әсерімен қозғалады.
В.И.Вернадский бойынша Элементтердің изоморфты қатарлары
1. Al, Fe, Cr, Mn, Ti, B (V), (Cl), V 6. NH4, K, Na, Cs, Rb, Te, Li, H
I I
II II, III
III
2. Ba, Ca, Sr, Pb 7. W, Mo 8. Ge. Se
I, II
III I I
3. Br, J, Cl, F, OH 9. Mg, Mn, Fe, Zn, Be, Cd, Cu, Ni, Co
I I
II, III II, III
4. V, P, As, Sb 10. Au, Ag, Hg, Cu, Pb, Tl
I
I II, III
5. Bi, Sb, As 11. Pt, Fe, Cd, Zr, Rh, Cu
I III
12. Os, Ru, Rh, Zr 13. Ca, Mg, Mn 14. O, F, OH 15. Co, Te, Ni
I I
III II, III III II
16. Si, Ti, Zr, Sn, Mn, Th 17. Nb, Ta 18. S, Se, Te
II,III I,II,III II, III
I. Мору қыртысы, төмен температура (Т) және қысым (Р) (гиперг)
II. Метоморфизация облысы, жоғары қысым (Р) және жоғары емес температура (Т)
III. Магматизация облысы, жоғары температура (Т) және қысым (Р) облысы
Вернадскийдің осы 18 қатарын қарай отырып келесідей қорытындыға келуге болады, изоморфты арасудың кең ауқымы температура және қысым жоғары мөлшердегі терең магмалық және метаморфтық түзілімдерге тиісті болып келеді. Егер термодинамикалық жағдайлар элементтердің изоморфты алмасуының дәрежесін жақсартса, кристаллохимиялық факторлар осы алмасулардың мүмкіндігін анықтайды.
Изоморфты алмасулардың мүмкіндігін анықтайтын факторлар:
1) атомдардың координациялық саны (kr) - бұл кристаллохимияның негізгі түсініктерінің бірі, кез-келген атомдар мен иондарды жақын қашықтықта қоршап тұратын атомдар мен иондардың санын көрсетеді;
2) байланыс конфигурацияларының типі (коваленнті қосындыларда);
3) атомдардың валенттілігі.
Изоморфизм дәрежесінің жақсартылуын анықтайтын фактор – атомаралық байланыс және химиялық байланыстың типі.
Жоғарыда айтылған сөздерге негізделе отырып изоморфизм түсінігін былай қорытындылауға болады: изоморфизм дегеніміз тек қана атомдардың бірдей координациялық сандарында, ал ковалентті қосындыларда - байланыс конфигурациясының жоғарылауы (оның жоғарылау дәрежесі атомаралық қашықтықтың жақын болуымен, химиялық байланыстың типімен және атомның электрондық қабығының құрылысымен анықталады) кезінде мүмкін болатын аналогтық элементтердің минералдардың құрылымында бір-бірін алмастыру қасиеті.
Изоморфизді екі түрге бөледі – изовалентті және гетеровалентті. Бірінші жағдайда, егер иондар арасындағы радиус жақындаған болса және кристалдық тордың балансы сақталса иондар бірдей зарядты (бірдей валентті) болады:
1) Ta+5 ион радиусы 0,68 және Nb+5 – 0,69 (қатарда танталит және колумбит);
2) Mg+2 – Fe+2 және Fe+2 – Mg+2 - жетілген изоморфизнің мысалы болып келеді (ромб Пх, оливин тобы, Пх және Аmf тобы);
3) Mn+2 – Ca+2 – волластонит – родонит және кальцит – родохрозит;
4) Zr+4 (0,87) – Hg+4 (0,86) - цирконда;
5) Al+3 (0,57) – Ga+3 (0,62) – нефелинде және басқа да алюмосиликаттарда;
6) Mo+4 (0,68) және Re+4 (0,68) – молибдениттерде;
7) K+1 (1,33) және Rb+1 (1,49) – дала шпаттарында және слюдаларда;
8) Mg+2 (0,78) және Ni+2 (0,78) – оливиндерде.
Гетеровалентті изоморфизм кезінде әртүрлі зарядтардағы иондардың өзара алмасуы жүзеге асады. Бұл жағдайда, иондар алмасуға тордың қосынды балансы өзгермейтіндей етіліп ұшырайды.
Мысалы, егер аз зарядты катион үлкен зарядты катионға алмасатын болса (және керісінше), онда зарядтардың компенсациясы болуы қажет. Бөл компенсация үш түрлі әдіспен жүзеге асырылады:
1) үлкен зарядты бір катионның орнына кіші зарядты катионның көп мөлшері торға кіреді немесе керісінше ( 2 Al+3 – 3 Mn+2 – слюдаларда, 2 Na+1 – Ca+2 – нефелинде, 3Ca+3 – 2 Y+3 - иттрафлюориттерде);
2) кіші зарядты алмастыратын үлкен зарядты катионмен бірге, параллелді басқа катионның орнына кіші зарядты катион кіреді (2Ca+2 - ∑TR+3 + Na+1 – апатиттерде, 2 Mg+2 – Al+3 + Li+1 – пироксендерде, Si+4 Na+1 – Al+3 Ca+2 - плагиоклаздарда);
3) үлкен зарядты катионның кіруі кезінде қосындының анионды бөлігінде өзгеріс байқалады. Кіші зарядты анион үлкен зарядты анионмен алмасады (Ca+3 + F-1 - ∑ TR+3 +O-2 - апатиттерде).
3) Биогендік түрі. Ол жануарларда және өсімдік ағзаларында элеменнтерді анықтаумен сипатталады. Ең алғаш В.И.Вернадский биосфераны зерттегенде қарастырылған. Жер үстіндегі өтіп жатқан геохимиялық процестерді тірі организмдердің әрекетін ескермей нақты сипаттауға болмайды (сонымен қатар, туынды геохимиялық ореолдардың пайда болу процесін). Тірі организдерде қазір барлық элементтер анықталған. Өсімдіктерде олар күрделі органикалық қосынды ретінде кездеседі. Көптеген металлдар, табиғи органикалық қышқылдармен әсерлесіп, қосындыларды туғызады. Бұл қосындылар соңғы кезде геохимиялық іздеу жұмыстарын жүргізу кезінде ескерілетін болған.
4) Сулы ерітінділер – гидросфера деп аталатын Жердің жеке қабығын құрайды. Сулы ерітінділердің негізгі бөлігі дүниежүзілік мұхиттың еншісіне тиеді, ал ғана бөлігі – континенттердің жерүсті және жерасты суларына тиеді. Оларға әртүрлі жағдайда пайда болған гидротермалар жатады. Геохимиялық іздеулер кезінде негізгі көңіл элементтер ион, молекула, органикалық және кешенді қосындылар ретінде кездесетінжерасты және сирек жерүсті суларға бөлінеді. Элементтердің негізгі бөлігі, ерітінділердегі диссоциация процесінің нәтижесінде аниондармен және катиондармен көрсетілген. Аниондар (теріс зарядты ион) негізінен кешенді, ал катиондар (оң зарядты ион) судың молекулаларымен байланысты болады. Иондардың бөлінуі судағы ионды, металлды және ковалентті байланыстағы заттардың еруімен анықталады.
Сулы ерітінділердегі иондардың орын ауыстыруы электростатикалық қасиетке (кристаллизациялық қасиет), сонымен қатар ерітінділерде болып тұратын өзгерістермен және ерітіндіде болатын еритін иондардың басқа заттармен реакциясына байланысты болады. Нейтралды молекулалы иондарға қосылу немесе қарама-қарсы белгідегі иондарға қосылу кезінде көптеген элементтер табиғи сулы ерітінділерде кешенді қосындылар түрінде тасымалданады.
5) Сұйық дисперсті орталы коллоидтар. Элементтерді анықтаудың бұл түрі табиғатта кеңінен таралған. Бұлар континентті және мұхиттық суларда кездеседі, одан басқа, «өзінің кейпін білдіретін ландшафтың өте маңызды бөліктері, немесе коллоиды күйде болады, немесе өзінің жаралу процесінде коллоидты күйден өткен болып келеді» (А.И.Перельман, 1975). Сұйық дисперсті ортада, дисперсті (өзгеру - шашырау) фаза қатты және газ тәрізді күйде болуы мүмкін. Геохимиялық іздеулер үшін бірінші жағдай маңызды болып келеді. Мұнда дисперсті фаза металлдармен (Au, Ag, Pt, Bi, Sn және т.б.); металлдардың гидроксидтерімен (Fe(OH)3, Ti(OH)4, Al(OH)3 және т.б.); оксидтермен (MnO2, SiO2 т.б.); сульфидтермен (PbS, ZnS, Sb2S3, As2S3 және т.б.); сазды минералдармен (галлуазит, каолинит, монтмориллонит және т.б.) сипатталады.
Табиғатта коллоидтардың түзілуі екі негізгі әдіспен жүзеге асырылады:
1) дисперсиялық (кристаллдық заттың бұзылуы кезінде)
2) конденсациялық (молекулалық бөлікшелердің коллоидтық мөлшерге дейін қосылуы кезінде).
Дисперсиялылықтың өте жоғары дәрежесінде және дисперсиялық фазаның үлкен шамасы кезінде коллоидты жүйелер бос энергияның үлкен қорына ие болады. Оның өз еркімен төмендеуі сорбцияға ұшыратады.
6) Техногендік қосындылар - өзінің табиғи аналогі болмайды. Соңғы кезде көптеген әртүрлі аумақтарда, көбінесе, топырақтарда, донды түзілімдерде және суларда кездесіп кеңінен қолданыс табуда. Негізінен олар белсенді игерилетін аудандарда кездеседі, оларға бірінші кезекте, әртүрлі ауылшарушылық пайдаланатын жерлердің және ірі өнеркәсіптік комбинаттардың қасындағы бөлікшелерді жатқызуға болады. Элементтерді бұл анықтау түрі әртүрлі жасанды полимерлерді, пластмассаларды, металлдар қорытпаларын, пестицидтерді, гербицидтерді, жерүсті-активті заттарды және т.б. кіріктіреді. Бұған тағы да табиғатта кездесетін (және табиғи күйдегі элементтер), бірақ өздері табылған жерде нақты жағдайларда табиғи жолмен жаралмаған қосындыларды жатқызуға болады.
7) Магмалық балқымалар. Бұл түгелдей, өзгергішті, газбен қаныққан жүйелер. Бұлардағы элементтердің жағдайы осы уақытқа шейін проблемалық болып келеді. Магмалық балқымалардың Жер қыртысындағы элементтерді бөлу, қайта бөлу рөлі өте үлкен және сондықтан олардың элементтерінің жағдайы туралы гипотезалар қызығушылық туғызады. Ең бірінші магма туралы түсінік оксидтерден тұратын балқыма ретінде болған, бірақ 1935 жылы Ф.Ю. Левинсон-Лессинг магмада «болашақ минералдарға сәйкес кешендер» жатыр жазған. Н.В.Беловтың және Л.Н.Овчинниковтың жұмыстарында бұл жағдай тиянақты өңделген және толықтырылған. Қазір, магмада кешендердің екі негізгі түрі бар деп есептеледі:октаэдрлік топтар (оның ішінде [Mg O6] және [Ca O6] көп кездеседі) және тетраэдрлік топтар (оның ішінде [Si O4] және [Al O4] көп кездеседі). Бұлардан басқа қозғалмалы бос катиондар, еріген металлдардың атомдары, FeS және Fe2O4 типті қосындылар кездеседі деп есептеледі.
8) Шашырау күйі. Ең алғаш 1909 жыл оны В.И.Вернадский сипаттаған. Бұл Жер қыртысындағы элементтерді анықтаудың ерекше бір түрін көрсетеді және атомдардың кристаллдық торлардың бос кеңістігіндегі орналасуымен байланысты болып келеді. Атмосфераның төтенше жағдайда шашырауына жақсы себін тигізеді: басқа газдардың қосылыстарына түскен газ толығымен сол жерде еріп кетеді. Элементтердің шашырау жағдайындағы мөлшері 10-12 – 10-15 % дейін жетеді, ал шашыраудың шегі деп 1 см3 затта 1 атомның болуын айтады. Көптеген элементтерге бұл жағдай күнделікті болып келеді. Олардың қатарына йод, ксенон, радон жатады.
Элементтердің Жер қыртысындағы орналасу түрін қарастырғанда, табиғатта нейтралды атомдар емес, иондар жиі кездесетінін ұмытпау қажет. Геохимиялық процестерге қатысатын иондардың саны элементтердің санынан көп болады және саны 150-ге дейін жетеді. Ал әрбір ион, В.И.Вернадский бойынша миграция процесі кезінде «ерекше химиялық элемент» ретінде қарастырлуы керек.Элементтердің Жер қыртысында орын ауыстыруын олардың анықталған формацияларымен байланыстыра отырып, миграцияның негізгі 3 типін бөлуге болады.
Миграцияның 1 типі элементтерді анықтау түрінің олардың орын ауыстыруынсыз өзгеруін көрсетеді.Мысалы: элементтің минералды түрден сулы ерітінділерге ауысуы. Бұл типті сипаттау үшін элементтің бір түрден екінші түрге ауысу коэфициентін пайдалануға болады. Ең алғаш бұл коэфициенті Б.Б.Полынов биогенді түрлер үшін енгізген болатын: Кб = Р/П, бұл жерде К – биологиялық жұтылудың коэфициенті; Р - өсімдік белдеміндегі элементтің мөлшері; П – сол элементтің сол өсімдік өскен топырақтағы мөлшері.
Миграцияның екінші типі - элементтерің анықтау түрінің өзгеруінсіз орын ауыстыруы. Мұндай типтің мысалы ретінде минерал сынықтарының жерүсті суларында қозғалуы немесе ерітіндіде орналасқан элементтердің жерүсті және жерасты суларының қозғалуы кезінде орын ауыстыруы.
Миграцияның үшінші типі алғашқы екеуін қосады және элементтердің анықтау түрін өзгертуімен бірге орын ауыстыруынан тұрады. Мысалы: кенорындардағы минералдарды ерітетін элементтердің жерасты суларында қозғалуы; борпылдақ түзілімдердің тысы қалың болғанда минералды түрден биогенді түрге ауысуы.
Қарастырылған элементтерді анықтаудың түрлері тек қана салыстырмалы тұрақты жүйелер болып келеді. Жер қыртысындағы элементтердің көп бөлігі элементтердің миграциясын көрсететін жиі қозғалыс күйінде болады деп есептеуге болады.
Негізгі әдебиет: [1], 17-22 б., [2], 14-18 б.
Қосымша әдебиет: [9]
Бақылау сұрақтары:
1) «Элементтерді анықтау формасы» дегеніміз не?
2) Изоморфизм дегеніміз не?
3) улы ерітінділерде иондар қалай қозғалады?
4) Техногендер қосылыс дегеніміз не, олар қалай жаралады?
5) Элементтер миграциясының қандай формалары сізге белгілі?
6) Шашырау күйін сипаттаңыз.
3-ші дәрістің тақырыбы. Жер қыртысындағы элементтер миграциясының негізгі заңдылықтары.
Мазмұны: Табиғаттың барлық заттары және оларды құрайтын химиялық элементтердің атомдары әртүрлі геохимиялық және космохимиялық процестердің нәтижесінде тоқтамайтын және заңды қозғалыста, орын ауыстыруда, қайта топталуда және қайда бөліну күйінде болады.
«Химиялық элементтердің миграциясы» терминін 1923 жылы геохимияға А.Е.Ферсман енгізген. Бұл түсінікті ол, Жер қыртысындағы шашырауға және концентрацияға апаратын химиялық элементтердің орын ауыстыруын анықтайтын процестер кешені деп түсінді.
А.Е.Ферсман элементтердің миграция құбылысы, геохимиялық реакциялардың және геохимиялық кешендердің әр түрлілігін және көп түрлілігін анықтайтын табиғаттың маңызды құбылысы деп айтқан. Геохимиялық миграция түсінігін нақтылай отырып, ол кларк схемасында нақты бір геохимиялық жүйеде химиялық элементтердің таралуын орташа норма деп қараған, осының нетижесіндегі кез-келген ауытқулар миграция жолымен жүзеге асырылады деп айтқан.
Жер қыртысындағы кез-келген элементтің миграциялық жағдайының формасын А.Е.Ферсман бойынша келесідей схема бойынша көрсетуге болады:
Дисперстік жағдай (шашырау жағдайы) – орташа мөлшері (осы жүйенің кларкы) – жиналу (салыстырмалы концентрация) - өнеркәсіптік концентрация (кенорынның жаралуы).
Химиялық элементтердің миграциясы геохимиялық процестердің мазмұнын құрайда және кеңістікте атомдардың орын ауыстыруына, олардың сандық қатынастарының өзгеруіне әкеледі.
Химиялық элементтердің миграциясы біршама қозғалмалы жүйелерде сұйық күйінде (магмалық балқымалар және ерітінділер және т.б.), газ тәрізді фаза түрінде (атмосфера газдары, жанартаулық газдар, радиоактивті газдар және т.б.), сирек қатты минералды массаларда (таужыныстардағы атомдардың диффузиясы құбылысы және т.б.) жүзеге асады. Көптеген элементтердің миграциясы организмдердің және адамның тіршілігіне септігін тигізеді.
Жер жағдайындағы химиялық элементтердің миграциясы атомдық (инертті газдар, булар, сынап булары және т.б.), иондық (ерітінділер, балқымалар және коллоидты жүйелер), молекулярлық (ерітінділер, силикатты балқымалар) немесе коллоидтық, сонымен қатар дисперсті (таужыныстардың және минералдардың сынықтары) формада жүзеге асады.
Химиялық элементтер миграциялық қабілеттілігіне байланысты, яғни геохимиялық процестерде орын ауыстыруының интенсивтігімен өзара бөлінеді. Сонымен қатар, элементтердің миграциялық қабілеттілігі миграция ортасының термодинамикалық жағдайына байланысты өзгеріп отырады.
Белсенді мигранттардың қатарына жер қыртысының ауқымында орын алатын термодинамикалық жағдайлардың кең диапазонында оңай миграцияланатын химиялық элементтерді жатқызуға болады.
Осы элементтердің атомдары магмалық балқымаларда да, ерітінділерде де, сонымен қатар гипергенез белдемінің ерітінділерінде де оңай орын ауыстыра алады. Мысалы белсенді миграцияланатын элементтерге галогендер, сілтілі металлдар және т.б. жатады. Белсенді емес мигранттар (мысалы платина тобының элементтері) тек қана термодинамикалық жағдайлардың тар диапазонында (магмалық балқымалар) протокристаллизация сатысы - базальтты магманың оливинді таужыныстар жаралу кезіндегі дифференциациясы(перидотиттер, дуниттер, пироксениттер, габбро, нориттер ) кезінде миграцияланады. Жер қыртысының көптеген элементтері белсенді мигранттар болып келеді.
Элементтердің гипергендік миграцияға қабілеттілігі бойынша геохимиялық классификациясы
Әуедегі мигранттар
Активті Пассивті
(химиялық қосындылар тұғызады) (химиялық қосындылар тұғызбайды)
O, H, C, N, J Ar, He, Ne, Kr, Xe, Rn
Сулы мигранттар
Қатты қозғалмалылар
Ca, Na, Mg, Sr, Ra Cl, Br, F, B
Әлсіз қозғалмалылар
K, Ba, Rb, Li, Be, Cs, Ti Si, P, Ge, Sn, Sb, As
Тотығу жағдайдағы қышқыл суларда
жақсы миграцияланады
Zn, Cu, Ni, Pb, Cd
Тотығу жағдайдағы қышқыл және
сілтілі суларда жақсы миграцияланады
Hg, Ag
Тотығу жағдайындағы қозғалмалылар және әлсіз қозғалмалылар және қалпына келтіргіш жағдайда инертті
V, Mo, Se, U, Re
Гельді ортада қозғалмалылар және әлсіз қозғалмалылар және күкіртсутекті тотығу және қалпына келтіру ортада инертті
Fe, Mn, Co
Көп жағдайда аз қозғалатындар
Органикалық кешендермен әлсіз Органикалық кешендермен әлсіз
сулы миграция. Өте қышқыл ортада сулы миграция. Сілтілі ортада
біртіндеп миграцияланады. біртіндеп миграцияланады.
Al, Ti, Cr, Ce, Nd, Y, La, Ca, Th, Sc, Sm, Zn, Nb, Ta, W, Hf, Te
Cd, Dу, Tb, Er, Ho, Eu, Lu, Yb, In, Bi
Химиялық қосындыларды тұғызбайды , табиғи күй-жағдай тән
Os, Pd, Ru, Pt, Au, Rh, Zr
Жер қыртысының жергілікті бөлікшелерінің ауқымында химиялық элементтердің концентрациясы біршама қысқа қашықтықтағы миграциялардың сыртқы жағдайының өзгеруіне байланысты болады. Мұндай миграцияның интенсивтігі азаятын жергілікті бөлікшелерді А.И.Перельман геохимиялық бөгеттер (барьерлер) деп атауды ұсынды.
Элементтер миграциясының гипергенді белдеміндегі геохимиялық бөгеттер жақсы зерттелген. Олар өз кезегінде физика-химиялық, биохимиялық және механикалық болып бөлінеді.
Гипогенді (тереңдік) миграция кезінде термодинамикалық, тотықтыру-қалпына келтіру және сілтілі-қышқылды бөгеттер негізгі рөлді атқарады.
Мысалы, көптеген гидротермальды процестің теориясында кендердің жаралуы термодинамикалық бөгеттермен байланысты болып келеді. Д.И.Коржинский және оның мектебі метасоматиттердің және кендердің жаралуында сілтілі-қышқылды бөгеттерге көп көңіл бөледі. Сульфидті кендердің жаралуы күкіртсутекті (қалпына келтіру) бөгеттермен байланысты болады.
Элементтердің миграциясы кезінде гипогенді және гипергенді миграция белдемдерінде минералдардың тұрақтылығы (устойчивость) негізгі рөлді атқарады.
Гипергенез белдемінің әртүрлі жағдайындағы химиялық элементтердің миграциясының интенсивтігінің жалпылама сандық сипаттамасын алу үшін А.И.Перельман сулы миграцияның коэфициентін пайдалануды ұсынды.
Кх = Сх` . 100 / (mСх)
мұнда:
Сх` - судағы элементтердің мөлшері (мг/л)
Сх – таужыныстардағы элементтердің мөлшері (%)
m – судың минералды қалдығы (мг/л)
Кх мәндері болғанда әртүрлі жағдайда элементтер миграциясының қатарын орнатуға болады. Бір элементтің әртүрлі жағдайда миграция интенсивтігінің әртүрлі болуы миграцияның контрастылығы деп аталатын коэфициентпен сипатталады, КК әртүрлі жағдайдағы элементтің сулы миграциялы коэфициентерінің қатынасынан тұрады.
Миграцияның контрастылық коэфициенті (КК) геохимиялық бөгеттерде, яғни әртүрлі миграция шарттары бар екі ортаның шекарасында өтетін процестерді сандық түрде сипаттауға мүмкіндік береді.
Элементтердің миграциялық қабілеттілігі түсінігін олардың нақты минерал жаралу процесі көлемінде геохимиялық қозғалысын бағалауға қолдануға болады. Яғни элементтердің миграциясын тек сандық жағынан қарамау керек (активті немесе активті емес), сонымен қатар сандық, яғни қанша элемент бірлік уақыт аралығында қозғалмалы күйге ауысады. Және осы сан тек қана элементтің ішкі қасиеттеріне байланысты болмайды, сол геохимиялық жүйеде болатын сол элементтің атомының жалпы санына байланысты болады.
Мысалы, Na және Li миграциялық қабілеттілігі бірдей болса, басқа да бірдей жағдайларда (мысалы таужыныстарынан табиғи суға) Na Li-ге қарағанда қозғалмалы күйге өте көп өтеді, себебі Na мөлшері таужыныстарында Li-ге қарағанда көп болып келеді.
Егер Х (Cu, Pb, Ba) мына элементтің табиғи жүйеде атомдарының жалпы санын Вх деп белгілесек, ∆t уақыт аралығында қозғалмалы күйге өткен атомдардың санын ∆Вх деп белгілеуге болады. Онда атомдардың қозғалмалы күйге өткен салыстырмалы бөлігі ∆Вх/ Вх құрайды, ал уақыт бірлігінде мынаған тең:
∆Вх/ Вх . 1/∆t – бұл шама миграциялық қабілеттілікті сипаттайды,
Рх символымен белгіленеді.
Миграциялық қабілеттіліктің теңдеуі пайда болады:
Рх = 1/ Вх . ∆Вх/∆t ,
ал шексіздік аз уақыт ішінде дифференциалдық түрде:
Рх = 1/ Вх . dВх/dt – миграциялық қабілеттіліктің теңдеуі.
Бұл тек қана гипергенді ортада өтетін миграция процесіне қолданылады, себебі тереңді гипогенді жағдайда В –ның t- дан байланысы анықталмаған.
Дүниежүзілік кеңістікте химиялық элементтердің миграция процесі және элементтердің активті немесе пассивті орын ауыстыру процесі, бұл атом құрылысының, оның ядросы мен электронды қабығының заңдылығының терең білінулері және дүниежүзілік кеңістікте нақты бір термодинамикалық жағдайда осы заңдардың атом тарихына әсер ету көріністері.
Химиялық элементтердің миграциясы көптеген факторлар нәтижесінде туындайды, бірақ оларды екі топқа бөлуге болады: 1) ішкі – химиялық элементтердің және оның қосындыларының атомдарының қасиеттерімен байланысты, 2) сыртқы – миграция жағдайының термодинамикалық шарттары.
Осы факторлардың әрбір жеке тобы геохимиялық миграцияның тек қана кейбір маңызды түрлерін түсіндіре алады. Бұл жағдай құбылысты толық түсінуге мүмкіндік бермейді. Толық түсіну үшін барлық факторлар тобын олардың қарама-қайшы әрекетінің (в их противоречивом взаимодействии) жағдайын қарастыру қажет.
Ішкі және сыртқы факторлардың қарама-қайшы әрекеттері геохимиялық процестің негізгі себебі элементтердің миграциясы ретінде В.И.Вернадскийдің, А.Е.Ферсманның, А.Н.Заварицкийдің эвалюциялық геохимиялық концепцияларына кіреді. Олар бұдан геохимиялық жүйелер эвалюциясының заңдарын диалектикалық негізін бөліп алған.
Сонымен, геохимиялық миграция процесінің себебі –бұл жер қыртысында жүзеге асатын миграцияның ішкі және сыртқы – макропланетарлық және космостық факторлар арасындағы қарама-қайшылық.
Негізгі әдебиет: [1] 22-23 б.; 36-43 б., [2] 18-19 б., [4] 34-40 б.
Қосымша әдебиет: [15]
Бақылау сұрақтары:
1) Химиялық элементтер миграциясының қандай түрлері және типтері болады?
2) Жер жағдайында химиялық элементтер қандай түрде миграцияланады?
3) Иондардың еркін миграциясы кезіндегі реттілікпен түзілу қатарын көрсетіңіз
4) «Ұшпалылық» дегеніміз не және ол түзілу қатарындағы элементтер жағдайына қалай әсер етеді?
5) Геохимиялық барьерлердің қандай типтері және класстары бар?
6) Барьердің контрастылығын қалай анықтауға болады?
7) Барьердегі элементтің концентрациясын қалай анықтауға болады?
4-ші дәрістің тақырыбы. Жер қыртысындағы химиялық элементтердің геохимиялық миграциясының ішкі факторлары.
Мазмұны: Миграцияның негізгі ішкі факторлары ретінде атомның келесі қасиеттерін бөлуге болады: 1) гравитациялық; 2) байланыс қасиеті; 3) химиялық; 4) радиоактивті.
1) Атомдардың гравитациялық қасиеті оның массасының мөлшерімен байланысты және Жердегі және космостағы элементтердің дифференциациясы процесі кезінде өте маңызды болып келеді. Атомдардың гравитациялық қасиеттері ең үлкен рольге Жер жаралуының ерте сатыларында ие болған.
Барлық элементтердің миграция процесі біріншіден, бүкіл әлемдік тартылыс күшінің әсерімен жүзеге асады, сонымен қатар космостық денелердің ортасында ауыр атомдар жинақталады, бұзылған бөліктерінде жеңіл атомдар жинақталады. Атодардың гравитациялық қасиетіне меншікті салмақ және атомдық көлемдер жатады.
Бұрыннан белгілі, магмалық кристаллизацияның ерте минералдары дала шпатымен салыстырғанда үлкен меншікті салмақты хромит, оливин, пироксендер, гравитациялық күштің әсерінен магмалық ошақтың түбіне жиналып, таужыныстарды құрайды. Сонымен қатар, жер қыртысының континенттері өзінің астында жатқан таужыныстардан қарағанда біршама жеңіл таужыныстардан құралғаны бізге мәлім. Жердің орталық бөліктерінде ең көп тараған элементтердің ішінен темір мен никель бар деп сесептеледі.
Бірақ, таужыныстарда таралған бірқатар элементтер ең ауыр элементтер және оның қосындылары гравитациялық қасиеттерге бағынбайтынын көрсетеді. Мысалы, мынандай элементтер Nb, Ta, Zn, Hf, W, Mo және әсіресе Th, U (атомдық нөмерлері 41, 73, 30, 72, 74, 42, 90, 92) біршама қышқыл магмалармен және постмагмалық, яғни салыстырмалы жеңіл таужыныстармен байланыста болады.
Сонымен, элементтердің бөлінуі көз-қарасынан қарағанда элементтер арасында Жер шары қабықтарының құрылуында негізгі рольді атқаратын гравитациялық қасиет Жер дамуының ерте сатыларында пайда болады. Аз таралатын элементтердің бөлінуінде гравитациялық қасиет маңызды рөлді атқармайды. Бұның бәрі магмалық процестерге жатады.
Гипергенді таужыныстарда гравитациялық қасиет маңызды рөлді атқарады. Ауыр және механикалық төзімді қосындылар (алтын, алмас, касситерит, циркон, топаз, вольфрамит, рутил, ильменит және т.б.)тұғызатын көптеген элементтер осы қосындылардың (шашырандылар) гравитациялық қасиетімен байланысты концентрация түзуге бейім болып келеді.
Элементтердің геохимиялық типімен байланысты атомдық (және молекулалық) көлемдер В.М.Гольдшмидт бойынша, осы типтердің космостық денелерде шетінен ортасына қарай кеңістікті таралуында негізгі рөлді атқаратын элементтер миграциясының жолын анықтайды (атмофилдер – H, N, C, O, Cl, Br, J, He, Ne, Ar, Kr, Xe, литофилдер – Si, Ti, Zt, Hf, Th, F, B, Al, Sa, K, Na, Rb, Li, Be, Mg, Sr, Ba, Cr, халькофилдер – S, Sc, Te, As, Sb, Bi, Ca, In, Tl, Pb, Zn, Cu, Cd, Hg, Ag, Ni, Co, сидерофилдер – Ke, Ni, Co, P, C, Os, Ir, Pt, Pd, Au, Ge, Sn. Mo, Ta).
2) Байланыс қасиеттері (термикалық қасиеттер) - элементтің немесе қосындының атомдарды , иондарды немесе молекулаларды ажыратуға бағытталған күштерге қарсы тұруымен сипатталады. Бұл күштерге механикалық және жылулық күштер жатады (механикалық – бұл қашықтау (отрыв), жылулық – атомдарды қозғалмалы күйге алып келеді).
Атомдардың немесе қосындылардың бір агрегатты күйден екінші агрегатты күйге ауысуымен байланысты ажыратушы күштердің әсерінен байланыс қасиеттері қайнау температурасымен (ұшпалылықпен) және химиялық элементтердің және қосындылардың балқуымен анықталады.
Қайнау температурасымен байланысты элементтердің ұшпалылығы, осыдан олардың жоғары миграциялық қозғалысы мына реттілік бойынша төмендейді: ұшпалы газдар (He, Ar, N, O), қозғалмалы металлоидтар (F, Cl, Br, J, S), металлдар (Hg), сілтілі және сілтіліжерлі металлдар (Li, Rb, Cs, K, Na, Ca, Mg), жәй металлдар (Fe, Ni, Co, Cu) және қиын ұшпалы элементтер (Pt тобы, C, W, Na, Mo, Hf, B, Zr).
Жер қыртысында өтетін миграция процесі кезінде ұшпалылық қайна температурасы 600С аспайтын элементтердің геохимиялық тарихында маңызды рөлді атқарады. Қайнау температурасы 4000С төмен болатын элементтерде ұшпалылық геохимиялық процестердегі миграцияның негізгі факторы болып келеді.
Ұшпалылыққа ұқсас жер қыртысындағы магмалық балқымалар жағдайындағы химиялық элементтердің миграциясы үшін қосындылардың (қышқылдар, силикаттар және галоидты қосындылар ) балқу температурасы негізгі рөлді атқарады.
Қыртысішті магмалық температуралардың интервалы 700-13000С. Осы температуралық интервал жер қыртысы жағдайындағы элементтердің және оның қосындыларының термикалық қасиеттері туындайтын облыс ретінде қарастырылады.
3) Химиялық қасиеттері. Табиғатта өте жоғары температура кезінде барлық қосындылар дисоциацияланған (дисоциация – атомдардың тарауы) күйде болады және осы жағдайда атомдар мен иондардың табиғатымен байланысты факторлар пайда болады. Ортаның температурасы төмендегенде миграция процесі кезінде молекулалар басты маңызға ие болады. Кейбір элементтердің миграция мінезі мен дәрежесі осы жағдайдағы қосындылардың миграциялық қасиетіне байланысты болады.
Элементтердің және олардың қосындыларының химиялық қасиеттері жер қыртысындағы таужыныстардың магмадан кейінгі эволюция сатысындағы элементтердің геохимиялық миграциясының басты факторы болып келеді.
Миграция процесіндегі элементтердің химиялық қасиеттерінің рөлі келесі негізгі қағидалармен сипатталады:
1.Миграция дәрежесі және жолы нақты жағдайдағы элементтердің негізгі қосындыларының тұрақтылығына байланысты болады. Яғни, кез-келген термодинамикалық және химиялық жайдайдағы элементтердің миграциясы оның негізгі қосындыларының тұрақтылығымен анықталады:
а) мысалы, магманың жоғары температурасы кезінде миграцияға қабілеттілігі сол элементтен туындайтын сол жағдайдағы қатты фазаға түсетін балқу және қайнаудың ең жоғарғы нүктесі бар қиын балқитын қосындылардың жаралу мүмкіндігіне байланысты болады;
б) сулы ерітінділер жағдайында көптеген элементтер қатарының миграциялық қабілеттілігінің төмендеуі олардың қосындыларының қиын ерігіштігімен сипатталады. Мысалы, қиын еритін фосфорқышқылды және күкірт қышқылды тұздардың жаралуымен;
в) гипергенез жағдайында мықты (стойкий) қосындыларға тотығу процесіне ұшырамайтындар жатады.
2. Элементтер қосындыларының жаралуы бірнеше мүмкіндік бар кезде бос энергиялармен анықталады. Т
Бос энергия арқылы табиғи парагенезистегі сульфидті минералдардың бөліну реттілігінің қарапайым түрі: Fe(FeS2), Cu, Zn (Mn), Pb, Ag, Cd, Te, Hg.
Элементтердің ковалентті байланысты тұғызу қабілеттілігі кешенді қосындылар (ZnS, Fe2O, FeO, CaO, CaMgCO3) құрамында сулы ерітінділерде осы элементтердің миграциялану мүмкіндігін анықтайтын басты фактор болып келеді.
А.Е.Ферсман миграция процесі үшін химиялық элементтер атомдарының ионизация потенциалының рөлін келесідей түсіндірді:
а) жақын ионизация потенциалы бар атомдар миграцияның сол қасиеттеріне ие болады (R, Na, Li, Rb, Si, Ge);
б) бірдей типті торлардан тұратын атомдар мен иондар миграциялық қасиеті бойынша бірдей болады.
3. Химиялық элементтер атомдары мен иондарының радиустарының бірдей болуы миграция жолының бірдей болуын сипаттайды. Өте үлкен немесе өте кіші радиусты атомдар мен иондар миграцияның және қайта бөлінудің жоғары қабілеттілігімен сипатталады. Мысалы, ион радиусы өте кіші және өте үлкен мөлшерде болатын элементтер жиналатын гранитті пегматиттер.
4) Радиактивті қасиеттері. Атомдардың радиоактивті қасиеті миграция процесі радиоактивті элементтердің таралуы кезіндегі және жаңа ядролардың басқа физика-химиялық қасиетттермен жаралуы кезінде сол элементтер санының үнемі өзгеруімен сипатталады.
Негізгі әдебиет: [1], 23-29 б. [2] 19-25 б.
Қосымша әдебиет: [9]
Бақылау сұрақтары:
1) Элементтер миграциясының негізгі ішкі факторларын атаңыз.
2) Элементтердің геохимиялық миграциясына атомдардың гравитациялық қасиеттерінің әсері қандай?
3) Элементтердің геохимиялық миграциясы процесінде химиялық қасиеттердің рөлі қандай?
4) Әртүрлі қосындылардың жаралуы миграцияға қалай әсер етеді?
5-ші дәрістің тақырыбы. Жер қыртысындағы химиялық элементтердің геохимиялық миграциясының сыртқы факторлары.
Мазмұны: Геохимиялық миграцияның сыртқы факторлары атомды қоршаған ортамен байланысты болады. Осы орталардың негізгілерін қарастырайық.
1. Температура. Температураның көтерілуімен балқымаларда және ерітінділерде орналасқан элементтердің миграциялық қабілеті артады, химиялық реакцияның жылдамдығы артады және изоморфты ауысулардағы элементтердің өзара ерігіштігі артады.
Геохимиялық процестің жүруінің негізгі шартына температураның төмендеуі жатады. Температура заттың қозғалмалылығын және агрегатты күйін, химиялық реакцияның жылдамдығын, балқымалар мен ерітінділердегі кристаллизацияның жылдамдығын және реттілігін, элементтердің кристалдық температуралары бойынша дифференциациясын анықтайды.
В.С.Соболев табиғи процестерде силикаттардың жаралуы мен бұзылуында температураның рөлі қандай екенін былай көрсеткен:
а) температураның төмендеуі судың жұтылуымен реакцияға септігін тигізеді, яғни құрамында су көп мөлшерде болатын силикаттардың және парагенезистердің жаралуына алып келеді;
б) температураның төмендеуімен жәй және қос силикаттардың бұзылуына алып келетін CO2 және өте қышқыл ангидридтердің активтілігі артады;
в) температураның төмендеуі қатты фазадағы өзара ерігіштікті төмендетеді және нақты бір катиондардың таза химиялық қосындыларына (ZnS, CuS) жақындайтын изоморфты қосылыстардың таралуына және минералдардың жаралуына алып келеді;
г) температураның төмендеуі катиондар координациясының ең үлкен саны бар қосындылардың жаралуына септігін тигізеді;
д) температураның төмендуімен схемада көрсетілгендей кремний оттекті тетраэдрлі ассоциациялардың өте күрделілеріне тенденциясы байқалады:
аралды – баулылар (цепочечные) – ленталы – қабатты
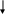
[SiO4]-4 [Si2 O6]-4 [Si3 O9]-9 [Si5 O15]-10 [Si6 O18]-12 [Si4 O10] [Si3 O7]
эпидот тальк, слюда
– каркасты
[AlSiO4], [AlSi2 O6], [AlSi3 O8]
калий дала шпаты, цеолиттер, лейцит, содалит
Калий дала шпаты K [AlSi3 O8] және лейцит K [AlSi3 O8] кристаллдық тордағы судың рөлінің артуымен байланысты болады.
Жер қыртысында магмалық балқымаларда температура 1600-15000 1200-13000 дейін болады және жер қыртысының терең бөліктерінде -850С дейін литосфера бетінде (Антарктидада).
Сонымен, жер қыртысындағы элементтер миграциясының геохимиялық процесі температураның мынандай диапазонында 1600-15000С өтеді. Геохимиялық процестердің нақты бір температуралары минералогиялық құрамы әртүрлі геологиялық денелердің жаралуына септігін тигізеді. Сол үшін геохимиялық процестердің температуралары генетикалық классификациялардың, минералогиялық процестердің және де пайдалы қазба кенорындарының басты факторы болып келеді.
Бірақ, табиғи процестердің температура туралы ой тұжырымдау өте қиын, себебі бұл процестер бұрын (геологиялық бұрын) болған, ал қазір біз осы процестердің тек қана нәтижелерін зерттей аламыз.
Геохимиялық процестердің температурасын геологиялық және минералогиялық термометрлер арқылы анықтайды, бұл сондай минералдар немесе олардың комбинациялары, немесе өздерінің жаралу, өзгеру температуралары белгілі болатын минералдардың нақты бір қасиеттері. Осылардың көмегі арқылы сол процестің температурасын нақты анықтауға болады.
Бірақ, көптеген минералдардың жаралу температуралары әр түрлі болады. Бұл жағдай бірнеше факторлардың (қысым, қоспалар, ерітінділер мен балқымалардың құрамы) әсеріне байланысты болады. Сол үшін бұларды минералогиялық термометрлер ретінде пайдалануға болмайды.
Мұндай жағдайда тек қана типоморфты минералдарды пайдалануға болады, себебі олар геохимиялық процестерде нақты бір орынға ие болады. Олар геохимиялық процестердің шарттарын (температура) және уақытын анықтайды, сол себепті оларды зерттеу геохимиялық процестерді түсіну үшін өте маңызды болып келеді.
Минералогиялық термометр ретінде қолданылатын типоморфты минералдардан киноварьды HgS (гидротермалды процестің соңғы сатысында пайда болатын минерал – бөліну температурасы 1400С төмен) мысалы ретінде алуға болады.
Өте көп модификацися бар кварцта қолданылуы мүмкін:
1)
Пегматитті процестегі гранитті магманың
кварцы – 800-7000
– ашық-сұр немесе мөлдір түйірлі немесе
кристалшық түрінде (![]() - кварц).
- кварц).
2) Сұрғылттау морионға дейінгі кварц – бағаналы кристаллдар (альфа-кварц) Т-700-5500.
3) Ақ немесе сұр кварц. Жиі морионның кристаллдарын өседі – Т-550-5000.
4) Кварц – дұрыс өспеген үзілмелі, Т-500-4000С.
5) Кварц – сүтті кварц, сирек тау хрусталінің кристаллдары, Т-400-3000С.
6) Кварц – ұсақ кристаллды жаралулар, кейде халцедонға немесе аметистке ауысатын, қысқа бағаналы кристалшықтар – Т-300-2000С.
7) Кварц – щетка тәрізді тау хрусталінің жаңа жаралулары – Т-2000С және одан төмен.
Бұл кварцтың типоморфты қасиеттерінің схемасы тек қана пегматитті процестерге емес, сонымен қатар гидротермалды жаралуларға тән.
Кальцит – температура бөлінуіне байланысты кристаллдар түрі өзгеруінің мынандай жолына ие болады:
350-3000С – пластинаклы (0001);
300-2000С – негізгі ромбоэдр (1011);
150-1000С – жайпақ ромбоэдр (0112);
1000С және төмен - өткір ромбоэдрлар (4041).
Геохимиялық процестердің температураларын анықтау үшін біршама объективті және дәл мәліметттерді минералдардағы газ-сұйықты қосуларды минералтермомертлік зерттеулер береді.
Бұл әдіс әр алуан және постмагмалық және гипергендік процестердегі минералдардың жаралу температураларын анықтауға мүмкіндік береді. Сонымен қатар, кристаллизация кезіндегі қысымды бағалау үшін қолдануға болады.
2. Қысым. Қысым химиялық элементердің миграциясына үлкен әсер етеді, мысалы тектоникалық жарылымдардар пайда болған кезде магмалық ошаққа әсер етеді. Осымен байланысты ұшпалы компоненттердің бөлініп шығуы пневматолит-гидротермальды процестердің басталуына және магмалық ошақтан химиялық элементтердің қоршаған ортаға интенсивті миграциясын қамтамасыз етеді.
Қысымның тербелісі температураның тербелісімен тығыс байланысты болады. Қысым элементтердің балқу және қайнау температурасына әсер етеді. Мысалы, қысым 1 атм. көтерілсе, темірдің балқу температурасы 0,0110С –ге көтеріледі.
Температура және қысымның біршама тербелісі және олардың арақатынасы элементтің физикалық күйінің өзгеруін анықтайды, сонымен қатар, элементтердің өзара миграциясы: балқыту, еріту, төмендеу және т.б. (элементтер миграциясының маңызды шарты болып келеді) жүзеге асады.
Гипергенді процестерде қысымның өзгеруімен осы процестің жүруіне үлкен әсер ететін қоршаған ортадағы оттегінің, көмір қышқылының және т.б. газдардың мөлшерінің өзгеруі байланысты.
Миграция үшін өте маңызды болатыны стресс - жанама (бүйірлік ) қысым (негізінен минерал жаралу процестерінде). Мысалы, стресс минералдарға мусковит, хлорит, эпидот, цоизит, тальк, дистен, ставролит жатады.
Стресс – минералдардың өздерінің қайта кристаллдануына септігін тигізетін, заңды-кеңістікті бағытын тудыруын шақыратын метоморфизм факторларының бірі.
Жер қыртысындағы геохимиялық поцестер үшін қысымның төменгі шегі тропо-(атмосфераның төменгі қабығы) және литосфераның шекарасында 1атм. деп қабылданады.
Егер геохимиялық процестерді біздің бақылауымыз жететін 30 км тереңдікте өтеді десек, онда қысымның жоғарғы шегі 7500-10000 атм. болады. Тектоникалық процестер кезінде туындайтын қысымның шамасы туралы айту өте қиын. Өйткені, физиктердің есебі бойынша, алмас 60000 атм. жоғары қысым кезінде көміртегінің мықты модификациясы болып келеді, яғни жоғарғы шегін де осындай шамаға үлкейтуге болады. Бұндай шаманы жер қыртысының геохимиялық процестері кезінде жетеді, бірақ жер қыртысында алмастың кездеуі сирек сияқты өте сирек кездеседі.
3. Ортаның химиялық құрамы миграцияның ерекшеліктерін, жер қыртысы жағдайындағы химиялық элементтердің табиғи ерітінділерде және балқымаларда концентрациясын және шашырауын анықтайтын фактор болып келеді. Сонымен қатар миграция процесі кезіндегі элементердің тәртібі физикалық химияның заңдарымен реттеліп отырады, бұларды білмей тіпті қарапайым геохимиялық құбылыстарды зерттеу мүмкін емес.
Геохимиялық жүйеде миграция ерекшеліктерін анықтайтын өте маңызды фактор осы элементтер санының басқа да элементтер санының қатынасына тең болатын заттардың концентрациясы болады. Көбінесе концентрация еріген заттағы молекулалар санымен сипатталады, 1 литр ерітіндіде, немесе молекулалар санында еріген 1000 г еріткіш болады.
Сутекті иондардың концентрациясы (ерітінділердің қышқылдығы немесе сілтілілігі – сутекті потенциал) рН – катиондар мен аниондардың меншікті белсенділігін, элементтер арасындағы химиялық реакциялардың бағытын және минералдардың табиғи қосындыларының жаралуын сипаттайды.
Суда (Н2О) молекулалар мен бірге судың дисоциацияланғаниондары (Н+1) және (ОН)1-1 кездеседі, олардың концентрациялары Сн = Сон = 10-7.
Сулы ерітіндінің қышқылдық дәрежесін анықтау үшін сутекті иондар концентрациясын минус таңбасымен алынған және рН шамасымен белгіленетін концентрацияның логарифмі түрінде көрсеткен ыңғайлы болады.
pH
= - loqCH
=
-loq(10-7)
= 7![]()
pH = 7 - нейтралды ерітінділер;
pH
от 7 до 1 – қышқыл ерітінділер (![]() төмендеуімен қышқылдық артады);
төмендеуімен қышқылдық артады);
pH от 7 до 14 – сілтілі ерітінделер ( неғұрлым көп болса, соғұрлым ерітінді сілтілеу болады);
pH – шөгінді жаралу ортаның сілтілі-қышқылды тепе-теңдігін көрсетеді:
а) ерітінділердің қышқылдығының артуы орын басу реакцияларына қолайлы болады, бұл процес кезінде күшті негіздердің әлсіз негіздерді қысым көрсетіп шығаруы болады, (мысалы КДШ альбиттену кезінде калийдің (39), натриймен (22) қысым көрсетіп шығарылуы, кварцтану – біршама күшті кремнийлі (28) негізбен әлсіздерді қысым көрсетіп шығару, сонымен қатар және Аl (26).
б) өз кезегінде ерітінділердің сілтілігінің көбеюі біршама күшті негіздердің әлсіздерді қысым көрсетіп шығару реакциясына қолайлы жағдай жасайды. Мысалы, калийлі метасоматоз, микроклинизация, ортоклазизация, сонымен қатар кварцтың дала шпатымен және слюдамен орын басуының барлық сәттері.
Гипергенді, сонымен қатар топырақты процестердегі химиялық элементтердің миграциясы үшін рН үлкен мәнге ие болып келеді. Көптеген гипергенді және шөгінді минералдардың жаралуы рН нақты мөлшерімен байланысты.
Гипергенді процестердегі элементтердің миграциялық қабілеттілігінің маңызды сипаттамасы рН мөлшері болып келеді, осыдан ерітіндіден сол элементтің гидрототықтардың түсуі (құлауы) басталады. Бұл мөлшер сол элемент атомының қасиетіне (ион радиусы, валенттілік, поляризация, энергетикалық қасиеттері) және сыртқы ортаның жағдайына (ерітінді, концентрация температурасы, басқа иондардың құрамы және т.б.) байланысты болады.
А.И.Перельман араласқан тұздардың ерітінділерінен металдар гидрототықтардың құлауы басталуының рН көрсеткен (однонормальных):
pH pH pH
10.5 Mq (OH)2 6 Pb (OH)2 3.5 Ga (OH)2
9 Aq (OH) 5.7 Be (OH)2 3.0 Sn (OH)2
8 La (OH)3 5.5 Fe (OH)2 2.4-4.5 Fe (OH)3
7-8 Hq (OH) 5.4 Cu (OH)2 2 Sn (OH)4
8.5-8.8 Mn (OH)2 5.2 Zn (OH)2 1.4-1.6 Ti (OH)4
6.8 Co (OH)2 2.5 Si 2 Zr (OH)4
6.7 Ni (OH)2 4.2 UO2 (OH)4
4.1 Al (OH)2
Гидрототықтар құлауының рН мәліметтері қандай жағдайда элементтер ерітіндіге өтеді және шашырайтынын, ал қандай жағдайда, керісінше, ертінділерден түседі және концентрацияланатынын алдын ала болжауға мүмкіндік береді. Бұл жағдай жер қыртысындағы химиялық элементтердің миграциясы туралы бірқатар геохимиялық мәселелерді шешуге мүмкіндік береді. Мысалы, кремний (Si) рН= 2,5 болғанда гидраттарды түзеді. Сол үшін SiO2 қышқыл ортада оңай жинақталады және сілтілі ерітінділерде жақсы миграцияланады.
Ек валентті Fe+2 Fe+3 қарағанда ерітінділерде қышқылы аз суларда орналаса алады. Бұл жағдай Fe+2 тундар мен тайганың болоталарында интенсивті және дала мен шөлдалада (әлсіз сілтілі сулар) әлсіз миграциясын түсіндіреді, ал сонымен қатар Fe+3 шынайы ерітінділердегі миграциясының шектеулі мүмкіндігін түсіндіреді.
рНт (3-5) болғанда күшті негіздердің шығуымен қатар алюмосиликаттардың ыдырауын күтуге болады.
рН эксперименталды түрде анықталады. Табиғи геохимиялық процестерде ортаның қышқылдылығы мен сілтілігін ортаның минерал-индикаторладың көмегімен анықтауға болады.
Тотығу-қалпына келтіру шарттары (Еh оттекті потенциал), сутекті иондардың концентрациясы сияқты (рН сутекті потенциал) геохимиялық процестердегі элементтер миграциясының химиялық реакцияларының бағытын анықтайды.
Тотығу-қалпына келтірудің химиялық реакциялары химиялық элементтердің өзара қатынасты атомдарының валенттілігінің өзгеруіне алып келеді және электрондардың атомдарды жоғалтуымен, олар өз кезегінде тотығады, және қалпына қайта келетін атомдармен иемденуімен қорытындыланады. Тотығатын заттар, электрондар беретін атомдар, қалпына келтіргіштер деп аталады, ал қалпына келетін зат – тотықтырғыш деп аталады.
Негізгі әдебиет: [1], 23-29 б. [2] 25-34, [3]
Бақылау сұрақтары:
1) Элементтер миграциясына температура және қысымның әсері қандай?
2) Элементтер миграциясына ерітінділердің электролитикалық диссоциациясының дәрежесі қалай әсер етеді?
3) Элементтер миграциясына ортаның сілтілігі қалай әсер етеді?
4) Элементтердің миграциялық қабілеттілігіне қышқылдандыру – қайта қалпына келтіру жағдайының әсері қандай?
5) Элементтер миграциясына организмдердің тіршлігінің әсері қандай?
6-шы дәрістің тақырыбы. Геохимиялық аномалиялар туралы жалпы түсініктер.
Мазмұны: Геохимиялық аномалия – бұл не нақты таужыныстар, өсімдіктер, сулар типіне тән, не геохимиялық ландшафтқа, не нақты ауданға тән геохимиялық нормадан ауытқу. Бұл фон мен салыстырғанда элементтер мөлшерінің көтерілуі немесе төмендеуі. Геохимиялық аномалиялар өлшемі бойынша бөлінеді: өлшемі кенді денеге немесе кенорындарға сай жергілікті (локальді); концентрация өрістеріне немесе шашырау өрістеріне сай келетін аймақтық.
Аймақтық аномалиялар ұсақ масштабты геохимиялық зерттеулер кезінде, ал жергілікті орта және ірі масштабты геохимиялық зерттеулер кезінде анықталады.
Геохимиялық аномалияларды кенді денелерге және пайдалы қазбалар кенорындарына қатысты перспективті, перспективті емес және жалған деп бөлуге болады.
Перспективті аномалиялар пайдалы қазбалармен байланысты, сол үшін олар ең бірінші кенді денелерді және пайдалы қазбалар кенорындарын іздеу кезінде зерттелу керек.
Перспективті емес аномалиялар – бұл таужыныстардағы элементтердің жоғары, бірақ өнеркәсіптік емес концентрацияларымен байланысты геохимиялық аномалиялар. Жұмыстардың бірінші этаптарында перспективті аномалияларды перспективті емес аномалиялардан ажырату өте қиын. Бұл үшін сол бөлікшенің геологиялық және геохимиялық ерекшеліктерін ескері қажет.
Жалған аномалиялар жоғарғылардан, сол типтегі таужыныстардағы элементтердің жоғары мөлшерімен байланысты еместігі мен өзгешеленеді. Жалған аномалиялардың пайда болуы сынамалардың бір топқа дұрыс жинақталмауы мен немесе территоряның ландшафты-геохимиялық аудандастыруының дұрыс болмауы мен байланысты болады немесе іздеу жұмыстарын жүргізгенде өсімдіктердің биогеохимиялық ерекшеліктері ескерілмеген.
Элементтер мөлшерінің таралуы мен байланысты аномалиялар дұрыс (положительный) немесе жағымсыз (отрицательный) болуы мүмкін. Біріншілері жоғары концентрациясымен, екіншілері - элемент-индикаторлардың бірден төмендеуімен айрықшаланады. Аномалияларды бөлу үшін минималды аномалды мөлшерін (Сан) немесе нормалды фондық мөлшеріне (Сф) салыстырмалы тербелуінің жоғарғы және төменгі шегін анықтау керек.
Сан = Сф + 3S ;
мұнда: Сан – элементтің аномалды мөлшері;
Сф – элементтің фондық мөлшері;
S – орта квадраттық ауытқу.
Барлық бұрын қарастырылған геохимиялық аномалиялар табиғи түрге жатады, яғни адамның кедергісісіз жаралған аномалиялар.
Ноосфераның жаралуы кезінде химиялық элементтердің гипергенді миграциясы көбінесе антропогендік іс-әрекетімен анықталатын болды. Нәтижесінде бірқатар геохимиялық барьерлерде осы іс-әрекеттің нәтижесінде туындаған аномалиялар құрылды. Бұндай аномалиялар техногендік деп аталды. Қазіргі кезде техногенді процестер үлкен масштабтарға жетті, табиғи және техногенді барьерлерде олардың әсерімен өнеркәсіптік концентрациядағы нақты элементтердің жиналулары болуы мүмкін.
В.А.Алесеенко (2000 ж.) теногендік барьерлерді «әлеуметтік геохимиялық барьерлер» деп тауды ұсынды. Бұл термин мен өнеркәсіптік және тұрмыстық қалдықтардың қоймалану белдемдері біріктіріледі. Миграциондық ағымға түсіпқалған осы заттардың техногендік қайнар көздерін ластандырғыштар деп атайды. Бұларға нақты өнеркәсіптер, тау қазылымдары, нақты ауыл шаруашылық ландшафтар жатады. Техногендік аномалиялардың өлшемдері кең ауқымда (бірнеше км-ден 100 км-ге дейін) таралады. Техногенді аномалияларда элемнттер минералды, биогенді немесе изоморфты формаларда, ерітінділер және газды қосылыстар түрінде кездеседі.
Аномалияларды табиғи және техногенді түрлерге бөлудің негізгі критерияларына – аномалиялардың морфологиясы, олардың нақты таужыныстарға және геологиялық құрылымдарға туралануы, сонымен қатар осы аномалияларды туғызатын химиялық элементтердің ассоциациялары жатады.
В.И.Вернадскийдің ережесінен шығатын, кез-келген табиғи нысанда барлық химиялық элементтер кездеседі, көп жағдайда жер қыртысының кейбір бөлікшелері түпкі таужыныстарда, топырақтарда, суларда, атмосферада бірқатар элементтер бірге жинақталады. Осы бірге жинақталуды «элементтер ассоциациясы» деп атайды. Мұндай бірге жинақталуларды ішкі және сыртқы факторлар мен сипатталған миграция шарттарының ортақтығымен түсіндіруге болады. Егер нақты бір элементтердің концентрациясына ішкі факторлар шешуші әсер етсе, жоғары мөлшерде орналасқан элементтер ассоциациясы әртүрлі ландшафты-геологиялық жағдайлардың кең диапазонында сақталады. Мысалы: жарлулары радиоактивті ыдыраумен байланысты тұрақты ассоциациялар – U, Pb, He, Th-Pb-He, K-Ar.
Егер ассоциациялардың жаралуына негізгі әсерді ішкі факторлар тигізсе, онда элементтердің бірге орналасуы нақты жағдайлардың кешенімен шектелген. Мысалы: Au-Cu-As-Pb-Zn-Fe – ассоциациясы тек қана алтын құрамды кендерге тән, бұлардың морылуы (при выветривании) кезінде жаңа ассоциациялар пайда болуы мүмкін - Au-As-Fe, Cu-As-Zn-Au-Fe және т.б.
Техногенді геохимиялық аномалияларға химиялық элементтердің өзіндік ассоциациялары тән болады. Олар негізінен ластану кезіндегі ғылым және техниканың даму деңгейімен анықталады. Бұндай аномалиялар – қорғасынмен, мырышпен, мыспен, молибденмен, никельмен, ванадиймен, кобальтпен, бариймен, марганецпен, титанмен, хроммен, темірмен көрсетілген, оларды тағы ластандырғыш заттар деп атайды. Техногенді аномалияларда жеке элементтермен жаралған контурлар жиі сәйкес келмейді. Әрбір элементтің техногенді аномалияларының контрастылығы әртүрлі болуы мүмкін.
Геохимиялық зерттеулерді жүргізген кезде әртүрлі таужыныстарды жинақтайтын (шөгінді, магмалық, метаморфтық), элементтерді құрайтын элементтер ассоциациясымен жиі кездесуге болады. Мысал ретінде пайдалы қазбалар кенорындарының түпкі таужыныстарында жоғары концентрациясында орналасқан элементтер ассоциациясы туралы мәліметтерді көрсетуге болады (кесте №1).
