
- •II вопросы для самоконтроля
- •III литература:
- •Занятие №2 электропроводность растворов электролитов
- •II вопросы для самоконтроля
- •III литература:
- •Занятие №3 кондуктометрия. Кондуктометрическое титрование
- •I. План изучения темы
- •II. Вопросы для самоконтроля:
- •Лабораторная работа:
- •Занятие №4 электродные процессы. Классификация электродов.
- •II. Вопросы для самоконтроля:
- •Занятие № 5 термодинамика гальванического элемента потенциометрия
- •Лабораторная работа:
- •1. Евстратова к. И. , Купина н. А. , Малахова е. Е. "Физическая и коллоидная химия". М. 1990 - стр.160-200.
- •3. 3. Голиков г.А. «Руководство по физической химии». М. 1988. Стр. 245-248
- •3. Лекционный материал. Занятие №6 потенциометрическое титрование
- •Лабораторная работа:
- •3. Лекционный материал. Занятие №7 полярографический метод анализа
- •Занятие №9 свойства буферных растворов
- •IV. Вопросы для самоконтроля:
- •V Лабораторная работа
- •I. Рассчитать объемы растворов кислоты и соли, которые надо взять для смешивания.
- •III. Методом потенциометрии измерить значение рН полученного раствора.
- •IV. Сравнить экспериментальное значение рН с заданным. Определить погрешность приготовления раствора. Задание №2
- •VI. Литература:
- •6. Лекционный материал.
- •Рефрактометрия
- •2. Лекционный материал. Занятие №11 формальная химическая кинетика
- •3. Голиков г.А. «Руководство по физической химии». М. 1988. Стр.253-258, 265-274.
- •4. Лекционный материал. Лабораторная работа
- •Занятие №12 кинетика химических реакций различных порядков
- •3. Голиков г.А. «Руководство по физической химии». М. 1988. Стр.258-265.
- •4. Лекционный материал. Лабораторная работа
- •Занятие №13 влияние температуры на скорость химической
- •3. Голиков г.А. «Руководство по физической химии». М. 1988. Стр.276-296.
- •4. Лекционный материал. Лабораторная работа
- •Занятие №14 каталические реакции. Ферментативный катализ.
- •3. Голиков г.А. «Руководство по физической химии». М. 1988. Стр. 338-363.
- •4. Лекционный материал. Лабораторная работа
- •Занятие №15 основы фармакокинетики
- •I. План
- •II. Цель самоподготовки
- •VI. Литература.
- •2. Лекционный материал. Занятие №16
- •(Коллоквиум)
Занятие №3 кондуктометрия. Кондуктометрическое титрование
I. План изучения темы
1. Измерение сопротивления раствора электролита с помощью моста Кольрауша.
1. Определение удельной электропроводности по величине сопротивления раствора электролита.
3. Кондуктометрия. Прямая кондуктометрия и кондуктометрическое титрование.
4. Определение степени диссоциации и константы диссоциации слабого электролита, ионного произведения воды, произведения растворимости труднорастворимой соли по электропроводности раствора электролита.
5. Кондуктометрическое титрование. Назначение, особенности и техника выполнения метода.
6. Кривые кондуктометрического титрования. Анализ хода кривых титрования (нахождение эквивалентного объема, изменение ионного состава по ходу титрования):
:
а) сильной кислоты сильным основанием;
б) слабой кислоты сильным основанием;
в) смеси сильной и слабой кислот сильным основанием.
II. Вопросы для самоконтроля:
1. Что отражает "константа (постоянная) кондуктометрической ячейки"?
2. Запишите уравнение для расчета константы кондуктометрической ячейки (КЯ) по измеренному сопротивлению стандартного раствора и табличному значению его удельной электропроводности.
3. Приведите уравнение для расчета удельной электрической проводимости раствора электролита по величине сопротивления раствора электролита и константе кондуктометрической ячейки.
4. Какие величины можно определить, измеряя электропроводность (сопротивление) раствора электролита?
5. Как определить кондуктометрически:
а) степень диссоциации слабого электролита;
б) константу диссоциации слабого электролита;
в) ионное произведение воды;
г) произведение растворимости труднорастворимой соли?
6. Запишите уравнение для расчета степени и константы диссоциации слабого электролита по измеренной электропроводности.
7. Почему электропроводность растворов электролитов измеряют при постоянной температуре?
8. Назовите особенности, назначение и преимущества кондуктометрическтго титрования.
9. Приведите кривые кондуктометрического титрования раствора:
а) сильной кислоты;
б) слабой кислоты;
в) смеси сильной и слабой кислоты раствором щелочи.
10. Объясните особенности хода кривых кондуктометрического титрования раствора:
а) сильной кислоты;
б) слабой кислоты;
в) смеси сильной и слабой кислоты раствором щелочи.
11. Приведите схему моста Кольрауша и охарактеризуйте принцип определения сопротивления раствора электролита.
12. Почему при измерении сопротивления раствора электролита пользуются переменным током высокой частоты?
Лабораторная работа:
КОНДУКТОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ СТЕПЕНИ И КОНСТАНТЫ ДИССОЦИАЦИИ СЛАБОГО ЭЛЕКТРОЛИТА
№ п/п |
Вид действия |
Способ действия |
|||
1. |
Определить постоянную электролитической ячейки |
1. Измерить сопротивление 0,01 N KCl (см.приложение).
2.
Рассчитать постоянную ячейки
= 0, 001278 Ом-1см-1. |
|
||
2. |
Установить значения удельной электропроводности растворов уксусной кислоты с концентрациями: 0,05 0,025 0,0125 0,00625 0,003125 |
1. Измерить сопротивление каждого из предложенных растворов. 2. Рассчитать, используя найденное на 1 этапе значение постоянной ячейки, удельную электропроводность каждого раствора
|
|
||
3. |
Установить значения эквивалентной электропроводности и степени диссоциации уксусной кислоты в предложенных растворах |
1.
Рассчитать для каждого раствора
эквивалентную электропроводность
как
2.
Степень диссоциации кислоты в каждом
растворе найти как
|
|
||
4. |
Установить зависимость удельной, эквивалентной электропроводностей и степени диссоциации уксусной кислоты от ее концентрации в растворе |
1. Построить графики:
а)
б)
в)
|
|
||
5. |
Найти среднее значение константы электролитической диссоциации уксусной кислоты. |
1. Для каждого из растворов уксусной кислоты рассчитать KДИС по уравнению
2. Установить среднее значение Kg CH3COOH |
|
||
Полученные данные внести в таблицу:
№ п/п |
С |
RХ, Ом |
Х, Ом-1см-1 |
V, Ом-1моль-1см2 |
|
KДИС |
1 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
4 |
|
|
|
|
|
|
5 |
|
|
|
|
|
|
Провести сравнение с табличным значением Кдис уксусной кислоты.
Приложение
ОПРЕДЕЛЕНИЕ СОПРОТИВЛЕНИЯ РАСТВОРА ЭЛЕКТРОЛИТА С ПОМОЩЬЮ ПРИБОРА
"СПУТНИК РАДИОЛЮБИТЕЛЯ".
Прибор "Спутник радиолюбителя" состоит из 3-х блоков:
1. Измерительный блок
2. Звуковой генератор
3. Блок питания
Измерительный блок служит для измерения омического (Rа), индуктивного (Rс) или емкостного (с) сопротивлений. Собран измерительный блок по мостиковой схеме, принципиально имеющий вид:
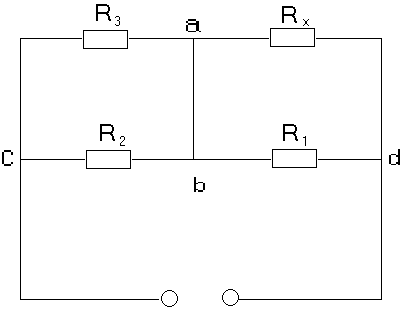
Диагональ моста "сd" питается от 2-го блока - звукового генератора, в диагональ "ав" включается телефон.
Звуковой генератор генерирует 8 фиксированных частот, которые могут быть использованы в работе. При измерении сопротивления используется одна из частот, генерируемых звуковым генератором. Питание звукового генератора осуществляется блоком питания, который в свою очередь питается от сети переменного тока с частотой 50 гц и напряжением 220 в.
ПОСЛЕДОВАТЕЛЬНОСТЬ РАБОТЫ С ПРИБОРОМ:
1. Блок питания подключить в сеть переменного тока.
2. К клеммам "RL" измерительного блока подключить электролитическую ячейку.
Электролитическая ячейка представляет собой два платиновых электрода с фиксированным расстоянием между открытой частью электродов, и опущенных в раствор, сопротивление которого хотят определить. Для определения сопротивления в сосуд электролитической ячейки наливают такое количество испытуемого раствора, чтобы электроды были погружены своей открытой частью на 50 мм ниже уровня жидкости в сосуде.
3. Установить переключатель частот звукового генератора на частоте 1 кгц.
4. Переключатель вида измерений (1-ый блок) установить на минимальное омическое сопротивление (R3).
5. Вращением ручки "множитель", стрелка указатель которой покажет значение R1/R2, добиться минимального звука в наушниках. Если при данном значении R3 минимальный звук отсутствует при всех возможных положениях переключателя "множитель", или имеет место, когда этот переключатель находится в одном из крайних положений, следует изменить величину сопротивления R3 и подобрать такое его значение, при котором минимальный звук в телефонных наушниках будет иметь место, когда стрелка-указатель множителя находится внутри шкалы. Перемножив показание переключателя вида измерений на показание множителя, получим значение измеряемого сопротивления:
![]()
III. ЛИТЕРАТУРА:
1. Евстратова К. И. , Купина Н. А. , Малахова Е. Е. "Физическая и коллоидная химия". М. 1990. стр.139-160.
2. Стромберг А. Г. , Семченко Д. П. "Физическая химия". М. 1999. стр. 246-247.
3. Голиков Г.А. «Руководство по физической химии». М. 1988. стр. 225-227
4. Лекционный материал.
При подготовке к занятию использовать методические рекомендации предыдущего занятия.
