
- •2. Білки молока 66
- •Тема 1. Властивості розчинів біополімерів, як високомолекулярних сполук
- •1.1. Природні біополімери
- •Одержання біополімерів
- •1.3. Деякі властивості вмс
- •1.4. Набухання та розчинення
- •1.5. Молекулярно-масові розподілення біополімерів
- •1.6. Драглі полімерів
- •Пластифікація полімерів
- •Тема 2. В’язкість розчинів вмс
- •В’язкість розчинів вмс
- •Поліелектроліти
- •Білки як поліелектроліти
- •Ізоелектрична точка білків
- •2.5. Колоїдний захист
- •2.6. Біологічне значення онкотичного тиску
- •Тема 3. Набухання високомолекулярних сполук
- •3.1. Явище набухання полімерів. Значення в природі та техніці
- •3.2. Вплив форми макромолекул полімерів
- •3.3. Ентропійний характер набухання
- •3.4. Стадії набухання та розчинення полімерів
- •Тема 4. Термодинаміка розчинення
- •Термодинамічна характеристика процесу розчинення вмс.
- •Вплив природи розчинника і полімеру на значення термодинамічних показників процесу розчинення
- •Тема 5. Дублення
- •5.1. Дублення
- •5.2. Вулканізація
- •5.3. Деструкція полімерів
- •5.4. Механічна деструкція
- •5.5. Термічна деструкція
- •5.6. Фотохімічна деструкція
- •5.7. Ультразвукова деструкція
- •Лабораторна робота №4-5
- •1. Лактоза молока
- •2. Білки молока
- •Лабораторна робота №12
- •Глосарій
Тема 5. Дублення
План:
5.1. Дублення.
5.2. Вулканізація.
5.3. Деструкція полімерів.
5.4. Механічна деструкція.
5.5. Термічна деструкція.
5.6. Фотохімічна деструкція.
5.7. Ультразвукова деструкція.
5.1. Дублення
Дублення – поширений різновид структурування біополімерів. Воно представляє цікавість не тільки при структуруванні білків у виробництві натуральної шкіри, але і при виготовленні білкових клеїв, шкір, картонів та ін. Дублення, напевне, буде в подальшому відігравати важливу роль у виробництві нових видів штучної шкіри.
Певні речовини при взаємодії з білками проявляють властивості, які спричиняють дублення білків. До них відносяться неорганічні сполуки: солі хрому, алюмінію, заліза, кремнію, титану, цирконію та ін., органічні сполуки рослинного походження (екстракти), жири, масла, альдегіди, а також синтетичні продукти (синтани) типу поліфенолів, сульфокислот і деякі промислові відходи (лігносульфонові кислоти).
В технології одержання матеріалів для виготовлення взуття використовуються солі хрома, алюмінію, рослинні екстракти, жири та альдегіди. В результаті недостатнього вивчення таких складних поліфункціональних об’єктів, як білкові речовини, на сьогодні немає однозначних уявлень про механізму дублення. Однак, в цілому ефект дублення безсумнівно є наслідок змішаного структурування білків сполуками, які викликають дублення з утворенням широкого набору просторових хімічних, ковалентних, координаційних зв’язків та всіх видів міжмолекулярної взаємодії.
Так, при дубленні білків катіонними комплексними сполуками хрому утворюються поперечні зв’язки за рахунок включення кислотних (-COOH) та основних (-NH2) груп бокових частин білкових ланцюгів у внутрішню сферу хромових комплексів.
Для аніонних комплексів аналогічна взаємодія, проходить, ймовірніше, за участю основних груп. Одночасно з координаційними зв’язками в цьому випадку можливо утворення інших типів зв’язків.
Одна з найпростіших схем структурування при хромовому дубленні має наступний вигляд:
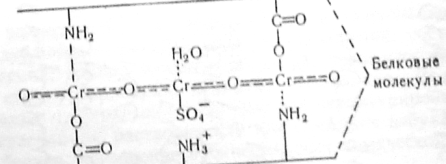
Схема 5.1. Структурування білків при хромовому дубленні.
Дія інших дубильних мінеральних солей в цілому анологічна.
При дубленні жирами, які містять залишки легкоокислюваних ненасичених жирних кислот, не виключається утворення наступних видів поперечних зв’язків:

Схема 5.2.1. Структурування білків при дубленні жирами.
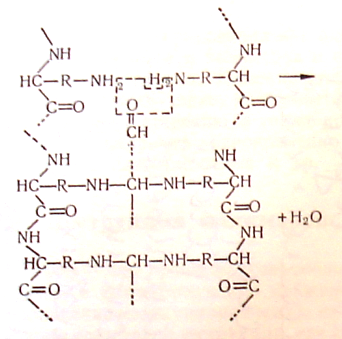 .
.
Схема 5.2.2. Структурування білків при дубленні жирами.
В цьому випадку активною сполукою є перекис. Дублення прискорюється при збільшенні притоку кисню повітря, при помірному підвищенні температури, присутності каталізаторів (сиккативів) та ін.
Рослинні екстракти, як складні поліфункціональні сполуки типу депсидів, поліфенолокислот та ін., імовірно, можуть структурувати білки за рахунок різних видів зв’язку, які умовно можна описати наступною схемою:
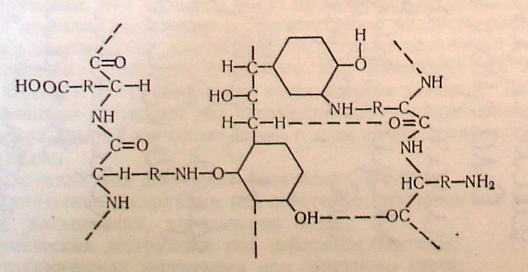
Схема 5.3. Структурування білків при дубленні рослинними екстрактами.
Дубильну дію альдегідів, внаслідок відносної простоти їх будови, вивчено більш повно. Так, вже не викликає сумнівів той факт, що при взаємодії білка з альдегідом останній переважно реагує з основними (-NH2) групами білкових ланцюгів, блокуючи їх:
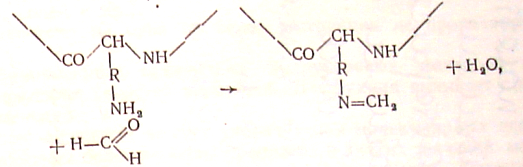
Або «зшиває» групи сусідніх ланцюгів,

Схема 5.4. Структурування білків при дубленні альдегідами.
Треба підкреслити, що блокування функціональних груп білка при дубленні є найважливіший етапом тому, що без «зшивання», тобто структурування, дублення неможливе. В результаті дублення в білках відбуваються типові для структурування зміни властивостей: втрата розчинності, зниження набухання нерозчинних білків, підвищення міцності, ріст хімічної стійкості.
