
- •Практическая работа №3
- •Ход работы
- •1. Фильтрование пробы воды с помощью бумажных фильтров
- •2. Консервирование на различные ингредиенты
- •Консервация проб
- •Практическая работа №4
- •1. Определение растворенного кислорода
- •Ход работы
- •Определение точной вместимости кислородных склянок и склянок бпк5
- •2. Определение бпк5
- •Ход работы
- •Практическая работа № 6
- •Ход работы
- •Практическая работа № 7
- •Ход работы
- •Практическая работа № 8
- •Цель работы – научиться количественному определению массовой концентрации общего железа в пробах природных и очищенных сточных вод фотоколориметрическим методом с 2,2-дипиридилом.
- •Ход работы
- •8. Расчет
- •Практическая работа №9
- •Часть 1. Весовой метод
- •Ход работы
- •Часть 2. Турбидиметрический метод
- •Ход работы
- •Практическая работа №10
- •Ход работы
- •Ход работы
- •Ход работы
- •Практическая работа №11
- •Ход определения
- •II. Тонкослойная хроматография.
- •III. Элюирование
- •IV. Измерение
- •V. Расчет.
- •VI. Оформление результатов с учетом погрешности метода.
- •Практическая работа №12
- •Ход работы
Практическая работа № 8
Определение содержания железа в пробах природной и питьевой воды. Определение общего железа и двухвалентного железа фотометрическим методом, приготовление реактивов, растворов, построение градуировочного графика. Проведение измерений, расчет концентраций железа в воде.
Цель работы – научиться количественному определению массовой концентрации общего железа в пробах природных и очищенных сточных вод фотоколориметрическим методом с 2,2-дипиридилом.
Диапазон измерения массовой концентрации общего железа без разбавления пробы – 0,05-2,00 мг/дм3.
В этом интервале суммарная погрешность измерения с вероятностью Р=0,95 находится в пределах 0,01-0,03 мг/дм3.
Приборы, посуда, реактивы: КФК-3, мерные колбы на 50 см3, пипетки градуированные на 1, 2 см3, пипетки Мора на 25 см3, мерные колбы вместимостью 50 см3, р-ры: гидроксиламина солянокислого, ацетатного буферного раствора, 2,2-дипиридила.
Метод основан на взаимодействии ионов двухвалентного железа с 2,2-дипиридилом в области рН 3,5-8,5 с образованием окрашенного в красный цвет комплексного соединения трехвалентного железа. Интенсивность окраски пропорциональна массовой концентрации железа. Восстановление трехвалентного железа до двухвалентного проводится гидраксиламином. Окраска развивается быстро и устойчива в течение нескольких дней.
Ход работы
1. Исследуемую пробу воды тщательно перемешать
2. Отобрать 25 см3 (или меньший объем, содержащий не более 0,1 мг железа/дм3) в мерную колбу вместимостью 50 см3.
3. Прибавить 1 см3 10%-ного раствора гидроксиламина солянокислого, 2,00 см3 ацетатного буферного раствора, 1,00 см3 раствора 0,1%-ного раствора 2,2-дипиридила и довести до метки дистиллированной водой. После добавления каждого реактива содержимое колбы тщательно перемешать.
4. Раствор оставить на 15-20 минут для полного развития окраски.
5. Окрашенный раствор фотометрировать, применяя зеленый светофильтр (λ =540 нм) и кюветы с толщиной оптического слоя 1-5 см, по отношению к дистиллированной воде, в которую добавлены те же реактивы.
6. Массовую концентрацию железа С, мг/дм3, найти по градуировочному графику
7. Для построения градуировочного графика в мерные колбы вместимостью 50 см3 внести 0,0; 2,0; 10,0; 15,0; 20,0 см3 рабочего стандартного раствора железоаммонийных квасцов (0,005 Fe/см3). Добавить до объема 25 см3 дистиллированной водой. Далее провести анализ полученных растворов, как исследуемой пробы воды. Оптическую плотность измерить в тех же условиях, что и пробы. Построить градуировочный график, откладывая по оси абцисс массовую концентрацию железа, в мг/дм3, а по оси ординат – соответствующие значения оптической плотности.
8. Рассчитать
коэффициент а методом наименьших
квадратов по формуле:
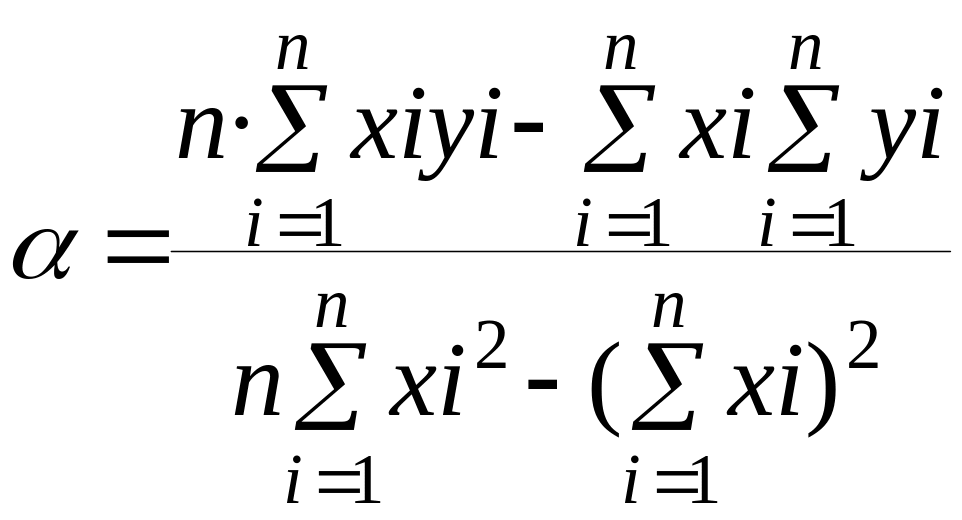 ,
где
,
где
n – количество измерений, х – концентрация железа, мг/дм3, D – оптическая плотность. Сравнить с найденным значением коэффициента а= D/С по калибровочной кривой (пакет анализа EXСEL – статистические расчеты)
Градуировочные графики на железо общее
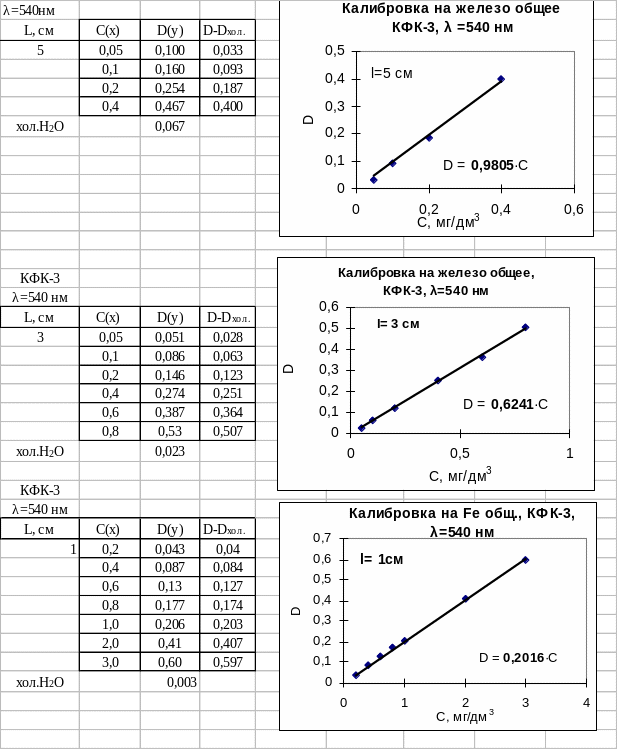
8. Расчет
Массовую концентрацию
железа (Х) в анализируемой пробе, мг/дм3,
с учетом разбавления вычислить по
формуле:
![]()
![]() ,
где С – концентрация железа, найденная
по градуировочному графику (или
рассчитанная по формуле Х=D/a,
где D = Dиссл.пр.
– Dхол. –Dпр.
, где Dиссл.пр. – оптическая
плотность исследуемой пробы, Dхол.
– оптическая плотность холостой пробы
– дистиллированная вода, Dпр.а
– оптическая плотность пробы (фон), а
– коэффициент, найденный из уравнения
регрессии или методом наименьших
квадратов), мг/дм3; V
– объем воды, взятой для анализа, см3;
50 – объем, до которого разбавлена проба,
см3.
,
где С – концентрация железа, найденная
по градуировочному графику (или
рассчитанная по формуле Х=D/a,
где D = Dиссл.пр.
– Dхол. –Dпр.
, где Dиссл.пр. – оптическая
плотность исследуемой пробы, Dхол.
– оптическая плотность холостой пробы
– дистиллированная вода, Dпр.а
– оптическая плотность пробы (фон), а
– коэффициент, найденный из уравнения
регрессии или методом наименьших
квадратов), мг/дм3; V
– объем воды, взятой для анализа, см3;
50 – объем, до которого разбавлена проба,
см3.
За окончательный результат анализа принимают среднее арифметическое результатов двух параллельных измерений, допустимое расхождение между которыми не должно превышать 25% при массовой концентрации железа на уровне предельно допустимой. Результат округляют до двух значащих цифр.
ПДКв железа составляет 0,3 мг Fe/дм3 (лимитирующий показатель вредности – органолептический), ПДКвр – 0,1 мг/дм3 (лимитирующий показатель вредности – токсикологический).
Вывод. Охарактеризовать пробу воды по содержанию в ней железа. Сравнить полученную величину с ПДК.
