
- •Практическая работа №3
- •Ход работы
- •1. Фильтрование пробы воды с помощью бумажных фильтров
- •2. Консервирование на различные ингредиенты
- •Консервация проб
- •Практическая работа №4
- •1. Определение растворенного кислорода
- •Ход работы
- •Определение точной вместимости кислородных склянок и склянок бпк5
- •2. Определение бпк5
- •Ход работы
- •Практическая работа № 6
- •Ход работы
- •Практическая работа № 7
- •Ход работы
- •Практическая работа № 8
- •Цель работы – научиться количественному определению массовой концентрации общего железа в пробах природных и очищенных сточных вод фотоколориметрическим методом с 2,2-дипиридилом.
- •Ход работы
- •8. Расчет
- •Практическая работа №9
- •Часть 1. Весовой метод
- •Ход работы
- •Часть 2. Турбидиметрический метод
- •Ход работы
- •Практическая работа №10
- •Ход работы
- •Ход работы
- •Ход работы
- •Практическая работа №11
- •Ход определения
- •II. Тонкослойная хроматография.
- •III. Элюирование
- •IV. Измерение
- •V. Расчет.
- •VI. Оформление результатов с учетом погрешности метода.
- •Практическая работа №12
- •Ход работы
Практическая работа № 6
Определение интегральных показателей воды. Определение бихроматной окисляемости (БО) или химического потребления кислорода (ХПК) в поверхностных и очищенных сточных водах
МУ РД 52.24-421-95.
Цель: Научиться определять ХПК титриметрическим методом в пробах воды.
Приборы, оборудование, хим. реактивы: весы технические, шкаф сушильный, бани песчаные, колбы мерные вместимостью: 500 см3, пипетки градуированные на 1, 5, 10, 20, 50 см3,бюретка на 25 см3, цилиндры мерные на 25, 50, 100, 250 см3, 1 дм3, колбы конические на 0,5 дм3, стаканы химические на 0,5, 1,0 дм3, капельница, колбы круглодонные с пришлифованным обратным холодильником на 250 см3 (установки для определения ХПК), стеклянные капилляры, устройство для фильтрования проб с использованием мембранных или бумажных фильтров; р-ры: дихромата калия (калий двухромовокислый), соли Мора (NH4)2Fe(SO4)2·6Н2О, гидроксида натрия, N-фенилантраниловой кислоты, cульфат серебра, сульфат ртути, серная кислота, фильтры мембранные "Владипор МФА-МА", 0,45 мкм или фильтры бумажные обеззоленные "синяя лента", вода дистиллированная.
Диапазон определения содержания ХПК – 4-80 мг О/дм³. При величине ХПК > 50 мг О /дм3 определение следует проводить при соответствующем разбавлении пробы дистиллированной водой.
ХПК – количество кислорода, расходуемого на окисление содержащихся в воде органических и неорганических веществ в кипящем дихромате калия в кислой среде с добавлением катализатора:
Cr2O72-+4H++6ē→Cr3++7H2O
Ход работы
В колбу “О” (холостую) налить 20 см3 дистиллированной воды, в колбу «1» – 20 см3 исследуемой воды.
В обе колбы добавить 10 см3 (0,025 моль/дм3-экв) раствора К2Сг2О7 + 30 см³ Н2SО4 (концентрированной) + 150 мг Аg2SО4 (катализатор).
Бросить 2-3 стеклянных капилляров для равномерного кипения. К колбе присоединить обратный холодильник и поставить на песчаную баню, кипятить 2 часа.
4. Дать остыть колбе. Холодильник промыть 50 см3 дистиллированной водой, отсоединить холодильник и добавить еще 50 см3 дистиллированной воды и обмыть стенки колбы. Содержимое колбы охладить.
5. Перелить в коническую колбу, дважды ополаскивая круглодонную колбу дистиллированной водой по 20-30 см³.
6. Добавить 10 капель индикатора – фенилантрониловой кислоты.
7. Содержимое оттитровать солью Мора (0,025 моль/дм3-экв) – оттитровывается избыток дихромата калия в присутствии индикатора до перехода окраски из красно-фиолетовой в синевато-зеленую.
8. Аналогично проделать с колбой “0”.
9. Расчет:
Величину ХПК, мг О/дм3 рассчитать по формуле:
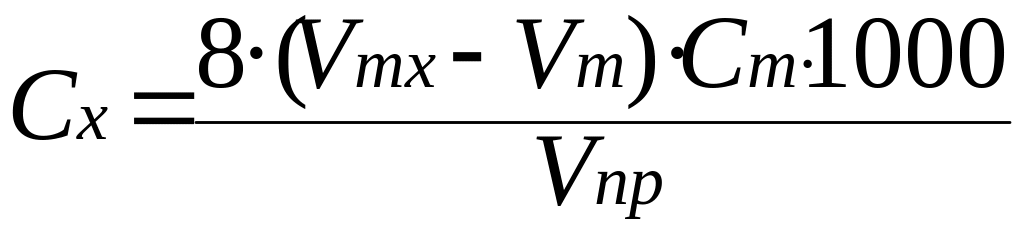 ,
,
где 8 – молекулярный вес атомарного кислорода;
Vmх – объем раствора соли Мора израсходованного на титрование в холостой пробе, см3;
Vm – объем раствора соли Мора израсходованного на титровании исследуемой пробы, см³;
9. Определение точной концентрации раствора соли Мора.
– Пипеткой Мора отобрать 10 см3 р-ра К2Сг2О7 0,025 моль/дм3-экв. в
коническую колбу.
– Добавить 180 см3 дистиллированной воды.
– Добавить 20 см3 H2SO4 (конц.) и 10 капель фенилантрониловой кислоты (после охлаждения).
– Титровать раствором соли Мора с N≈0,025 моль/дм³-экв. до перехода окраски из красно-фиолетовой в сине-зеленую.
– Титрование повторить.
– Расхождение результатов не должно быть > 0,05 см³. За результат принять среднее значение.
Точную концентрацию
раствора соли Мора найти по формуле:
![]() ,
где
,
где
См – концентрация раствора соли Мора, моль/дм3-эквивалента;
Сд – концентрация раствора дихромата калия, моль/дм3-эквивалента;
Vд – объём раствора дихромата калия, взятый для титрования, см3;
Vм – объём раствора соли Мора, пошедший на титрование, см3.
__
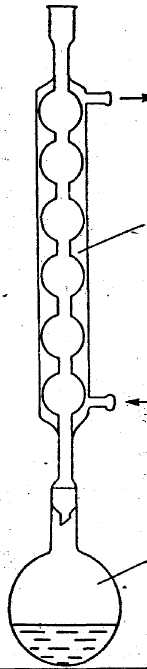
Рис. 4. Прибор для определения ХПК.
1 – кругдодонная колба для кипячения;
2 – обратный холодильник.
ПДКхпк = 15 мг О/дм³ для питьевой воды, ПДКхпк =30 мг О/дм³ для зоны рекреации.
Таблица
Степень загрязнения воды по величину ХПК
Степень загрязнения |
Величина ХПК, мг О/дм3 |
Очень чистая |
1 |
Чистая |
2 |
Умеренно загрязненная |
3 |
Загрязненная |
4 |
Грязная |
5-15 |
Очень грязная |
>15 |
Вывод: Дать оценку степени загрязнения исследуемой воды (по табл.), сравнить полученную величину ХПК с ПДК.
Нормы погрешности для определения в водах ХПК не установлены.
