
- •Основы оптики
- •Глава 1. Структура твердых тел, типы связей между ионами, дефекты в кристаллах
- •Глава 2. Основы теории поля
- •Глава 3. Система уравнение Максвелла и понятие об электромагнитной волне
- •Глава 4. Волновые уравнения для электромагнитного поля как следствия из электродинамики Максвелла
- •Глава 5. Интерференция когерентных электромагнитных волн
- •Глава 11. Поляризация оптического излучения
- •Глава 12. Зависимость коэффициента отражения от угла ввода излучения в диэлектрик
- •Глава 13. Волновая и лучевая природа законов отражения и преломления света
- •Глава 14. Основы лучевой и волновой оптики диэлектрических волноводов
- •Глава 15. Уширение импульсных сигналов в процессе их распространения по стекловолокну
- •Глава 16. Физическая природа ослабления сигналов в процессе их распространения по стекловолокнам
- •Глава 17. Основы фотометрии
- •Глава 1. Структура твёрдых тел, типы связей между ионами, дефекты в кристаллах
- •Понятие об идеальном монокристалле, элементарной ячейке, кристаллографических системах, классах и группах [1, 2]
- •Типы связей мевду ионами в твёрдых телах [3]
- •Ионы и ионная связь в молекулах
- •1.4. Ионно-ковалетный тип связи в твердых телах
- •1.5. Дефекты кристаллической структуры [5]
- •Аморфные тела, изотропия и анизотропия
- •Глава 2. Основы теории поля
- •2.1. Градиент скалярной' функции [8, стр. 36]
- •2.2. Поток вектора
- •Дивергенция вектора
- •2.4. Теорема остроградского - гаусса
- •2.5. Циркулшия вектора по контуру
- •2.6. Ротор вектора
- •2.7. Теорема стокса
- •Теорема остроградского – гаусса.
- •Теорема стокса.
- •Глава 3. Система уравнений максвелла и понятие об электромагнитной волне [8, с. 99-312], [9]
- •3.1 Система уравнений Максвелла в интегральной форме и электромагнитная волна
- •3.2. Вектор пойнтинга
- •3.3. Интенсивность электромагнитной волны
- •3.4. Система уравнений максвелла в дифференциальной форме
- •3.5. Система уравнений максвелла в операторной форме
- •Глава 4. Волновые уравнения для злектромагнигного поля как следствия из электродинамики максвелла
- •4.1. Вывод волновых уравнений [8, с. 302-306]
- •4.2. Волновой фронт [8, с. 276]
- •4.2. Волновая поверхность [8, с. 276]
- •4.4. Плоская электромагнитная волна
- •4.5. Решение волнового уравнения для плоской электромагнитной волны и его анализ
- •4.6. Фаза электромагнитной волны. Временная и пространственная характеристики фазы
- •4.7. Фазовая скорость
- •4.8. Волновой вектор
- •4.9. Монохроматическая электромагнитная волна
- •Фазовая скорость.
- •5.1. Взаимосвязь абсолютного показателя преломления диэлектрика с фазовой скоростью электромагнитной волны в нем и относительной диэлектрической проницаемостью
- •5.2. Оптическая и геометрическая длина пути элетромагнитной волны в веществе [8, с. 333]
- •5.3. Когерентные электромагнитные волны
- •5.4. Линейн0-п0ляри30ванная электромарнитная волна [8, с. 428]
- •5.5. Интерференция когерентных монохроматических электромагнитных волн, распространяющихся в однородной, изотропной диэлектрической среде
- •Глава 6. Отличие реального оптического излучения от идеальной монохроматической волны
- •6.1. Механизм излучения фотонов и образование волновых пакетов электромагнитных волн
- •6.2. Групповая скорость волнового пакета
- •6.3 Взаимосвязь фазовой скорости с грунтовой
- •Взаимосвязь фазовой скорости с групповой.
- •Глава 7. Когерентность оптического излучения
- •7.1. Временная когерентность [1 с. 347-370, 10]
- •7.2. Пространственная когерентность
- •7.3. Объем когерентности
- •Глава 8. Двухлучевая и многолучевая интерференции
- •8.1. Двухлучевая интерференция, интерферометр майкельсона [10, с. 134-136]
- •8.2. Многолучевая интерференция.
- •8.3. Интерференционный светофильтр [11 с. 204]
- •Глава 9. Электронная теория дисперсии
- •9.1. Взаимодействие валентного электрона диэлектрика с воздействующей на него электромагнитной волной
- •9.2. Дифференциальное уравнение движения для валентного электрона
- •9.3. Анализ решения дифференциального уравнения
- •9.4. Анализ зависимости
- •Глава 10. Дифракция свеta
- •10.1. Суть явлений дифракции
Типы связей мевду ионами в твёрдых телах [3]
Известны следующие типы связей в твердых телах: металлическая, ковалентная, ионная, водородная и другие. В большинстве диэлектриков связь, как правило, комбинированная - ионно-ковалентная. Этот тип связи типичен для большинства полупроводников и материалов, используемых для создания ВОЛС.
Ионы и ионная связь в молекулах
Известно, что электронейтральный этом, присоединивший к своей электронной оболочке один или более электронов, превращается в отрицательный ион.
Атом, отдавший из оболочки электроны, превращается в положительный ион. В качестве примера ионной связи рассмотрим взаимодействие ионов в молекуле сульфида кадмия (CdS ).
В процессе образования молекулы, атом Cd 0 отдает 2 своих валентных электрона атому S 0, превращаясь в положительный ион с устойчивой электронной оболочкой из 46 электронов:
Cd
0 - 2![]() Cd 2+
+ 2
Cd 2+
+ 2![]() ,
(рис. 1.8).
,
(рис. 1.8).
Рисунок 1.8
Атом серы S 0, присоединяя два электрона превращается в отрицательный ион с устойчивой оболочкой из 18 электронов:
S 0 + 2 S 2-, (рис. 1.9).
Под действием сил кулоновского притяжения положительный ион Cd 2+ и отрицательный ион S 2- начинают сближаться (рис. 10 а). Сближение ионов прекращается после перекрытия их электронных оболочек (рис. 1.10 б), поскольку силы кулоновского отталкивания оболочек преобладают над силами притяжения ионов. Под действием сил отталкивания ионы расходятся до тех пор, пока электронные оболочки не выйдут из состояния перекрытия. После этого снова начинается сближение ионов (рис. 1.10 в), и далее процесс повторяется. Таким образом, в молекуле любого вещества ее ионы находятся в состоянии непрерывного колебательного движения.

Рисунок 1.9

Рисунок 1.10
Заметим, что в большинстве случаев колебания дестабилизируют равновесие любой системы. В данном случае, колебания - основа существования молекулы.
1.4. Ионно-ковалетный тип связи в твердых телах
В качестве примера рассмотрим ионно-ковалентный тип связи в гексагональном монокристаллическом CdS, сочетающем в себе свойства полупроводника и пьезодиэлектрика [4], достаточно широко применяющемся в технике современной связи и радиолокации. В гексагональном CdS каждый ион Cd находится в тетраэдрическом окружении четырех ионов серы (рис. 1.11). Поскольку вероятность захвата двух электронов, отдаваемых атомом Cd 0, для каждого из четырех атомов S 0 одинакова, валентные электроны становятся коллективными, т.е. плотность электронного заряда "размазывается" по четырем соседним атомам S 0, на долю каждого из которых приходится 2 : 4 = 0,5 . На условной плоской сетке такое распределение зарядов можно представить в виде рисунка 1.12.
С другой стороны, каждый ион серы находится в тетраэдрическом окружении четырех ионов кадмия (рис. 1.13). На условной плоской сетке электронные связи иона серы с ионами Cd 2+ можно изобразить так, как показано на рисунках 1.14 и 1.15. Из рисунка 14 видно, что связь иона S 2- с четырьмя ионами Cd 2+ является комбинированной (гибридизированной) из четырех электронных пар. На каждом ионе S 2- замыкаются 4 связи, каждая из которых дает по 0,5 .
Поскольку положительные ионы Cd 2+ взаимодействуют с отрицательными ионами S 2- посредством парных электронов, рассмотренный тип связи носит название ионно-ковалентного.

Рисунок 1.11

Рисунок 1.12

Рисунок 1.13
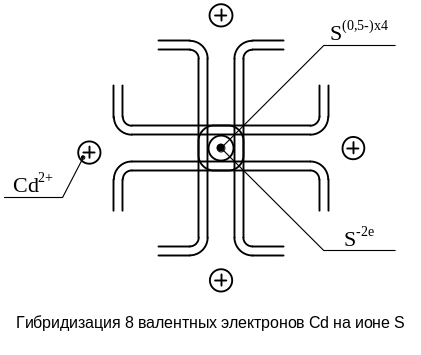
Рисунок 1.14
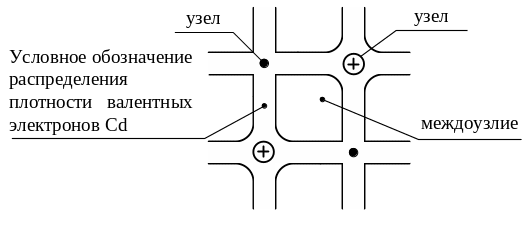
Рисунок 1.15
