
- •Спектрофотометрический анализ однокомпонентных систем Цель работы: Изучение физических основ и методики проведения спектрофотометрического анализа однокомпонентных молекулярных систем.
- •Задание
- •Простые тесты на число компонент а.Однокомпонентные системы
- •В. Закрытые двухкомпонентные системы
- •С. Открытые двухкомпонентные системы.
- •Порядок выполнения работы
- •Литература:
ЛАБОРАТОРНАЯ РАБОТА
Спектрофотометрический анализ однокомпонентных систем Цель работы: Изучение физических основ и методики проведения спектрофотометрического анализа однокомпонентных молекулярных систем.
Приборы и оборудование: Спектрофотометр СФ-26, набор кювет, однокомпонентная молекулярная система.
Задание
Измерить электронный спектр поглощения анализируемого раствора в области 400-900 нм, Выбрать аналитическую длину волн
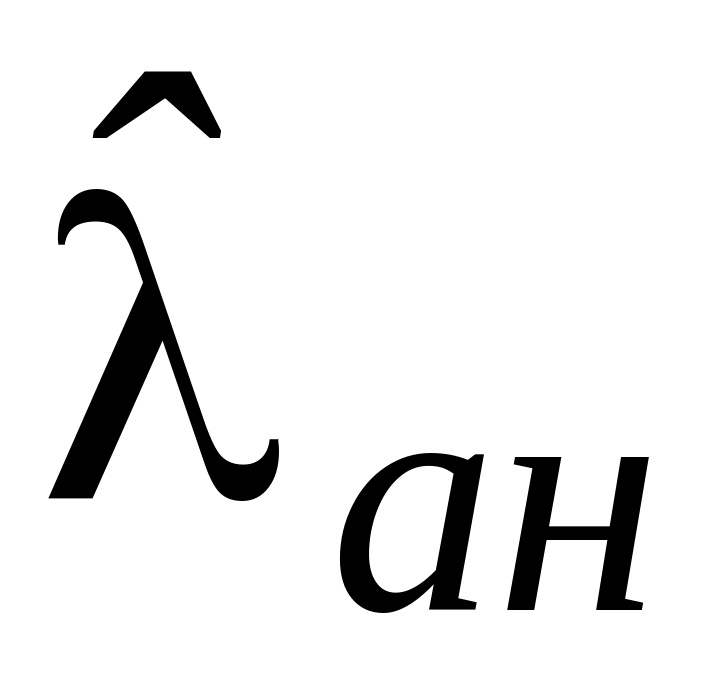 .
.Определить возможный интервал концентраций определяемого вещества. Приготовить 4-5 стандартных растворов.
Измерить значения
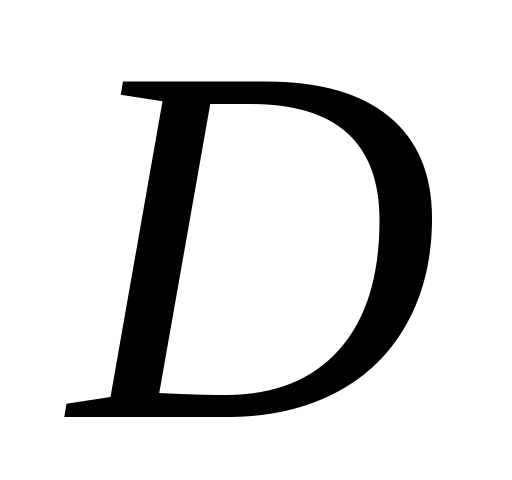 на длине волны
для всех стандартных растворов. Построить
аналитическую кривую.
на длине волны
для всех стандартных растворов. Построить
аналитическую кривую.Измерить значения
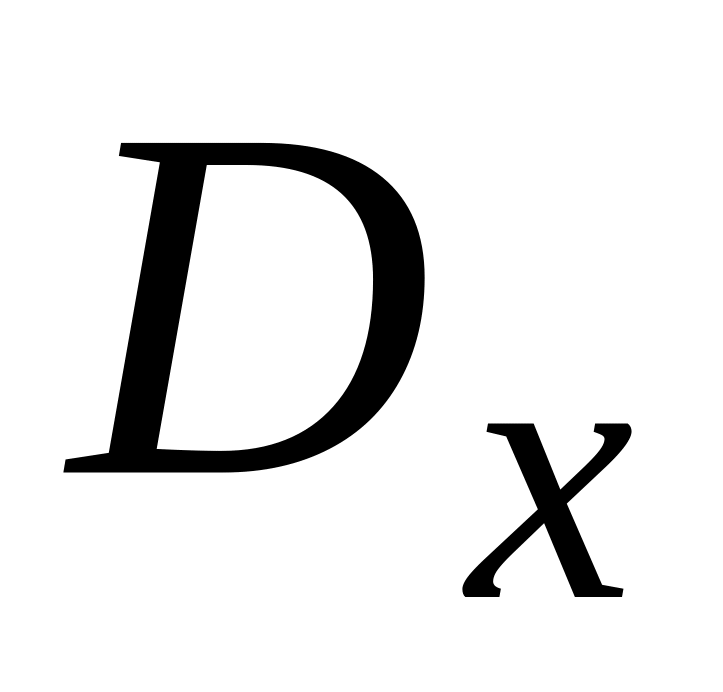 анализируемого
раствора на длине волны
.
Пользуясь аналитической кривой,
определить концентрацию определяемого
вещества.
анализируемого
раствора на длине волны
.
Пользуясь аналитической кривой,
определить концентрацию определяемого
вещества.Изучить следующие вопросы:
Определение числа компонентов методом тестов:
Однокомпонентные системы,
Закрытые двухкомпонентные системы,
Открытые двухкомпонентные системы.
Анализ однокомпонентных систем с неизвестным коэффициентом экстинкции компонента
 .
.
Теоретическое введение
Целью количественного спектрофотометрического молекулярного анализа является определение концентрации молекулярного вещества в смеси или растворе (в пробе) на основе спектра поглощения пробы.
Физической основой абсорбционного спектрофотометрического анализа однокомпонентной пробы является закон Бугера
![]() ,
(1)
,
(1)
где I0
–
интенсивность
падающего на вещество монохроматического
излучения, I-
интенсивность излучения, прошедшего
через слой вещества, толщина которого
l,
![]() - коэффициент
экстинкции (молекулярный
показатель поглощения),
описывающий поглощательные свойства
вещества на данной длине волны, с
– концентрация поглощающего вещества
в растворе.
- коэффициент
экстинкции (молекулярный
показатель поглощения),
описывающий поглощательные свойства
вещества на данной длине волны, с
– концентрация поглощающего вещества
в растворе.
Закон Бугера можно записать и в другой форме:
![]() ,
(2)
,
(2)
где
![]() – оптическая плотность поглощающего
вещества на данной длине волны.
– оптическая плотность поглощающего
вещества на данной длине волны.
Зависимости D(λ), D(ν), ….; ε(λ), ε(ν), … , - представляют собой спектр поглощения.
При изучении реакционных смесей в первую очередь возникает вопрос о числе входящих в них компонентов и об их идентификации.
Компонентом молекулярного раствора (смеси) называется вещество, присутствующее в растворе и поглощающее излучение в используемом диапазоне длин волн.
Псевдокомпонентом называется смесь нескольких веществ, которые присутствуют в растворах всегда в постоянном соотношении.
Закрытой называют такую систему, в которой концентрации компонентов связаны зависимостью:
![]() (или
(или
![]() ),
(3)
),
(3)
где: νi – стехиометрический коэффициент i го компонента; сi – концентрация i го компонента х – любой параметр, влияющий на концентрацию компонентов.
Системы,
для которых
![]() ,
называются открытыми.
,
называются открытыми.
Изомолярной называют серию растворов с постоянной суммарной концентрацией реагирующих веществ, но с различным отношением из концентраций.
Задача определения числа компонентов в анализируемой системе решается различными методами. Наиболее распространенным методом числа компонентов является метод тестов. Суть метода состоит в том, что для спектрофотометрической системы, содержащей заданное число компонентов, должны выполняться вполне определенные соотношения между измеряемыми величинами, а именно, между значениями оптической плотности, соответствующими различным длинам волн и различным состояниям растворов. Реализация метода тестов состоит в проверке выполнимости (или невыполнимости) этих соотношений.
