
- •Москва, 2002
- •Глава 1. Биохимические основы церебрального энергетического обмена
- •Заключение
- •Глава 2. Современные методы оценки церебрального энергетического обмена
- •Заключение
- •Глава 3. Использование электрофизиологических показателей для оценки церебрального энергетического обмена
- •3.1. История изучения уровня постоянных потенциалов головного мозга
- •Глава 4. Современные методы регистрации и анализа уровня постоянных потенциалов головного мозга человека
- •Глава 5. Энергетический обмен при развитии и старении мозга
- •5.2. Церебральный энергетический обмен в среднем возрасте
- •5.3. Церебральный энергетический обмен при старении
- •Глава 6. Закономерности изменения церебрального энергетического обмена при различных функциональных состояниях
- •6.4. Влияние гипервентиляции на показатели энергетического обмена мозга
- •Глава 7. Изменение церебрального энергетического обмена при заболеваниях центральной нервной системы
- •7.1.1. Нарушения энергетического обмена при заикании
- •7.3. Энергетический обмен мозга при болезни Альцгеймера
- •Глава 8. Связь церебрального энергетического обмена с функциональной активностью и гемодинамикой мозга
- •Глава 9. Взаимосвязь церебрального энергетического обмена с характеристиками иммунитета
- •Глава 10. Церебральный энергетический обмен и некоторые психофизиологические характеристики личности
- •Глава 11. Энергетические характеристики деятельности мозга и функциональная межполушарная асимметрия (фма)
- •Предисловие
- •Глава 1
- •Общие представления об энергетическом обмене
- •1.2. Особенности энергетического обмена мозга
- •1.5. Специфические механизмы регуляции рН ликвора и мозга
- •Заключение
- •Глава 2
- •2.1. Неинвазивные методы исследования энергетического обмена мозга (пэт, ямр-спектроскопия и др.)
- •2.2. Электрофизиологические методы для определения энергетического обмена
- •Глава 3
- •3.1. История изучения уровня постоянного потенциала головного мозга
- •3.4. Потенциалы сосудистого происхождения
- •3.5. Что мы регистрируем от кожи головы с помощью неполяризуемых электродов и усилителя постоянного тока?
- •3.6. Форма распределения упп по поверхности головы. Принципы интерпретации упп
- •Глава 4.
- •4.1. Виды постоянных потенциалов
- •4.2. Принципы регистрации упп и возможные артефакты
- •4.3. Современная аппаратура для изучения постоянных потенциалов
- •4.4. Процедура регистрации упп
- •4.5. Семиотика основных параметров упп
- •4.6. Пространственно-временной анализ упп
- •4.7. Нормативное шкалирование упп
- •Глава 5
- •5.1. Церебральный энергетический обмен в детстве
- •5.2. Церебральный энергетический обмен в среднем возрасте
- •5.3. Церебральный энергетический обмен при старении
- •5.4. Динамика упп мозга при развитии и старении
- •5.6. Нейрофизиологические предикторы смерти
- •Заключение
- •Глава 6
- •6.3. Изменение церебрального энергетического обмена при обучении
- •6.6. Изменения церебрального энергетического обмена при стрессе
- •6.6.3. Исследование взаимосвязи между параметрами упп головного мозга и уровнем гормона стресса кортизола
- •6.7.1. Упп у мужчин-спортсменов до и после тренировочной нагрузки
- •6.7.2. Упп у женщин-спортсменок до и после тренировочной нагрузки
- •6.7.4. Упп мозга и прогноз спортивных достижений
- •Заключение
- •Глава 7
- •7.1.2. Динамика церебрального энергетического обмена у больных заиканием при гипнозе
- •7.2.2. Изменения церебрального энергетического обмена у больных наркоманиями при гипнозе
- •7.3. Энергетический обмен мозга при болезни Альцгеймера
- •7.3.3. Стресс и энергетический обмен при ба
- •Покампе, то у больных ба эта зависимость нарушена (m.J. De Leon et al., 1997), что свидетельствует о десенситизации нейронов гиппокампа к глюкокортикоидам.
- •7.3.4. Стресс и перекисное окисление липидов при ба
- •7.3.5. Упп и вызванные потенциалы при ба
- •7.6. Церебральный энергетический обмен у больных с опухолями мозга
- •Заключение
- •Глава 8
- •8.1.1. Взаимосвязь параметров упп и ээг у здоровых испытуемых в состоянии спокойного бодрствования
- •8.1.2. Взаимосвязь параметров упп и ээг у здоровых испытуемых при гипервентиляции
- •8.1.3. Взаимосвязь ээг и церебрального энергетического обмена у родственников больных болезнью Альцгеймера в состоянии спокойного бодрствования
- •8.1.4. Взаимосвязь ээг и церебрального энергетического обмена у родственников больных болезнью Альцгеймера при гипервентиляции
- •8.2 Взаимосвязь церебрального энергетического обмена и вызванных потенциалов
- •8.2.1. Связь упп в затылочной области с компонентами зрительных вызванных потенциалов
- •8.2.2. Интегральная оценка взаимосвязи между распределением упп и характеристиками звп. Энергоинформационные состояния
- •Коэффициенты корреляции между латентными периодами звп и упп мозга после акупрессуры биологически активных зон
- •8.3. Вызванные потенциалы мозгового ствола и упп
- •Коэффициенты корреляции между параметрами упп и свпмс
- •8.4. Реоэнцефалограмма и характеристики упп
- •Заключение
- •Глава 9
- •Заключение
- •Глава 10
- •10.1. Функциональные энергетические состояния мозга и процесс обучения у младших школьников
- •10.2. Психофизиология успеха и избегания неудач у детей
- •10.3. Психофизиология старения
- •Глава 11
- •11.1. История изучения упп головного мозга и фма
- •11.2 Современный этап изучения динамической функциональной межполушарной асимметрии с помощью упп головного мозга
- •11.3. Межполушарная разность упп в височных областях у мужчин и женщин разного возраста
- •11.4. Динамика межполушарной асимметрии упп у правшей в течение дня
- •11.5. Различия в распределении упп у правшей и левшей
- •11.6. Анализ связи между различными видами асимметрий и распределением упп
- •11.7. Устойчивость межполушарной асимметрии упп при различных нагрузках
- •Устойчивость межполушарной разности упп в височных отведениях при различных нагрузках
- •11.8. Устойчивость межполушарной асимметрии при нагрузках в условиях патологии
- •11.9. Особенности характеристик звп, биохимических и иммунологических показателей в трех группах лиц с различной функциональной асимметрией
- •11.9.1. Характеристики звп
- •11.9.2. Иммунологические характеристики
- •Заключение
- •Общее заключение
- •Литература
1.2. Особенности энергетического обмена мозга
В отличие от других органов, энергетические потребности мозга удовлетворяются в основном за счет аэробного катаболизма глюкозы. Мозг практически не способен к синтезу глюкозы из белков и жиров (глюконеогенезу). Прохождение глюкозы через гемато-энцефалический барьер (ГЭБ), то есть барьер между кровью и мозгом, и ее поступление в нейроны и глию связано с системой транспортных белков, которая формируется в онтогенезе (S.J. Vannucci et al., 1994). На долю пассивной диффузии приходится не более 5% от общего переноса глюкозы.
Для осуществления своей деятельности мозг нуждается в значительном притоке энергии. Хотя масса мозга составляет приблизительной 2% от массы тела взрослого человека, он расходует свыше 20% всей потребляемой организмом энергии (G. Siebert et al., 1986). Существует большой разброс данных об использовании поступившей в мозг глюкозы. Согласно G. Siebert, (1986), около 7% глюкозы в результате гликолиза превращается в лактат и в таком виде поступает в кровоток, 30% глюкозы подвергается аэробному окислению в цикле Кребса, а 60% глюкозы используется для синтеза аминокислот, нейромедиаторов, гликолипидов и гликопротеидов. По другим данным (Н.Д. Ещенко, 1999), около 85-90% глюкозы полностью окисляется до СО2 и Н2О, около 5% расходуется в реакциях гликолиза и лишь 5-7% используется для синтеза аминокислот, нейромедиаторов и др.
Интенсивность процессов дыхания максимальна в коре больших полушарий, несколько меньше в мозжечке и промежуточном мозге. При переходе к филогенетически более старым отделам мозга – среднему, продолговатому и спинному мозгу - наблюдается ее дальнейшее снижение (Н.Д. Ещенко, 1999).
С помощью меченого углерода показано, что потребление глюкозы связано с увеличением активности структур мозга. Так, при световой стимуляции метаболизм глюкозы в первичной и ассоциативной зрительной коре увеличивался от 12 до 59% в зависимости от условий эксперимента, при тактильной и слуховой стимуляции нарастание метаболизма глюкозы выявлено в соответству
12
ющих проекционных областях (G. Siebert, et al., 1986). Энергопродукция значительно усиливается при эпилептических судорогах и снижается при фенобарбиталовом наркозе (Н.Д. Ещенко, 1999).
При повышение энергетических потребностей (например, при стрессе) в нервной ткани увеличивается гликолиз. Анаэробное окисление усиливается также при некоторых видах патологии, в частности при гипоксии и ишемии, что сопровождается накоплением лактата. Это может происходить и после тяжелой черепно-мозговой травмы, при болезни Альцгеймера и др. (A. Zauner et al., 1997).
Если поступление глюкозы в мозг снижается то в качестве энергетического источника могут быть использованы также продукты окисления жирных кислот - кетоновые тела. Повышенная утилизация кетоновых тел наблюдается у плода и в раннем детском возрасте. Снижение использования мозгом кетоновых тел для энергетического метаболизма по мере взросления обусловлено сокращением их концентрации в крови, уменьшением проницаемости ГЭБ для этих веществ и изменением активности ключевых ферментов, лимитирующих скорость этого процесса (Н.Д. Ещенко, 1999). При использовании кетоновых тел в качестве энергетического источника происходит закисление нервной ткани (ацидоз). Такой тип метаболизма у взрослого наблюдается при стрессе и некоторых видах патологии, например при сахарном диабете, гипертиреозе. Но даже в этих случаях за счет окисления свободных жирных кислот и кетоновых тел покрывается не более 20% энергетических потребностей мозга.
В качестве энергетического источника мозг может также использовать аминокислоты. В этом случае распад осуществляется по
13
метаболическому пути, получившему название шунта гамма-аминомасляной кислоты (ГАМК). Использование шунта ГАМК при дефиците глюкозы может приводить к повышению уровня ГАМК в случае увеличения расхода энергии. Так как ГАМК является тормозным медиатором, то повышение ее уровня снижает функциональную активность определенных отделов мозга. Этот процесс может рассматриваться как регуляция по механизму отрицательной обратной связи: высокая церебральная активность вызывает дефицит глюкозы, он запускает шунт ГАМК, в результате чего накапливается аминокислота, тормозящая мозговую активность. В норме использование шунта ГАМК ограничено.
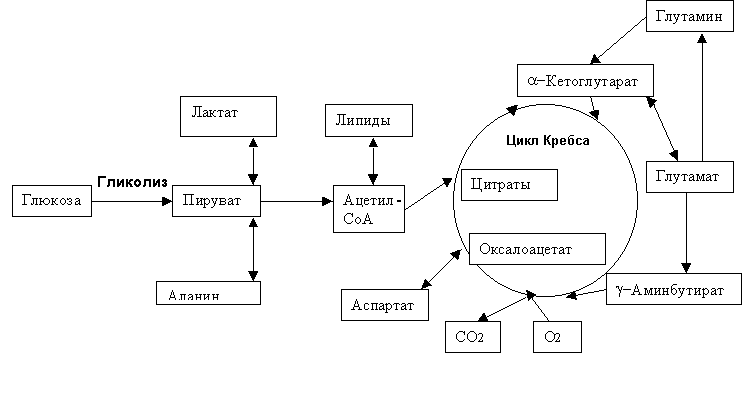
Рис. 1.1. Упрощенная схема метаболизма глюкозы в мозге (по G. Siebert et al, 1986.)
Высокая скорость энергетического обмена мозга связана с интенсивным образованием макроэргических соединений – АТФ и креатинфосфата. Система креатинфосфат - креатин играет роль в стабилизации уровня макроэргических соединений мозга (Н.Д. Ещенко, 1999).
1.3. Конечные продукты энергетического обмена. Изменение кислотно-щелочного равновесия при энергетическом обмене
При гликолизе и цикле Кребса конечными продуктами обмена являются лактат, углекислый газ и вода. СО2 частично вступает в реакцию с водой с образованием ионов Н+ и НСО3-. Поэтому, в целом, при катаболическом превращении глюкозы и других веществ происходит смещение кислотно-щелочного равновесия (КЩР) в кислую сторону. Однако существуют эффективные механизмы поддержания стабильности кислотно-щелочного баланса в мозге, о которых будет рассказано в следующем параграфе.
Для характеристики КЩР принято использовать рН - отрицательный десятичный логарифм концентрации водородных ионов. В зависимости от того, в какую сторону изменяется реакция жидких сред организма, существует два типа нарушений КЩР. Понижение рН по сравнению с нормальным уровнем называется ацидозом, а повышение - алкалозом.
1.4. Общие представления о кислотно-щелочном равновесии в крови и мозге. Потенциалы ГЭБ
Водородный показатель крови и, особенно, мозга поддерживается на достаточно стабильном уровне, а его изменения существенное влияют на активность многих ферментных систем. Несмотря на то, что выброс кислых продуктов метаболизма в кровь меняется, слабощелочная реакция крови, характерная для человека, поддерживается в узких пределах (рН 7,37-7,43). В регуля
14
ции КЩР участвуют несколько механизмов, связанных с буферными свойствами крови, газообменом в легких, выделительной функцией почек.
Буферные свойства обусловлены содержанием в крови или других жидкостях бикарбонатов, неорганических фосфатов и белков, которые соединяются с избытком кислот или оснований и образуют вещества, не влияющие на рН.
Регуляция рН с помощью газообмена происходит следующим образом. В зависимости от состояния КЩР дыхательный цикл меняется так, чтобы через усиление или ослабление поступления кислорода и выделения углекислого газа нормализовать кислотно-щелочной баланс мозга. При системном метаболическом нарушении pН хорошо контролируется модуляцией дыхания цикла. Дыхательный цикл трансформируется под воздействием внеклеточной концентрации ионов водорода, влияющих на хеморецепторы продолговатого мозга (O. Rabary, 1994). Изменения происходят достаточно быстро - за несколько минут.
Почки регулируют КЩР, увеличивая или снижая концентрацию HCO3- и H+ в жидкостях организма. Изменения рН происходят медленно - в течение нескольких часов или даже суток.
При ряде патологических состояний в крови накапливаются такие большие количества кислот или оснований, что описанные регуляторные механизмы не могут поддерживать рН на оптимальном уровне.
