- •Фогель ф., Мотульски а. Генетика человека: в 3-х т. Т. 2: Пер. С англ. – м.: Мир, 1990. – 378 с.
- •Ф. Фогель, а.Мотульски генетика человека
- •4. Действие генов
- •4.1. Развитие менделевской парадигмы
- •4.2. Гены и ферменты
- •4.2.1. Гипотеза «один ген – один фермент»
- •Модель Бидла и Татума. Статья этих исследователей начиналась так:
- •4.2.2. Гены и ферменты у человека: современный уровень знаний
- •4.2.2.1. Обнаружение и анализ ферментативных нарушений
- •4.2.2.2. Типичные нарушения функций ферментов: ферменты эритроцитов
- •4.2.2.3 Мукополисахаридозы
- •4.2.2.5. Влияние кофакторов на активность ферментов [182]
- •4.2.2.6. Сцепленная с х-хромосомой недостаточность гипоксантин-гуанин—фосфорибозилтрансферазы (30800) [7055]
- •4.2.2.7. Фенилкетонурия: пример успешного лечения метаболического заболевания [182; 203]
- •4.2.2.8. Выявление гетерозигот
- •4.2.2.9. Лечение наследственных метаболических заболеваний [1289; 1057; 1058]
- •4.2.2.10. Необнаруженные дефекты ферментов
- •4.3. Гемоглобин человека [119; 31; 97а]
- •4.3.1. История изучения гемоглобина
- •4.3.2. Генетика гемоглобина
- •4.3.4. Талассемии [31; 972; 138; 1253; 222; 97а]
- •4.3.5. Популяциоииая генетика генов гемоглобина (см. [972], разд. 6.1.2.3)
- •4.3.6. Пренатальная диагностика гемоглобинопатии [966; 2269; 2322; 2361]
- •4.4. Генетика антител и системы антиген/рецептор
- •4.5. Фармакогенетика и экогенетика 4.5.1. Фармакогенетика
- •4.5.2. Экогенетика [143; 969; 1228; 1250]
- •4.6. Механизм аутосомной доминантности
- •4.6.1. Аномальная агрегация субъединиц
- •4.6.2. Аномальные субъединицы нарушают функции мультимерных белков
- •4.6.3. Аномальное ингибирование ферментов по типу обратной связи и структурно аномальные ферменты
- •4.6.4. Мутации рецепторов
- •4.6.5. Наследственные дефекты клеточных мембран
- •4.6.6. Накопление аномальных фибриллярных белков: наследственные амилоидозы (10480 10525) [1102]
- •4.6.7. Доминантно наследуемые опухолевые заболевания
- •4.7. Генетика эмбрионального развития
- •4.7.1. Активность генов в раннем развитии
- •4.7.2. Поздние стадии эмбрионального развития; фенокопии
- •4.7.3. Регуляция активности генов у бактерий и эукариот
- •4.7.4. Соотношения генотипа и фенотипа при хромосомных аберрациях у человека [1176]
- •4.7.4.1. Эффект дозы генов при трисомиях и картирование генов
- •4.7.4.2. Другие биохимические аномалии при хромосомных аберрациях
- •4.7.4.3. Изучение хромосомных аберраций на уровне клеток
- •4.7.5. Определение поля
- •5. Мутации
- •5.1. Спонтанные мутации
- •5.1.1. Генетические изменения, обусловленные мутациями de novo
- •5.1.2. Геномные и хромосомные мутации у человека
- •5.1.2.1. Частота возникновения мутаций (скорость мутирования)
- •5.1.2.2. Нерасхождение хромосом и возраст матери
- •5.1.2.3. У какого пола и в каком из мейотических делений происходит нерасхождение хромосом?
- •5.1.2.4. Нерасхождение, хромосомные варианты и сателлитные ассоциации
- •5.1.3. Генные мутации: анализ на фенотипическом уровне
- •5.1.3.1. Методы оценки частот мутаций
- •5.1.3.2. Результаты оценки частот мутаций
- •5.1.3.3. Частота мутаций и возраст отца
- •5.1.3.4. Возможные различия частот возникновения мутаций у индивидов разного пола
- •182 5. Мутации
- •5.1.3.5. Герминативноклеточные и соматоклеточные мозаики по доминантным и х-сцепленным мутациям
- •5.1.4. Генные мутации: анализ на молекулярном уровне
- •5.1.4.1. Частоты кодонных мутаций
- •5.1.4.2. Проблема оценки общей частоты мутаций на геном и на поколение
- •5.1.4.3. Мутации в гемоглобиновых генах и генетический код
- •5.1.4.4. Мутации у микроорганизмов: их вклад в понимание механизма мутаций у человека
- •5.1.5. Изучение генных мутаций в отдельных клетках
- •5.1.6. Соматические мутации
- •5.1.6.1. Образование мозаиков по геномным мутациям
- •5.1.6.2. Наследственные синдромы с повышенной нестабильностью хромосом [1465; 1464; 1634]
- •5.1.6.3. Молекулярные механизмы хромосомной нестабильности и образование опухоли, обусловленное соматической мутацией
- •5.1.6.4. Другие факты, свидетельствующие о роли соматической мутации в механизме канцерогенеза [1520]
- •5.1.6.5. Онкогены [1686; 1690, 1691, 1696}
- •5.1.6.6. Рак у человека с точки зрения генетики
- •5.1.6.7. Соматические мутации и старение
- •5.2. Мутации, индуцированные облучением и химическими мутагенами
- •5.2.1. Мутации, индуцированные радиацией
- •5.2.1.1. Основные факты и проблемы, поставленные в ходе их анализа
- •5.2.1.2. Проблема оценки генетического риска, обусловленного радиацией и другими мутагенными факторами окружающей среды
- •5.2.1.3. Результаты изучения мутагенного действия радиации на млекопитающих [1377]
- •5.2.1.4. Облучение популяции человека ионизирующей радиацией
- •5.2.1.5. Насколько может увеличиться частота возникновения спонтанных мутаций9
- •Данные о соматических хромосомных мутациях, возникающих под воздействием радиации.
- •5.2.2. Химически индуцированные (мутации)
- •5.2.2.1. Суть проблемы
- •5.2.2.2. Исследовательские стратегии при оценке генетического риска, обусловленного химическими мутагенами
- •5.2.2.3. Каким образом химические мутагены действуют на генетический материал?
- •5.2.2.4. Насколько широким является воздействие агента на человеческую популяцию?
- •5.2.2.5. Какого увеличения частоты спонтанных мутаций, обусловленного химическими мутагенами, следует ожидать?
- •6. Популяционная генетика
- •6.1. Описание популяций
- •6.1.1. Закон Харди—Вайнберга: генные частоты
- •6.1.2. Генетический полиморфизм
- •6.1.3. Наследственные болезни
- •6.2. Систематические изменения генных частот: мутации и отбор
- •6.2.1. Естественный отбор
- •6.2.1.1. Математические модели отбора: дарвиновская приспособленность
- •6.2.1.2. Отбор, приводящий к изменению генных частот в одном направлении
- •6.2.1.3. Отбор, приводящий к генетическому равновесию
- •6.2.1.4. Отбор, приводящий к нестабильному равновесию
- •6.2.1.5. Другие формулы отбора
- •6.2.1.6. Отбор, обусловленный инфекционными болезнями [1831; 211]
- •История некоторых инфекционных заболеваний.
- •6.2.1.7. Естественный отбор и история популяций: НbЕ и β-талассемия 1)
- •6.2.1.8. Отбор по системе групп крови аво и другим полиморфным системам
- •6.3. Отклонение от случайного скрещивания
- •6.3.1. Кровнородственные браки
- •6.3.1.1. Коэффициент инбридинга [103]
- •6.3.1.2. Инбридинг, размер изолята и наследственные заболевания
- •6.3.2. Концепция генетического груза
- •6.3.2.1. Теория
- •6.3.2.2. Практическое применение теории
- •6.3.2.3. Критическая оценка
- •6.3.2.4. Более прямые подходы к оценке числа рецессивных генов на индивид
- •6.3.3. Дифференциация субпопуляций: генетическое расстояние
- •6.3.4. Поток генов
- •6.4. Случайные флуктуации генных частот
- •6.4.1. Генетический дрейф
- •6.4.2. Генетический дрейф в сочетании с мутационным процессом и отбором
- •Оглавление
- •Глава 4 Действие генов 5
- •Глава 5. Мутации 142
- •Глава 6. Популяционная генетика 278
- •Электронное оглавление
- •4. Действие генов 5
- •4.1. Развитие менделевской парадигмы 5
- •4.2. Гены и ферменты 8
- •4.7. Генетика эмбрионального развития 126
- •5. Мутации 142
- •5.1. Спонтанные мутации 142
- •5.2. Мутации, индуцированные облучением и химическими мутагенами 222
- •6. Популяционная генетика 278
- •6.1. Описание популяций 279
- •6.2. Систематические изменения генных частот: мутации и отбор 294
- •6.3. Отклонение от случайного скрещивания 339
- •6.4. Случайные флуктуации генных частот 367
6.1. Описание популяций
6.1.1. Закон Харди—Вайнберга: генные частоты
Закон Харди—Вайнберга в случае аутосомных генов [124]. Закон Харди—Вайнберга обсуждался в разд. 3.2. Пусть аллели А1 и А2 имеют частоты А1 = р, А2 = q; р + q = 1; предположим, что скрещивание происходит случайным образом. Тогда частоты фенотипов в популяции будут следующими: p2AiA1, 2pqA1A2, q2A2A2. Это правило можно обобщить следующим образом. Если частоты п аллелей А1, А2, ..., Аn равны p1, p2 …pn и если скрещивание случайно по отношению к данному локусу, то частоты фенотипов определяются случайным попарным сочетанием этих аллелей:
![]()
В отсутствие возмущающих воздействий частоты генов и генотипов остаются постоянными от поколения к поколению. Для аутосомных генов такое состояие «равновесия Харди—Вайнберга» достигается в первом поколении случайного скрещивания. Однако в случае генов, сцепленных с полом, это не так.
Закон Харди—Вайнберга для случая генов, сцепленных с полом. Пусть аллели А1 и А2 встречаются в мужской части популяции с частотами pМ и qM(pМ + qM = 1), тогда фенотипы А1 и А2 будут также иметь частоты рМ и qM. Пусть среди женщин частоты генотипов A1A1, A1A2 и А2А2 равны r, 2s и t(r + 2s + t = 1). Тогда частоты аллелей А1 и А2 у женщин равны рF = г + s и qF = s + t соответственно. Эти женщины образуют ооциты типа A1 и А2 также с частотой pF и qF соответственно. Среди их сыновей аллели А1 и А2 встречаются в том же соотношении. Однако их дочери происходят от яйцеклеток, образовавшихся в результате слияния ооцитов (pFA1 + qFA2) и сперматозоидов, несущих Х-хромосому (рMА1 + + qМА2). Таким образом, следующее поколение будет иметь состав
![]()
Отсюда следует, что частоты аллеля А2 у мужчин и женщин следующего поколения
280 6. Лопуляционная генетика
равны
![]()
Это означает, что а) частота А2 у мужчин каждого поколения равна частоте А2 у женщин предыдущего поколения; б) частота А2 у женщин каждого поколения равна средней частоте этого аллеля у мужчин и женщин предыдущего поколения; в) справедливо равенство
![]()
Следовательно,
если аллельные частоты у мужчин
и женщин в данном поколении не равны,
разность
между ними в следующем поколении
уменьшается вдвое. Кроме того, изменяется
знак этой
разности- если qF
выше
qM,
то
q'M
будет
выше
q'F
Обе аллельные частоты qF
и
qM
сходятся
к общему значению
![]() ,
в
то время как распределение генотипов
у обоих полов стремится к равновесному
состоянию:
,
в
то время как распределение генотипов
у обоих полов стремится к равновесному
состоянию:
![]()
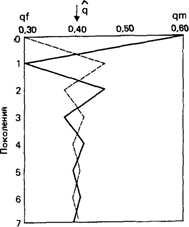
На рис. 6.1 показано, каким образом происходит приближение к состоянию равновесия. Из этого примера следует, что достижение равно ве-
|
Рис. 6.1. Приближение генных частот у мужчин к состоянию равновесия при наследовании, сцепленном с полом, qm = 0,6; qf= 0,3; q = 0,4; сплошной и пунктирной линиями обозначена частота гена у мужчин (qm) и женщин (qf) соответственно, q равновесная частота гена. |
сия Харди Вайнберга после одного поколения случайного скрещивания отнюдь не самоочевидно.
Другие ограничения закона Харди— Вайнберга перечислены в разд. 3.2. Разработке этого фундаментального принципа посвящена значительная часть популяционной генетики.
Генные частоты. Особей, составляющих популяцию, можно классифицировать в соответствии с их фенотипами. В некоторых случаях, особенно в случае генетического полиморфизма, эти фенотипы непосредственно соответствуют генотипам. Однако описание генетической изменчивости популяции на основе частот генотипов оказывается слишком громоздким. Закон Харди —Вайнберга позволяет характеризовать генетическую изменчивость, используя генные частоты. Введение понятия частоты гена упрощает дело; для системы с двумя аллелями вся необходимая информация содержится в одном числе (р или q). Методика определения генных частот в общем виде описана в разд. 3.2 и в приложении 1 (см. также [166; 144]).