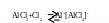- •Типи хімічних зв’язків та їх основні характеристики
- •Будова атома карбону
- •Метод валентних зв’язків
- •Метод мо лкао
- •Класифікація органічних реакцій
- •Класифікація органічних реакцій за типами хімічних перетворень зв’язків
- •Класифікація органічних реакцій за типами розриву зв’язку
- •Класифікація органічних реакцій за типами реагентів
- •Проміжні частинки в органічних реакціях. Взаємний вплив атомів молекулах
- •Алкани (парафіни)
- •Способи одержання алканів
- •Хімічні властивості алканів
- •Окиснення
- •Алкени (олефіни)
- •Способи добування алкенів
- •Дегідратація спиртів (відщеплення води).
- •Дегалогенування віцинальних дігалогеналканів (відщеплення галогенів)
- •Часткове гідрування (відновлення) алкінів (ацетиленів)
- •Хімічні властивості
- •Це явище обумовлене високою стабілізацією алільного проміжного радикалу за рахунок ефекту спряження. Внаслідок, при термічному хлоруванні пропілену:
- •Алкадієни
- •Методи добування
- •Дегідрування бутан-бутиленової бо пентан-пентенової фракції:
- •Дегідратація 1,3- та 1,4- гліколей:
- •Промисловий метод Лєбєдєва із спирту:
- •Електронна бувова спряжених дієнів
- •Хімічні властивості
- •Гідрування.
- •Приєднання галогенів
- •Алкіни (ацетиленові вуглеводні)
- •Методи добування алкінів
- •Аліциклічні сполуки
- •Ароматичні вуглеводні
- •Ароматичні вуглеводні ряду бензолу
- •Добування бензолу та його гомологів
- •Хімічні властивості
- •Прaвила орієнтації електрофільного замііщення в бензольному ядрі
- •Гетероциклічні сполуки
- •Пятичленні гетероциклічні сполуки
- •Способи одержання
- •Хімічні властивості
- •Реакції електрофільного заміщення
- •Шестичленні гетероциклічні сполуки
- •Ароматичні вуглеводні з конденсованими бензольними ядрами нафталін
- •Хімічні властивості
- •Антрацен
- •Загальні методи одержання
- •Хімічні властивості мос (загальні реакції) Магнійорганічні сполуки
- •Перегрупування Арбузова:
- •Галогенпохідні вуглеводнів Галогенпохідними називають сполуки, які містять зв’язки карбон-галоген. Поділяють на
- •Методи добування моногалогенпохідних
- •Хімічні властивості
- •Ароматичні сульфокислоти
- •Хімічні властивості сульфокислот визначаються наявністю сульфогрупи і їх можна розділити на три типи:
- •Реакції сульфогрупи
- •Реакції заміщення сульфогрупи на групи –он; –cn; –nh2.
- •Одно- і багатоатомні спирти
- •Методи одержання спиртів
- •V. Гідрування кетонів.
- •Феноли. Хінони. Методи одержання фенолів
- •Рекція Кольбе-Шмідта – одержання саліцилової кислоти (аспірин)
- •Альдегіди і кетони
- •Способи одержання альдегідів і кетонів
- •Азотовмісні органічні сполуки нітросполуки
- •Способи одержання нітросполук
- •Способи одержання жирно-ароматичних нітросполук
- •Рідкофазне нітруваня за Коноваловим
- •Нуклеофільне заміщення галогену на нітрогрупу
- •Одержання ароматичних нітросполук
- •Хімічні властивості
- •Реакції відновлення з утворенням амінів
- •Класифікація
- •Способи одержання амінів для первинних амінів
- •Для вторинних амінів
- •Для третинних амінів
- •Хімічні властивості
- •Основність амінів
- •Порівняння основності амінів
- •Ароматичні діазо- і азосполуки
- •Реакції діазосполук з виділенням азоту
- •Реакції без виділення азоту
- •Карбонові кислоти
- •Методи одержання одноосновних карбонових кислот
- •6. Реакції окиснення: насичених, ароматичних вуглеводнів, альдегідів і кетонів
- •Гідроліз галогенопохідних
- •Хімічні властивості карбонових кислот
- •Ненасичені кислоти Найпростіші ненасичені одноосновні кислоти:
- •Двохосновні карбонові кислоти
- •Способи одержання двохосновних карбонових кислот
- •Хімічні властивості
- •Кислотні властивості.
- •Реакції за карбоксильною групою
- •Реакції за карбоксильною групою
- •Особливості хімічних властивостей дикарбонових кислот
- •Хімічні властивості
- •Хімічні властивості.
- •Аминокислоты с неполярными или гидрофобными r – группами
- •Аминокислоты с незаряженными полярными r – группами.
Загальні методи одержання
Реакції елементів з галоген алканами (див. галогеналкани).
Реакції МОС з галогені дами більш електронегативних елементів:
![]()
Реакції МОС з більш електронегативними металами:
![]()
Реакції МОС з більш сильними С-Н кислотами:
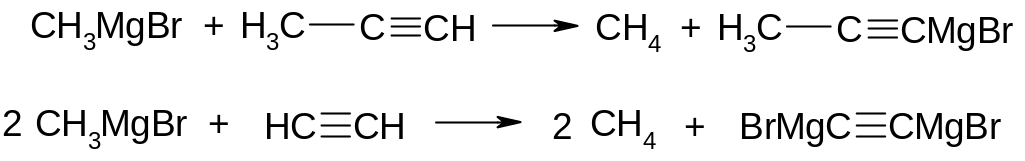
Рушійною
силою всіх реакцій є утворення більш
типової іонної сполуки (![]() )
та більш типової ковалентнозв’язаної
органічної сполуки
)
та більш типової ковалентнозв’язаної
органічної сполуки
![]() .
.
Як правил, всі МОС добувають у відсутності кисню та води.
Хімічні властивості мос (загальні реакції) Магнійорганічні сполуки
І. Розщеплення простих зв’язків
Реакції із сполуками, які мають активній (більш кислий) водень
(реакція Чугуєва-Черевітінова)
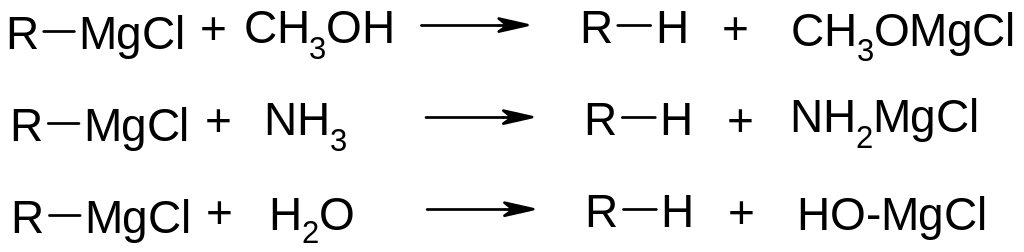
Реакції з електронегативними елементами (О, S, Se, Te, VII-група)
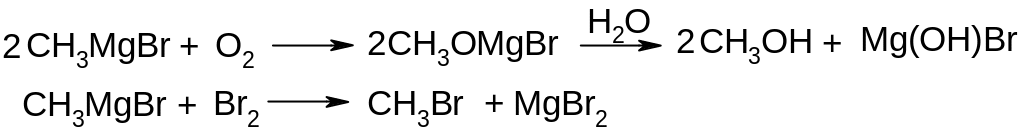
Реакції з галогеналкілами
![]()
ІІ. Приєднання по подвійним зв’язкам
Приєднання по карбонільній групі – утворення спиртів
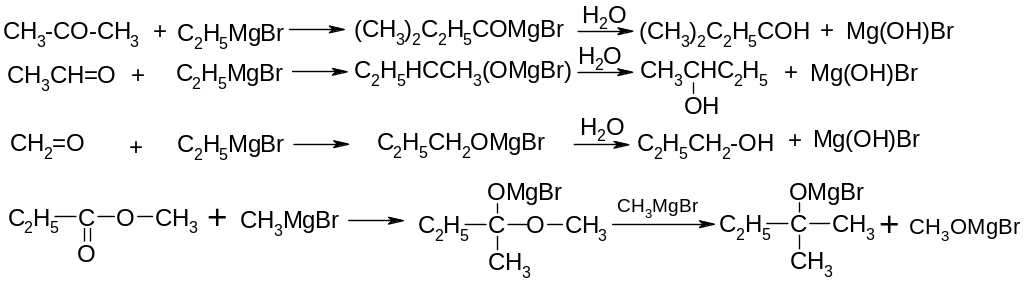
Взаємодія з двоокисом вуглецю – утворення кислот
![]()
Взаємодія з нітрилами – утворення кетонів
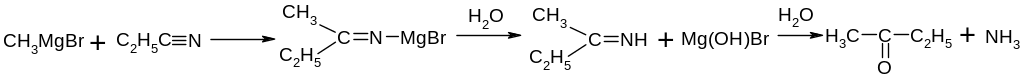
Кремнійорганічні сполуки
Енергія зв’язку Si-Si менша від енергії зв’язку С-С на 125 кДж/моль, тоді як енергія зв’язку С-О менша від енергії зв’язку SiO на 92,1 кДж/моль. Тому для кремнійорганічних сполук характерні не зв’язки Si-Si, а зв’язки Si-О-Si:
Алкілхлорсилани, алкілсилани.
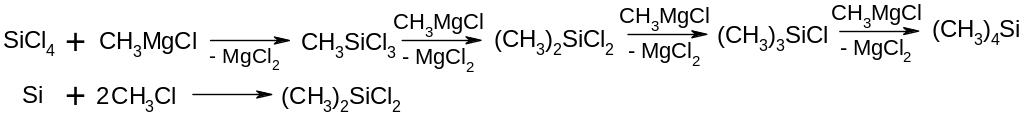
Силаноли, силоксани, силікони.
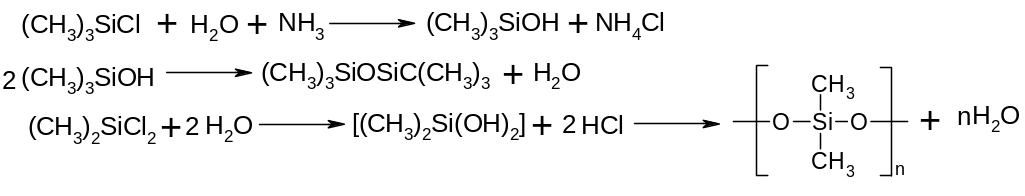
Фосфорорганічні сполуки
Фосфіни:
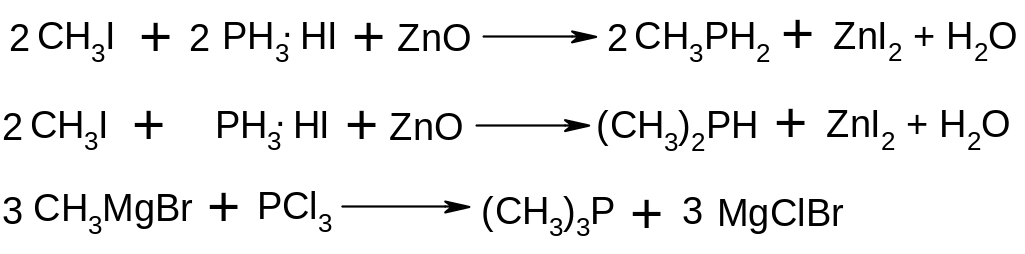
Окиснення:
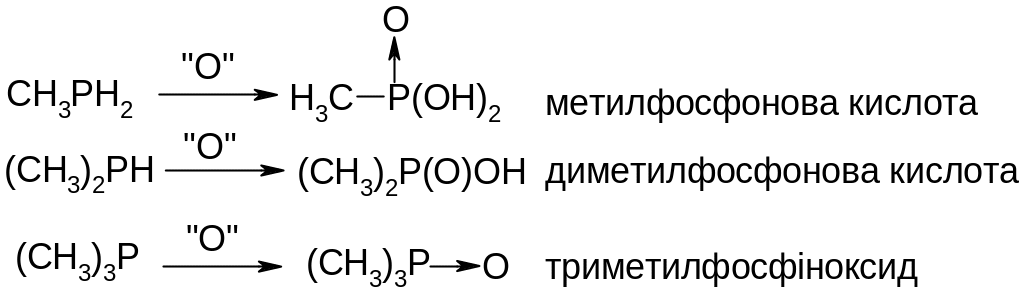
Перегрупування Арбузова:
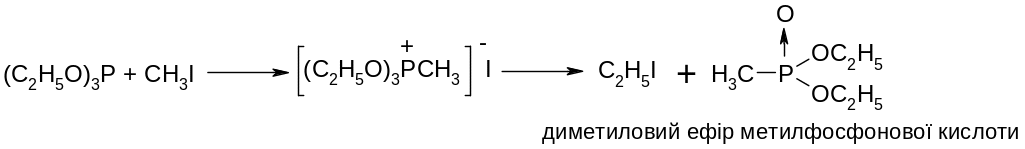
Свинецьорганічні сполуки
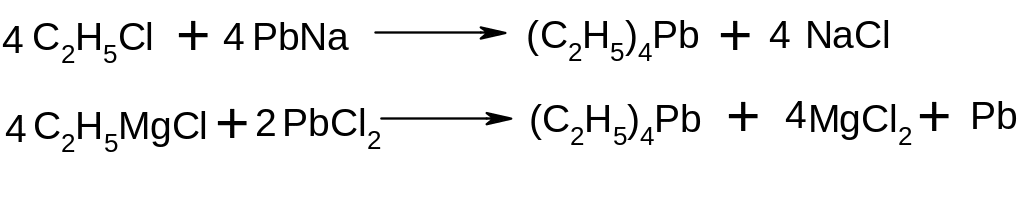
Галогенпохідні вуглеводнів Галогенпохідними називають сполуки, які містять зв’язки карбон-галоген. Поділяють на
Аліфатичні |
Ароматичні |
||
Насичені |
Ненасичені |
Галоген в ядрі |
Галоген в боковому ланцюзі |
алкілгалогеніди |
Вініл- та алілгалогеніди |
|
|
В свою чергу любий із типів галогенпохідних може мати 1, 2 і більше атомів галогену, тобто підрозділяють на моно-, ді-, три- і взагалі полігалогенпохідні. Галгенами можуть бути атоми F, Cl, Br, I.
Методи добування моногалогенпохідних
І. Галогенпохідні алканів.
Галогенування алканів(див. тему “Алкани”).
Приєднання галогеноводнів до алкенів (див. тему “Алкени”).
Заміщення гідроксильної групи (-ОН) в молекулах спиртів на галоген:
Взаємодія спиртів з галогеноводнями:
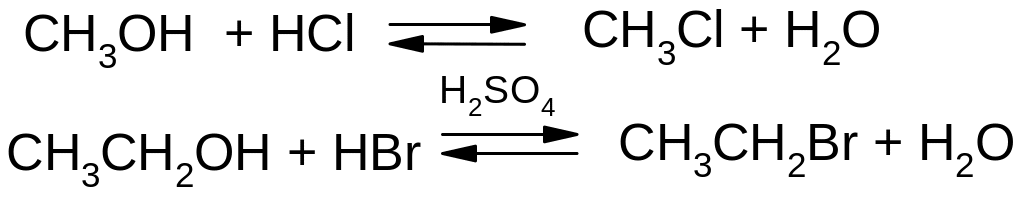
Взаємодія спиртів з галоїдними сполуками фосфору:
![]()
![]()
Взаємодія спиртів з хлористим тіонілом (SOCl2):
![]()
Обмін галогенів

ІІ. Галогенпохідні алкенів.
А. З атомами галогенів у подвійного зв’язку – вінілгалогеніди.
1. Приєднання галогенів до ацетиленових сполук (Дивись - Ацетилени)
Відщеплення галогеноводнів від гемінальних та віцинальних дигалогенідів
![]()
Б. Алілгалогеніди.
1. Алільне галогенування алкенів (Дивись - Алкени)
2. Приєднання галогеноводнів до супряжених дієнів (Дивись - Дієни)
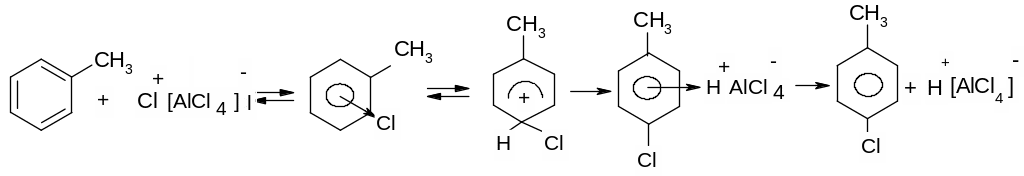
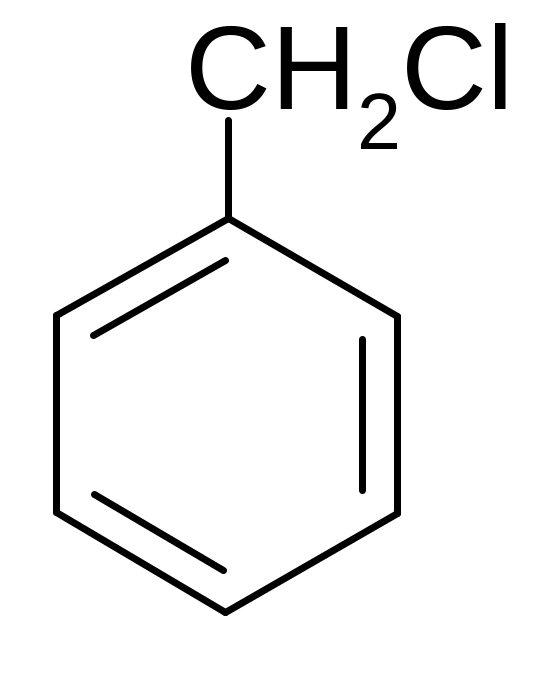
ІІІ. Галогенування бокового ланцюга алкілароматичних вуглеводнів.
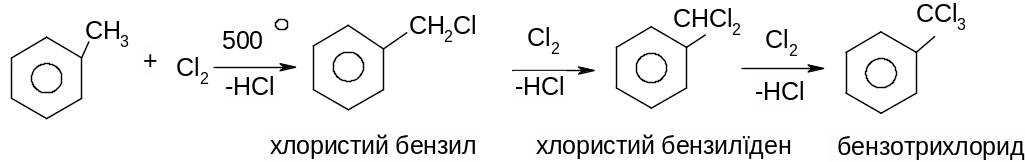
Механізм:
![]()
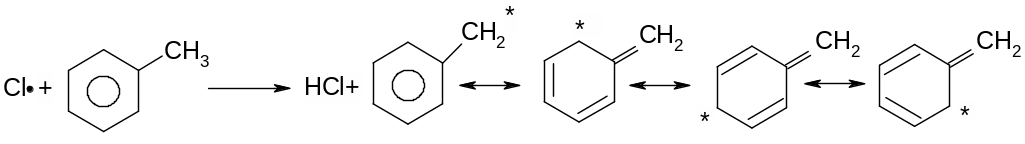
Оскільки бензильний радикал стійкіший за інші можливі за рахунок ефективної делокалізації неспареного електрону з-за супряження з ароматичним кільцем, галогенування любих алкілбензолів завжди проходить лише по α-атому вуглецю бокового ланцюга:
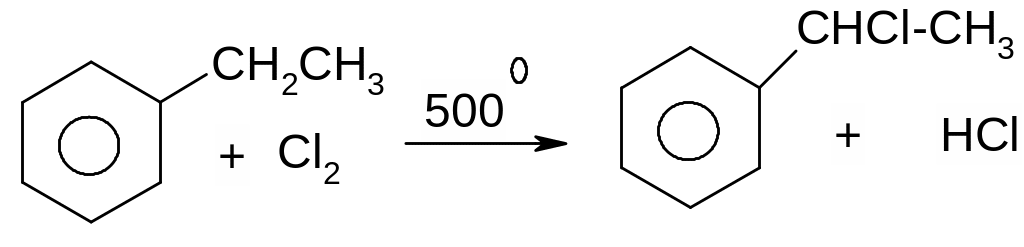
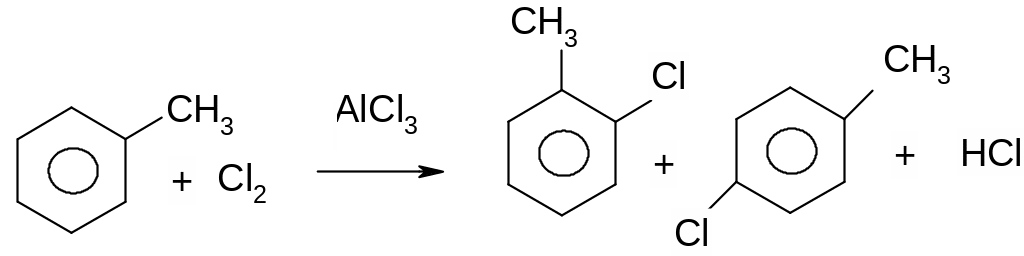
ІV. Галогенування ароматичних сполук в ядро.
Проходить лише каталітично: