
- •6.040204 – «Прикладна фізика»
- •6.040204 – «Прикладна фізика»
- •Вопросы и задачи
- •2.1 Краткое содержание
- •2.2. Вопросы и задачи
- •3.1. Краткое содержание
- •3. 2. Вопросы и задачи
- •4.1. Краткое содержание.
- •5. 1. Краткое содержание
- •6.1Краткое содержание
- •Методичні вказівки до практичних занять
- •«Молекулярна фізика»
- •6.040204 – «Прикладна фізика»
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
СХІДНОУКРАЇНСЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ
імені ВОЛОДИМИРА ДАЛЯ
МЕТОДИЧНІ ВКАЗІВКИ ДО ПРАКТИЧНИХ ЗАНЯТЬ
з дисципліни
«МОЛЕКУЛЯРНАЯ ФІЗИКА»
для студентів спеціальності
6.040204 – «Прикладна фізика»
частина 1
(електронне видання)
«До друку й у світ дозволяю»
Проректор ___________Ю.І. Осенін.
Протокол № 13 от 1.06.2010 г
Укладач ____________ Л.О. Єфіменко-Гарас
Увесь цифровий и фактичний матеріал,
Бібліографічні відомості перевірені.
Написання одиниць відповідає стандарту.
Луганськ, 2010
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
СХІДНОУКРАЇНСЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ
імені ВОЛОДИМИРА ДАЛЯ
МЕТОДИЧНІ ВКАЗІВКИ ДО ПРАКТИЧНИХ ЗАНЯТЬ
з дисципліни
«МОЛЕКУЛЯРНА ФІЗИКА»
для студентів спеціальності
6.040204 – «Прикладна фізика»
частина 1
(електронне видання)
ЗАТВЕРДЖЕНО
на засіданні кафедри
прикладної фізики
Протокол №13 від 01.69.2010 р.
Луганськ, 2009
УДК 539.19
Методичні вказівки до практичних зянять з дисципліни «Молекулярна фізика”» (для студентів спеціальності 6.040204 – «Прикладна фізика» / Ук.: Л.О. Єфіменко-Гарас - Луганськ: Вид. СНУ їм. В.Даля, 2010. - 30 с.
Методичні вказівки містять основний матеріал до практичних занять з дисципліни «Молекулярна фізика» (ч. 1, “Термодинаміка”). По кожній темі дається необхідний теоретичний матеріал, та відповідно підібрані питання та задачі. Наведено список необхідної літератури
Укладач Л.О. Єфіменко-Гарас, ст.в.
.
Від. за випуск Ю.А.Бранспіз, проф.
Рецензент С.Д. Кривоносов, доц.
Занятие 1
Тема: Основы молекулярно-кинетической теории. Идеальный газ
Краткое содержание
Все вещества состоят из атомов и молекул. Для измерения количества вещества вводится единица моль. В моле любого вещества содержится одинаковое число молекул (постоянная Авогадро).
Все молекулы находятся в непрерывном хаотическом движении, которое называется тепловым.
Количество вещества
![]() ,
или,
,
или,
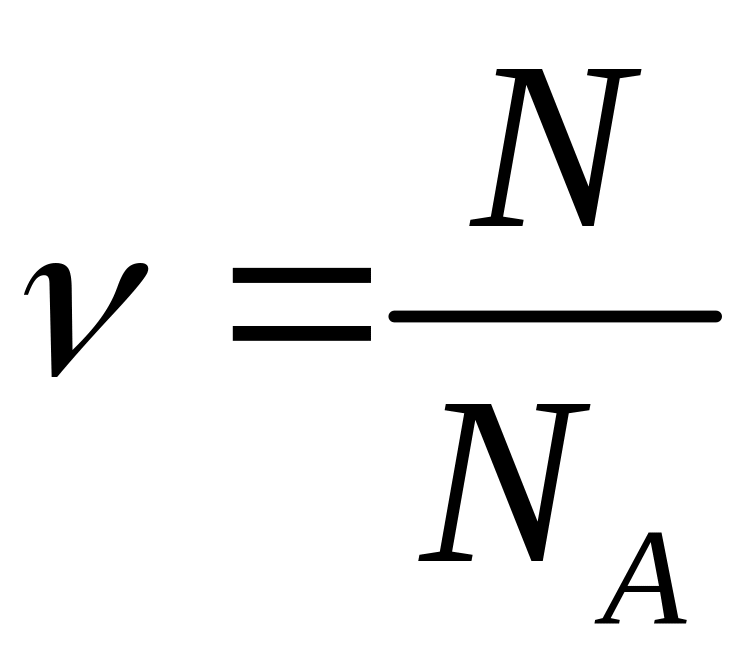 где
где
N - число структурных элементов системы, m - масса, M - молярная масса.
Число молекул однородной системы
![]() .
.
Концентрацию частиц (![]() )
можно вычислить, зная плотность вещества,
т. е.
)
можно вычислить, зная плотность вещества,
т. е.
![]() .
.
Сумма кинетической энергии хаотического движения молекул Wk и потенциальной энергии их взаимодействия Wp называется внутренней энергией тела U:
![]() .
.
Для идеального газа потенциальной энергией молекул пренебрегают.
Средняя кинетическая энергия, приходящаяся на одну степень свободы молекулы,
![]() ,
,
а приходящаяся на все степени свободы молекулы (полная энергия молекулы)
![]() ,
,
где k = 1,38·10-23 Дж/кг - постоянная Больцмана, T - термодинамическая температура, i - число степеней свободы молекулы.
Согласно молекулярно-кинетическим представлениям, давление газа на стенки сосуда возникает из-за ударов молекул о стенку. Основное уравнение молекулярно-кинетической теории связывает давление со средней кинетической энергией поступательного движения молекул
![]() ,
,
а так как
(в данном случае i = 3), то
![]()
Подставив сюда , получим уравнение состояния идеального газа
![]()
