
- •Углеводы.
- •Лабораторная работа №10. Моносахариды. Опыт №1: Качественная реакция на углеводы с α-нафтолом (реакция Молиша).
- •Опыт №3: Окисление моносахаридов аммиачным раствором гидроксида серебра (реакция ″серебряного зеркала″).
- •Лабораторная работа №11. Дисахариды. Опыт №1: Реакция дисахаридов с гидроксидом меди (II) в щелочной среде.
- •Лабораторная работа №12. Высшие полисахариды. Гидролиз крахмала.
- •Лабораторная работа №13. Выделение гликогена из печени.
- •Лабораторная работа №14. Жиры и масла. Опыт №1: Растворимость жиров и масел в органических растворителях.
- •Опыт №2: Определение непредельности растительного масла реакцией с бромной водой (под тягой).
- •Опыт №3: Взаимодействие растительного масла с водным раствором перманганата калия (реакция Вагнера).
- •Лабораторная работа №15 анализ и оценка пищевой ценности жиров.
- •Природные красители.
- •Хиноновые красители.
- •Некоторые n-гетероциклические соединения
- •Определение веществ - маркеров некоторых метаболических нарушений в организме.
Опыт №3: Окисление моносахаридов аммиачным раствором гидроксида серебра (реакция ″серебряного зеркала″).
Реактивы и оборудование: аммиачный раствор серебра, 1% раствор глюкозы, 1% раствор фруктозы; водяная баня, пипетки, пробирки.
Приготовление аммиачного раствора серебра.
К 1% раствору нитрата серебра при встряхивании по каплям прибавляют 5% раствор аммиака до тех пор, пока образовавшийся в начале осадок полностью не раствориться:
![]()
![]()

Ход работы: В двух чистых пробирках готовят по 2 мл аммиачного раствора серебра. В первую добавляют 1,5 мл 1% раствора глюкозы, во вторую 1,5 мл 1% фруктозы. Пробирки ставят на водяную баню при 70-80˚ С на 10-15 минут. Металлическое серебро выделяется и оседает на стенках обеих пробирок. Следует помнить, что при нагревании пробирки нельзя трогать и встряхивать, иначе серебро выпадет в виде черного осадка.
ОПЫТ №4: Реакция Селиванова на кетогексозы.
Реактивы и оборудование: 2% раствор глюкозы, 2% раствор фруктозы, насыщенный раствор меда, реактив Селиванова; водяная баня, пипетки, пробирки.
Приготовление реактива Селиванова:
50 мл концентрированной соляной кислоты смешивают с 50 мл воды, к полученному раствору добавляют 0,5 г резорцина.
Ход работы: В три пробирки наливают по 2 мл реактива Селиванова. В первую добавляют 3-4 капли 2% раствора фруктозы, во вторую столько же раствора меда, в третью – глюкозы. Пробирки ставят на водяную баню при 80˚ С на 5-10 минут. В пробирке с фруктозой появляется оранжевое, переходящее в розово-красное окрашивание. Раствор, содержащий глюкозу, не окрашивается. Так как натуральный мед состоит преимущественно из фруктозы, в пробирке с его раствором так же развивается розово-красное окрашивание. Этот опыт может служить проверкой натуральности меда.


Эта реакция позволяет различить альдозы и кетозы. При нагревании с соляной кислотой фруктоза (кетоза) превращается в оксиметилфурфурол, который вступает в реакцию конденсации с резорцином, в результате чего получается соединение окращенное в розово-красный цвет. Альдозы так же дают эту реакцию, но протекает она гораздо медленнее и при длительном кипячении.
Лабораторная работа №11. Дисахариды. Опыт №1: Реакция дисахаридов с гидроксидом меди (II) в щелочной среде.
Реактивы и оборудование: 1% раствор сахарозы, 1% раствор мальтозы (или лактозы), 10% раствор гидроксида натрия, 5% раствор сульфата меди (II); пипетки пробирки.
Ход работы: В одну пробирку наливают 1 мл 1% раствора сахарозы, во вторую – 1 мл 1% раствора мальтозы (лактозы). В обе пробирки добавляют по 1 мл 10% раствора гидроксида натрия. Растворы перемешивают, и в пробирки по каплям добавляют 5% раствор сульфата меди (II) до появления сине-голубого осадка гидроксида меди (II). Пробирки встряхивают. Осадок растворяется, а растворы приобретают светло-синюю окраску вследствие образования комплексных сахаратов меди (II):

мальтоза

ОПЫТ №2: Окисление дисахаридов реактивом Фелинга.
Реактивы и оборудование: 1% растворы мальтозы, лактозы и сахарозы, реактив Фелинга; спиртовки, пипетки, пробирки.
Ход работы: В три пробирки наливают по 1,5 мл 1% растворов мальтозы, лактозы и сахарозы. В каждую пробирку вносят по 1,5 мл фелинговой жидкости. Растворы перемешивают и нагревают их верхние части на спиртовках до начинающегося кипения. В пробирках с мальтозой и лактозой появляется красно-оранжевый осадок оксида меди (I).
Схема реакции окисления мальтозы реактивом Фелинга:

циклическая форма мальтозы

цепная форма мальтозы

мальтобионовая кислота
Положительную реакцию с реактивом Фелинга дают восстанавливающие дисахариды (мальтоза и лактоза), в водных растворах которых вследствие таутомерных переходов имеются свободные альдегидные группы. Сахароза же относится к не восстанавливающим дисахаридам не окисляется реактивом Фелинга.
Следует помнить, что длительное кипячение сахарозы в щелочной среде приводит ее расщеплению, а продукты гидролиза сахарозы восстанавливают реактив Фелинга до оксида меди (I).
Напишите уравнение реакции окисления лактозы реактивом Фелинга.
ОПЫТ №3: Гидролиз (инверсия) сахарозы.
Реактивы и оборудование: 1% раствор сахарозы, 10% раствор серной кислоты, реактив Фелинга, реактив Селиванова, 10% раствор гидроксида натрия; pH-метр или универсальная индикаторная бумага, спиртовки, водяная баня, фарфоровые кипятилки, пипетки, пробирки.
Ход работы: в пробирку наливают 3 мл 1% раствора сахарозы и 1 мл 10% раствора серной кислоты. Для равномерного кипения в пробирку помещают фарфоровые кипятилки. Содержимое пробирки кипятят 5 минут, а затем охлаждают. При кипячение раствора сахарозы в кислой среде происходит ее гидролитическое расщепление:
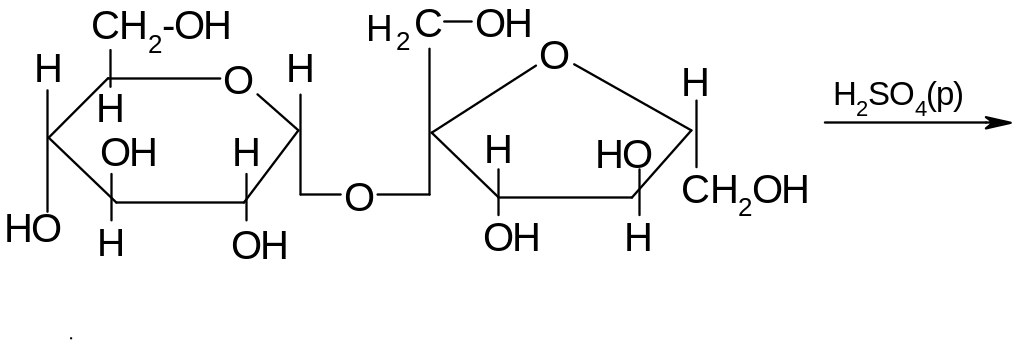
сахароза


D-глюкоза D-фруктоза
Для доказательства гидролитического расщепления сахарозы необходимо провести реакции, подтверждающие наличие в содержимом пробирки продуктов гидролиза. Для этого содержимое пробирки делят на две части. Первую часть раствора нейтрализуют 10% раствором гидроксида натрия (контроль по индикаторной бумаге или pH-метру), а затем добавляют равный объем фелинговой жидкости. Нагревают верхнюю часть раствора и наблюдают образование красного осадка оксида меди (I).
Во вторую пробирку добавляют 2 мл реактива Селиванова и нагревают на водяной бане при 80˚ С 5 –10 минут. Появляется розово-красное окрашивание. Параллельно проводят эти же реакции с исходным раствором сахарозы.
