

 O
O O
O
O
O O
O

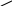
 C17H35-C
+ C-C ----
C17H35-C
+ CO + CO2
+HCl
C17H35-C
+ C-C ----
C17H35-C
+ CO + CO2
+HCl
OH Cl Cl Cl
Стеаринова кислота Оксалілхлорид Олеілхлорид
Хімічні властивості зумовлюються високою ацилювальною активністю галогенангідридів, завдяки чому їх використовують для одержання більшості функціональних похідних. Ацилгалогеніди дуже легко гідролізуються до карбонових кислот, тому їх зберігають без доступу навіть вологого повітря.
Найважливіші реакції ацилювання показані на схемі:
+Н2О O
 -------------------------
R-C
-------------------------
R-C
OH
Карбонова кислота
R1OH (чи R1ONa) O
------------------------ R-C
-HCl (чи NaCl) O-R1
Естер
O
+R1COONa R-C
 ------------------------
O
------------------------
O
-NaCl R1-C
 O
O
O
O
R-C ------- Ангідрид
Сl
Хлорангідрид +2NH3 O
----------------------- R-C
-NH4Cl NH2
Амід
+R1NH2 O
------------------------ R-C
-NCl NHR1
Зміщений амід
+С6H6(AlCl3)
------------------------
-HCl
Ароматично-аліфатичний кетон
Ацилювальна здатність галогенангідридів дозволяє одержувати естери третинних спиртів і фенолів, які не вступають у реакцію естеризації з карбоновими кислотами, наприклад
CH3
O O
 CH3-C
+ CH3-C-CH3
------
CH3-C
CH3
+ HCl
CH3-C
+ CH3-C-CH3
------
CH3-C
CH3
+ HCl
Cl
OH O-C-CH3
CH3
Ацетилхлорид Трет-бутловий Треттбутилацетат
спирт
------ + HBr
Бензоілбромід Фенол Фенілбензоат
Галогенангідриди можуть відновлюватися до спиртів (комплексними гідридами металів) чи до альдегідів (воднем на паладієвому каталізаторі):
[H] [H]
---------- --------------
LiAlH4 H2/Pd
Бензиловий Бензоілхлорид Бензальдегід
спирт
8.7.2 Ангідриди
Ангідридами називаються функціональні похідні карбонових кислот загального складу R-C(O)-O-(O)C-R1.
За складом ангідриди бувають таких типів:
симетричні, що містять залишки однієї карбонової кислоти:
СН3-С-О-С-СН3 Н-С-О-С-Н
О О О О
Оцтовий ангідрид Мурашиний ангідрид
Бензойний ангідрид
змішані, які складаються із залишків різних кислот, у тому числі й мінеральних%
O
 CH3-C-O-C-H
CH3-C
CH3-C-O-C-H
CH3-C
ONOH
O O
Мурашинооцтовий Ацетілнітрат Бензойнооцтовий ангідрид
ангідрид
циклічні, одержані внаслідок дегідратації дикарбонових кислот:
О О

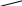
 С
С
С
С
СН Н2С
 О
О
О
О
СН Н2С
 С
С
С
С
О О
Малеіновий ангідрид Янтарний ангідрид
Способи одержання
дегідратація карбонових кислот (див. Параграф V.8.4)
ацилювання карбоксилатів, які в реакціях цього типу відіграють роль нуклеофілу:
O O O0C
СH3 – C + H-C ------- CH3-C-O-C-H + NaCl
Cl O-Na
O O
взаємодія галдогенацилів з оцтовим ангідридом:
O O
O CH3-C 1600C C15H31-C O
2C15H31-C + O --------- O + 2CH3-C
Cl CH3-C C15H31-C Cl
O O
Пальмітоілхлорид Оцтовий ангідрид Пальмітиновий
ангідрид
Хімічні властивості ангідридів нагадують галогенангідриди , але за ацилювальною здатністю уступають їм, тому реакції, як правило, протікають і умовах кислотного чи лужного каталіза. Розглянемо властивості ангідридів на прикладі оцтового ангідриду:
+ Н2О O
 ------------------
2CH3-C
------------------
2CH3-C
OH
Оцтова кислота
C2H5OH O
----------------- CH3-C + CH3COOH
O OC2H5
CH3-C Етилацетат
 О
-------------- 2NH3
O
О
-------------- 2NH3
O
CH3-C ----------------- CH3-C + CH3COONH4
O NH2
Ацетамід
(CH3)2NH O
----------------- CH3-C + CH3COOH
N(CH3)2
N,N-Диметилацетамід
