- •Тема №1 «Предмет, методи, завдання навчальної дисципліни»
- •Тема №3 «Фізичні основи динаміки. Закони збереження»
- •Тема №4 «Динаміка твердого тіла»
- •Тема №5 «Основні положення молекулярно-кінетичної теорії»
- •Тема №6 «Термодинаміка»
- •Проекти вічних двигунів першого роду.
- •Тема №7 «Фазові переходи. Явища переносу»
Тема №6 «Термодинаміка»
Перше начало термодинаміки.
Кількість теплоти.
Теплоємність. Теплоємність твердих тіл.
Закон Дюлонга-Пті.
Основи теорії Дебая.
Теплоємність газу.
Закон розподілу енергії за ступенями вільності.
Друге начало термодинаміки.
Призначення людини. Ентропія.
Третє начало термодинаміки.
Термодинаміка вивчає кількісні закономірності перетворення енергії в різних процесах (теплових, механічних, електричних, магнітних та ін.), зумовленого тепловим хаотичним рухом молекул.
Термодинаміка побудована на двох фундаментальних законах, які ще називають началами термодинаміки. Перше начало описує кількісну та якісну сторони процесів перетворення енергії, друге дозволяє судити про напрямок цих процесів.
Нехай деяка система, наприклад, газ у циліндрі під поршнем, характеризується внутрішньою енергією U1, отримала деяку кількість теплоти Q 5 і, перейшовши у новий стан з внутрішньою енергією U2, виконала зовнішню роботу А. Таким чином, зміна внутрішньої енергії системи дорівнює різниці теплоти, отриманої системою, і роботою, яку вона виконала:
![]() або
або ![]() . (6.1)
. (6.1)
У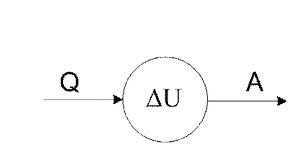 вівши
позначення
вівши
позначення
![]() ,
отримаємо вираз
,
отримаємо вираз
![]() . (6.2)
. (6.2)
Отримана формула є математичним записом першого начала термодинаміки, яке звучить так: вся кількість теплоти, передана системі, йде на зміну внутрішньої енергії системи і на виконувану системою роботу.
Перше начало термодинаміки було сформульоване лікарем і дослідником Юліусом Майєром у 1842-му, а потім, ясніше й чіткіше – німецьким фізиком, фізіологом і психологом Германом Гельмгольцем у 1847 році.
Отже, енергія не створюється і не зникає – вона просто видозмінюється. Перше начало термодинаміки можна ще назвати законом збереження і перетворення енергії.
Якщо в теплообміні беруть участь кілька тіл, то кількість теплоти, яку віддають більш нагріті тіла, повинна дорівнювати кількості теплоти, отриманої менш нагрітими тілами. Це положення називають рівнянням теплового балансу.
Кількість теплоти, передана тілу в процесі нагрівання, залежить від роду речовини, з якої складається тіло, від маси цього тіла і від зміни його температури. Кількість теплоти необхідна для нагрівання тіла масою 1 кг на 1оС, називають питомою теплоємністю. Питома теплоємність є табличною величиною. Питома теплоємність речовини у різних агрегатних станах (твердому, рідкому та газоподібному) є різною. Питома теплоємність позначається літерою с та вимірюється у Джоулях, поділених на кілограм-градус Цельсія.
Для тіла довільної маси існує така характеристика як теплоємність – кількість теплоти, потрібна для нагрівання даного тіла на 1оС. Для того щоб розрахувати, яка кількість теплоти потрібна для нагрівання тіла до певної температури, треба масу тіла помножити на питому теплоємність та на зміну температури, або теплоємність на зміну температури.
Якщо
система періодично повертається у
вихідний стан, то зміна її внутрішньої
енергії дорівнює нулю. Тоді
![]() .
Це означає, що неможливо створити
періодично діючий механізм, який би
виконував роботу, що перевищувала б
отриману ним енергію (вічний двигун
першого роду).
.
Це означає, що неможливо створити
періодично діючий механізм, який би
виконував роботу, що перевищувала б
отриману ним енергію (вічний двигун
першого роду).