
- •Предмет технической термодинамике и ее методы.
- •2.Основные понятия технической термодинамики. Характерные представители рабочих тел.
- •3.Термические параметры состояния состояние рабочего тела ( абсолютная температура, удельный объем, абсолютная давление)
- •4. Понятие идеального газа и реального газа. Уравнение состояния.
- •5 Теплота и работа как форма передачи энергии. Графическое определение теплоты и работы в координатах t-s, p-V.
- •7. Первый закон термодинамики в общем виде для закрытой термомеханической системы. Его аналитическое выражение и основные формулировки.
- •8. Первый закон термодинамики для изохорного , адиабатного и изотермического процессов.
- •9. Массовая объемная и мольная теплоемкость, взаимосвязь между ними.
- •10Зависимость теплоемкости от температуры. Определение средней теплоемкости идеальных газов.
- •11Зависимость теплоемкости от характера процесса. Уравнение Майера для идеального газа.
- •12. Основные определения и понятия газовой смеси. Теплоемкость смеси газов.
- •13. Общие свойства газовой смеси. Модификатор газовой смеси.
- •14. Сущность основные формулировки второго закона термодинамики и его аналитическое выражение.
- •15. Прямые и обратные циклы Карно, термический кпд и холодильный коэффициент циклов.
- •16 Понятие и физическая сущность энтропии.
- •17. Уравнение политропного процесса. Показатель поли тропы изохорного, изотермического, изобарного и адиабатного процессов, их уравнение.
- •19. Дать определение водяного пара в различных его состояниях.
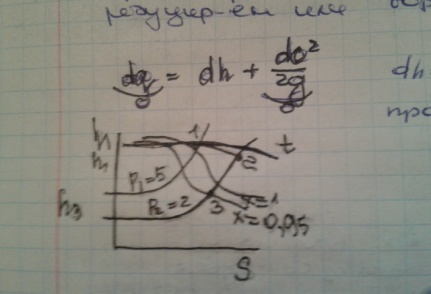
- •20. Диаграмма h-s процессы водяного пара.
- •21. Истечение газов и паров. Понятие о сопловом и диффузорном течении газа. Уравнение первого закона термодинамики для потока.
- •22. Дросселирование газов и паров, сущность процесса, процесс дросселирования в h-s диаграмме, практическое использование процесса дросселирования.
- •23. Основные положения теплопроводности, понятие изотермической поверхности, градиента температур. Основной закон теплопроводности- Закон Фурье.
- •24 . Теплопроводность при стационарном режиме. Теплопроводность однослойной и многослойной стенки. График изменения температур в однослойной и многослойной стенках.
- •25. Основы теории конвективного теплообмена. Физическая сущность конвективного теплообмена. Основной закон конвективного теплообмена.
- •26. Определения коэффициента теплоотдачи. Критерии подобия. Уравнение подобия для свободного движения теплоносителя в общем виде.
- •27 . Основы теории теплообмена излучением. Определение теплообмена излучением. Закон Стефана- Больцмана. Коэффициенты поглощения, отражения, пропускания.
- •28. Закон Стефана-Больцмана. Теплообмен излучением между двумя плоскими параллельными поверхностями. Приведенная степень чистоты системы тел.
- •29. Теплопередача. Понятия коэффициента теплопередачи, термического сопротивления теплопередачи, температурного напора. Уравнение теплопередачи.
- •30 Основы теплового расчета теплообменника с прямоточной и противоточной схемой движения носителя.
- •31 Характеристика топлива (высшая и низшая теплота сгорания, элементарный состав, выход летучих горючих).
- •32.Расход топлива для котельной предприятия. Влияние характеристик производимого пара на расход топлива. Условное топливо.
- •33. Назначение и классификация паровых котлов , используемых на предприятиях отрасли.
- •34. Устройство и принцип действия паровых котлов.
- •35. Назначение и принцип действия основных элементов парового котла.
- •36. Назначение и принцип действия вспомогательного оборудования котельной установки.
- •37. Тепловой баланс котельной установки. Составляющие уравнения теплового баланса.
- •38.Полезноиспользуемая теплота. Коэффициент полезного действия котла по прямому и обратному балансам.
- •39. Дать физическую интерпретацию потерь теплоты с уходящими газами и химическим недожогом.
- •40. Принципы обеспечения безопасности работы паровых котлов.
- •41. Схемы теплоснабжения предприятий отрасли. Основные теплоносители, используемые на предприятии, их характеристики.
- •42. Что такое холодильная техника и холодильная технология. Основы холодильной обработки и хранения продуктов.
- •43. Физические принципы получения низких температур.
- •49. Способы охлаждения камер хранения.
- •50. Характеристика и свойства холодильных агентов.
20. Диаграмма h-s процессы водяного пара.


диаграмма теплофизических свойств жидкости и газа (в основном воды и водяного пара), показывающая характер изменения различных свойств, в зависимости от параметров состояния. H, s-диаграммы чаще всего содержат в себе данные о свойствах воды в жидком и газообразном состояниях, так как они представляют наибольший интерес с точки зрения теплотехники.
Степень сухости - это параметр, показывающий массовую долю насыщенного пара в смеси воды и водяного пара. Значение x = 0 соответствует воде в момент кипения (насыщения). Критическая точка (К). При определённом, достаточно высоком давлении, называемом критическим, свойства воды и пара становятся идентичными. То есть исчезают физические различия между жидким и газообразным состояниями вещества. Такое состояние называют критическим состоянием вещества, которому соответствует положение критической точки. Следует заметить, что она на пограничной кривой лежит гораздо левее максимума этой кривой.
Изотерма - изолиния, построенная методом объединения точек по значениям энтальпии и энтропии, соответствующих определённой температуре. Изотермы пересекают пограничные кривые с изломом и, по мере удаления от верхней пограничной кривой, асимптотически приближаются к горизонтали. На схеме для упрощения представлены только три изотермы:t + Δt; t; t - Δt.
Изобара - изолиния, построенная методом объединения точек по значениям энтальпии и энтропии, соответствующих определённому давлению. Изобары не имеют изломов при пересечении пограничных кривых. На схеме представлены только три изобары:p + Δp; p; p - Δp.
Изохора - изолиния, построенная методом объединения точек по значениям энтальпии и энтропии, соответствующих определённому объёму. Изохоры на h, s-диаграмме в области перегретого пара, всегда проходит круче, чем изобары, и это облегчает их распознавание на одноцветных диаграммах. Построение изохор требует более кропотливой работы с таблицей состояний. На схеме представлены только три изохоры:v - Δv; v; v + Δv.
Изотермы и изобары в области влажного пара совпадают по причине линейной зависимости в состоянии насыщения.
21. Истечение газов и паров. Понятие о сопловом и диффузорном течении газа. Уравнение первого закона термодинамики для потока.
Процесс истечения- процесс перетекания газа из области одних давлений в обл. других. Канал, в кот.с уменьшением давления скорость газ-го потока возрастает-сопло. Канал, в кот.скорость газа уменьшается, а давление возрастает- диффузор.
q=h2-h1+
22. Дросселирование газов и паров, сущность процесса, процесс дросселирования в h-s диаграмме, практическое использование процесса дросселирования.
Если в трубопроводе, на пути к движению газа или пара встречается сужения проходного сечения, то вследствие сопротивления возникающих при таком сужении,Ргаза или пара за местом сужения, всегда Р газа или пара меньше чем перед сужением. Это яв-е при котором пар или газ переходит с высокого давления на низкое без совершения работы и без теплообмена с окр.средой- дросселирование.
dh=const,процесс изоэнтальпийный.
Процесс дросселир-я яв-ся необратимым процессом,протекающим с увеличением энтропии и снижением работоспособ-ти раб.тела. тем не менее он находит применение в практике и создается искусственно в холодильных установках для понижения темпер-ры, в приборах, измеряющих расход газа, в установках, сжижающих газ и др.
