
- •Введение
- •1 Подбор методики определения выбранного компонента. Анализ основных групп методов исследования для решения поставленной задачи
- •1.1 Трилонометрическое определение магния в воде
- •1.2 Атомно-абсорбционный метод определения ионов магния
- •1.3 Классический весовой метод
- •1.4 Метод определения магния комплексонометрическим титрованием
- •2 Выбор метода
- •3 Методика выполнения определения содержания магния комплексонометрическим титрованием
- •3.1 Описание методики
- •3.2 Аналитические расчеты
- •3.3 Маркировка используемых реагентов
- •3.4 Устранение мешающих влияний
- •Составление плана проведения эксперимента
- •Построение матрицы планирования
- •Составление математической модели техногенного риска по исследуемому компоненту
- •7 Техника безопасности при проведении экспериментальных работ в химических лабораториях
- •8 Обработка результатов эксперимента, в соответствии с теорией оценки погрешностей
- •Перечень используемой литературы
7 Техника безопасности при проведении экспериментальных работ в химических лабораториях
1.При всех экспериментальных работах в химической лаборатории соблюдать максимальную осторожность, помня, что несчастный случай происходит вследствие небрежности, невнимательности, знакомства с приборами, аппаратами и свойствами с которыми производится работа.
2.Для каждой проводимой реакции брать определенное количество определенной концентрации вещества, предусмотренную для этого посуду строго соблюдать условия опыта.
3.Категорически запрещается определять свойства вещества пробой на вкус или вдыханием их паров, помня, что 3/4 всех применяемых веществ ядовиты.
4. Работа с нагреванием на рабочих столах кислот, аммиачных жидкостей, процессов с выделением сероводорода, хлора, брома и т. д. запрещается.
5.Все пролитое, просыпанное и разбитое должно быть немедленно убрано.
6.Остатки взрывоопасных, огнеопасных и ядовитых веществ запрещается выбрасывать в мусорные ящики, выливать в раковину. Их необходимо собирать в специальные отдельные емкости, которые находятся в вытяжном шкафу. а после работы выносятся для хранения в специальные помещения.
7.После окончания опыта обязательно промыть посуду и убрать рабочее место. Никаких опытов в грязной посуде не проводить.
8.Тщательно готовить рабочее место до начала работы: убрать ненужные химреактивы, пустую посуду, ненужные приборы, приспособления, навести чистоту.
9.Подступы к пожарному инвентарю, электрощиту, раковине, выходу из помещения и проходам между столами и оборудованием, не должны за- громождаться.
ПОМНИТЕ! Стесненность и загромождение проходов приводят к лишним проблемам во время чрезвычайных происшествий и ликвидации последствий.
10.Запрещается при проведении сложных химических работ, связанных с возможностью пожара, взрыва, загазованностью и т. д. оставаться в лаборатории одному. В отдельных случаях работа в одиночку может быть допущена с разрешения администрации.
11. В случае прекращения работы вентиляции всякие работы, связанные с выделением паров и газов должны быть немедленно прекращены.
12. Необходимо соблюдать определённую осторожность при переливании опасных жидкостей с использованием воронки. Необходимо помнить, что может, произойти выброс из сосуда под воздействием скопившегося воздуха или паров.
13.Для работ под вакуумом или повышенном давлении применять только проверенную толстостенную специализированную посуду.
8 Обработка результатов эксперимента, в соответствии с теорией оценки погрешностей
Погрешность приборов
Пипетка мерная на 50 мл. [ГОСТ 2029274] – погрешность 1%, второй класс точности.
Δ = 1% – относительная ошибка
Пипетка градуированная на полный слив вместимостью 10 мл. [ГОСТ 2922891] – погрешность ±0,1 мл., первый класс точности.
Δ
= 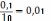 %
– относительная ошибка
%
– относительная ошибка
Бюретка на 25 мл. [ГОСТ 2925191] – погрешность ±0,2 мл. , второй класс точности.
Δ
= 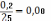 %
– относительная ошибка
%
– относительная ошибка
Цилиндр мерный с пластиковым основанием на 100мл. [ГОСТ 177074] – погрешность ±1 мл. , второй класс точности.
Δ = % – относительная ошибка
Колба коническая для титрования на 250 мл.
Δ = 7,14% – ошибка проведения эксперимента
Погрешность расчетов
1 серия:
∆11 = 8,8 - 8,75 = 0,05
δ11
=
 = 0,57 %
= 0,57 %
∆12 = 8,5 - 8,45 = 0,05
δ12
=
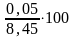 = 0,59 %
= 0,59 %
∆13 = 8,4 - 8,35 = 0,05
δ13
=
 = 0,6 %
= 0,6 %
∆14 = 8,7 - 8,65 = 0,05
δ14
=
 = 0,58 %
= 0,58 %
2 серия:
∆21 = ׀8,7 – 8,75׀ = 0,05
∆21 = = 0,57 %
∆22 = ׀8,4 – 8,45׀ = 0,05
∆22 = = 0,59 %
∆23 = ׀8,3 – 8,35׀ = 0,05
∆23 = = 0,6 %
∆24 = ׀8,6 – 8,65׀ = 0,05
∆24 = = 0,58 %
ВЫВОДЫ
В данной научно-исследовательской работе было проведено определение ионов магния в питьевой воде методом комплексонометрического титрования. Выбор этого метода обусловлен точностью, простотой, материальной базой лаборатории. Исследовано влияние мешающих факторов. Выведено зависимость от значений мешающих факторов:
рН и температура не оказывают влияния на изменение содержания магния в питьевой воде.
В ходе работы были рассчитаны основные виды погрешностей и их значения также повлияли на результаты эксперимента.
Рассмотрена техника безопасности при выполнении работы с выбранными реактивами. Выполнена маркировка соответствующих реактивов.
