
- •Введение
- •1 Подбор методики определения выбранного компонента. Анализ основных групп методов исследования для решения поставленной задачи
- •1.1 Трилонометрическое определение магния в воде
- •1.2 Атомно-абсорбционный метод определения ионов магния
- •1.3 Классический весовой метод
- •1.4 Метод определения магния комплексонометрическим титрованием
- •2 Выбор метода
- •3 Методика выполнения определения содержания магния комплексонометрическим титрованием
- •3.1 Описание методики
- •3.2 Аналитические расчеты
- •3.3 Маркировка используемых реагентов
- •3.4 Устранение мешающих влияний
- •Составление плана проведения эксперимента
- •Построение матрицы планирования
- •Составление математической модели техногенного риска по исследуемому компоненту
- •7 Техника безопасности при проведении экспериментальных работ в химических лабораториях
- •8 Обработка результатов эксперимента, в соответствии с теорией оценки погрешностей
- •Перечень используемой литературы
3.2 Аналитические расчеты
Содержание ионов магния в воде рассчитывают по формуле (2):
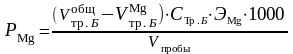 ,
мг/л (2)
,
мг/л (2)
где
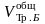
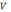 – объем трилона Б, затраченного на
титрование при определении общей
жесткости;
– объем трилона Б, затраченного на
титрование при определении общей
жесткости;
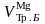 – объем
трилона Б, затраченного на титрование
при определении содержания магния;
– объем
трилона Б, затраченного на титрование
при определении содержания магния;
СТр.Б – нормальность раствора трилона Б;
ЭMg – эквивалент магния
Обьемы трилона Б, затраченного на титрование пробы (для Mg 2+):
 1=8,8
мл
1=8,8
мл
 2=8,5
мл
2=8,5
мл
 3=8,4
мл
3=8,4
мл
 4=8,7
мл
4=8,7
мл
Вычисляем эквивалент магния:
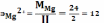 мг-экв.
мг-экв.
Определяем содержание магния в воде по формуле (2):
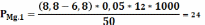 мг/л.
мг/л.
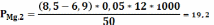 мг/л.
мг/л.
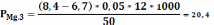 мг/л.
мг/л.
 мг/л.
мг/л.
Таблица 1 – результаты статистической обработки
№ |
PMg |
P̄Mg |
(PMg- P̄Mg)2 |
S |
Sc̄ |
|
Δ |
1 |
24,00 |
21,20
|
7,84 |
9,51 |
4,76 |
15,146 |
7,14 |
2 |
19,29 |
4,00 |
|||||
3 |
20,40 |
0,64 |
|||||
4 |
22,80 |
2,56 |
1. Находим стандартное отклонение S, характеризующее рассеяние отдельных измеряемых значений или результатов относительно среднего значения P̄Mg .
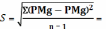 9,51
9,51
2.Находим стандартное отклонение среднего результата.

n=4
Вычисляем доверительный интервал .
Таблица 2 – Коэффициенты нормированных отклонений (коэффициенты Стьюдента) при доверительной вероятности Р=0,95
Число степеней свободы f |
tP,f |
Число степеней свободы f |
tP,f |
1 |
12,706 |
6 |
2,447 |
2 |
4,303 |
7 |
2,365 |
3 |
3,182 |
8 |
2,306 |
4 |
2,776 |
9 |
2,262 |
5 |
2,571 |
10 |
2,228 |
Из таблицы 2
tp,s = 3,182
– критерий Стьюдента при заданной доверительной вероятности р=0,95 и числе степеней свободы f=n-1. n=4,тогда f=3.
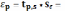 15,146
15,146
Рассчитываем относительную ошибку анализа.
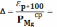 7,14%
7,14%
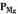 =21,200
± 15,146 мг/л.
=21,200
± 15,146 мг/л.
3.3 Маркировка используемых реагентов

«ч» – чистый, содержание основного компонента более 90%.
Физические свойства: представляет собой белый кристаллический порошок или кристаллы белого цвета.
Тпл= 1100С, Тразл.= 255°С.Растворим в воде при Т=200С.Токсичен. ПДК в воздухе рабочей зоны 2 мг/м3 .
Применение: применяется в производстве синтетических моющих средств, в целлюлозно-бумажной промышленности и производстве каучука - как стабилизатор в процессах полимеризации. В аналитической химии Трилон Б используется в качестве маскирующего агента. Элюат в ионообменной хромотографии.
[ГОСТ 10652] – относится ко 3-му классу опасности.
«чда» – чистый для анализа, содержание основного компонента более 99%.
Физические свойства: Гидрат окиси натрия NaOH - белое твердое вещество. Если оставить кусок едкого натра на воздухе, то он вскоре расплывается, так как притягивает влагу из воздуха. Едкий натр хорошо растворяется в воде, при этом выделяется большое количество теплоты. Раствор едкого натра мылок на ощупь.
Тпл= 65,1 °C,ρ= 1,829 г/см³. ПДК 0,5 мг/м³.
Применение: Гидроксид натрия применяют в химической, косметической, бумажной, нефтеперерабатывающей промышленности, для ликвидации засоров в канализационных трубах в составе специального геля.
[ ГОСТ
4328-77] – 2-й класс опасности.
– 2-й класс опасности.

Физические свойства: Удельная электропроводность дистиллированной воды, как правило, менее 5 мкСм/см. Молекулярная масса 18,01. Диэлектрическая проницаемость 4.0 – 4.3. Будучи очень чистой, в отсутствие посторонних механических включений может быть перегрета выше точки кипения, или переохлаждена ниже точки замерзания без осуществления фазового перехода. Фазовый переход интенсивно происходит при введении механических примесей или встряхивании.
[ГОСТ 6709-72]

 p
p