
Основні операції гравіметричного аналізу.
Взяту наважку переносять у хімічний стакан і розчиняють, використовуючи як розчинник воду, кислоту або луг. Розчинник звичайно беруть у такій кількості, щоб концентрація отриманого розчину була 0,5 - 1%. У методиці аналізу вказані кількість розчинника та умови розчинення.
Щоб прискорити розчинених, вміст склянки підігрівають і перемішують скляною паличкою. При цьому потрібно стежити, щоб жодна крапля розчину не була втрачена, - це призведе до помилки в аналізі.
Осадження. Осадження - одна з найважливіших операцій гравіметричного аналізу. Мета її - перевести обумовлену частину аналізованого речовини в хімічну сполуку, зручну для визначення ваговим способом. Наприклад, барій в хлориді барію визначають у формі сульфату барію, який осаджують з водного розчину хлориду барію додаванням сірчаної кислоти:
ВаС12 + Н2SO4 = ВаSO4 ↓ + 2НС1
Алюміній з розчинів його солей осаджують додаванням оцтовокислого розчину 8-оксихіноліну. У осад випадає оксіхінолінат алюмінію:
А13+ + ЗС9Н6N (OН) = А1(С9Н6NO)3↓+ 3H+
При цьому необхідно, щоб осадження відбувалося кількісно, тобто визначаємий іон повністю переходив в осад.
Для цього обрана осаджувана форма, тобто з'єднання, яке осаджується з розчину, повинно володіти дуже малою розчинністю. Для кількісного аналізу вибирають сполуки, добуток розчинності яких не перевищує 1·10-8. Виходячи з цього підбирають реактиви для осадження. Відомо, що при осадженні підвищення концентрації одного з іонів, що утворять осад, приводить до пониження концентрації другого іона. Тому при осадженні беруть надлишок розчину осаджувача (в наведених вище прикладах - сірчаної кислоти або 8-оксихіноліну).
Осадження ведуть, доливаючи розчин осаджувача в склянку з розчином аналізованого речовини при безперервному перемішуванні скляною паличкою. Повноту осадження перевіряють після відстоювання осаду і утворення над ним прозорого розчину. До нього обережно додають декілька крапель розчину осаджувача-відсутність помутніння вказує на повноту осадження.
Для подальшого аналізу велике значення має структура осаду, який утворився. Дуже зручні крупнокристалічні осади: вони швидко фільтруються, легко промиваються від домішок. Дрібнокристалічні і аморфні осади гірше фільтруються і промиваються, а іноді проходять через пори фільтра.
Для отримання добре фільтрованих кристалічних осадів слід дотримуватися таких правил:
вести осадження з гарячого розведеного розчину гарячим розведеним розчином осаджувача;
додавати осаджувач дуже повільно, а на початку осадження - по краплині;
безперервно перемішувати розчин скляною паличкою; відфільтровувати осад тільки після повного охолодження розчину.
Слід зазначити, що якщо в кристалічному осаді присутні повільно осідаючи дрібні кристалики, то при стоянні вони укрупнюються - осад дозріває. Тому після осадження доцільно витримати розчин з випали з нього кристалічним осадом в теплі протягом декількох годин, а потім вже повільно охолодити і відфільтрувати.
Деякі сполуки, наприклад гідроксид заліза або алюмінію, осідають тільки у вигляді аморфних опадів. У цьому випадку більш щільні і осади, що легше фільтруються, отримують при дотримуванні наступних умов:
ведуть осадження з концентрованих гарячих розчинів концентрованими розчинами осаджувача;
швидко додають розчин осаджувача;
ведуть осадження в присутності електролітів, сприяють коагуляції колоїдних частинок.
Аморфні осади на відміну від кристалічних не витримують після осадження, а зараз же переносять на фільтр, фільтрують та промивають.
Фільтрування. Мета операції - відділення осаду від розчину, з якого він випав (маточного розчину).
Для фільтрування в гравіметричного аналізу використовують беззольні паперові фільтри (рис.3). Ці фільтри при згорянні утворюють так мало золи, що цією масою можна знехтувати. В залежності від характеру осаду використовують беззольні фільтри різних марок. Їх розрізняють за кольором стрічки на упаковці фільтру. Найщільніші (тобто з найменшим розміром пор)-з синьою стрічкою,, фільтри середньої щільності-з білою стрічкою, найменш щільні, швидко фільтруючі - з червоною стрічкою.

Рис.3. Беззольні паперові фільтри.
Паперовий фільтр поміщають в скляну воронку. Для цього круглий фільтр складають навпіл по діаметрі, потім знову пополам і вкладають в суху лійку. Потім наповнюють фільтр дистильованою водою і щільно притискають до вирви. Фільтр і воронку вибирають з таким розрахунком, щоб осад займав не більше половини фільтра - інакше важко добре промити осад. Край паперового фільтра повинен на 10-15 мм не доходити до краю воронки. Воронку поміщають в кільце, укріплене на штативі. Під воронку поміщають склянку таким чином, щоб скошений кінець носика воронки стосувався стінки склянки.
Фільтрацію ведуть, декантуючи рідину: зливають на фільтр по скляній паличці відстояну рідину, не взмучиючи осад. Коли майже весь розчин злитий, додають 50-70 мл промивної рідини, перемішують осад, дають йому відстоятися і знову декантують. Декантації повторюють два-три рази і, нарешті, зливають на фільтр рідину разом з осадом. Стакан споліскують два-три рази маленькими порціями промивної рідини і зливають на фільтр. Промивну рідину зручно подавати з промивалки (рис. 4), при цьому слід добре обполіскувати стінки склянки промивної рідиною. Потім обполіскують скляну паличку, по якій зливали осад. При цьому недопустима втрата частинок осаду - він має бути перенесений на фільтр кількісно.
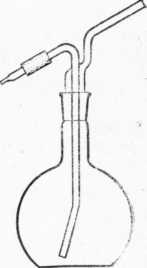
Рис.4. Скляна промивалка з пришліфованою пробкою.
Фільтрацію продовжують до тих пір, поки з носика воронки не перестануть стікати краплі рідини. Після цього приступають до остаточної промивки осаду. Струменем рідини з промивалки обполіскують верхній край фільтра, змиваючи осад в нижню частину фільтра.
Основне правило фільтрації і промивки: наливати на фільтр нову порцію рідини тільки після того, як повністю отфільтровалась попередня.
Для промивання використовують або дистиляційну воду, або воду з невеликою кількістю осаджувача. Промивку ведуть для видалення з осаду залишків маточного розчину.
По закінченні роблять пробу на повноту промивки, тобто на відсутність в рідини, що стікає з воронки, речовини, що відмивається. Наприклад, для перевірки на повноту відмивання сульфат-іонів до декількох крапель рідини, що стікає з воронки, додають краплю розчину хлориду барію. Відсутність помутніння вказує на закінчення промивки. Далі воронку з осадом накривають аркушем фільтрувального паперу, змоченою дистильованою водою, щільно притискають папір до країв воронки і поміщають у сушильну шафу. Після підсушування фільтр з осадом кількісно переносять в прожарений і зважений фарфоровий тигель.

Рис.5. Фільтруючий тигель. 1 – тигель; 2 – крупний фільтр.
Якщо аналіз закінчується не прожаренням, а висушуванням осаду (як, наприклад, при визначенні алюмінію у формі 8-окси-хіноліната), то фільтрування зручно вести через скляні фільтруючі тиглі з пористими скляними пластинками (рис. 5). Такий тигель ретельно промивають соляною кислотою і водою, висушують в сушильній шафі до постійної маси. Фільтрацію через тигель ведуть за допомогою водоструминного насоса через відсмоктувати колбу. Тигель вставляють у колбу, включають насос і ведуть фільтрацію декантацією і промиванням, як описано вище. По закінченні фільтрування та промивання фільтруючий тигель з осадом розміщують у сушильній шафі та висушують до сталої маси.
Прожарювання осаду. Після фільтрації і промивки на фільтрі знаходиться чистий осад. Щоб дізнатися його масу, в більшості випадків фільтр спалюють, а осад підсушують і прожарюють.
Слід мати на увазі, що при прожарюванні склад осаду може змінитися і так звана вагова форма обумовленої частини речовин не збігається з осаджується формою. Наприклад, при гравіметричному визначенні заліза іони заліза (III) осаджують у формі гідроксида:
Fе3 + + ЗОН- = Fе(ОН)3↓
Гідроксид заліза (III) відфільтровують, осад підсушують і прожарюють при температурі 900 ° С. При прожарюванні гідроксид заліза (III) відщеплює воду і перетворюється на оксид заліза (III):
2Fе(OН)3 = Fе2O3 + ЗН2O
Тут осаджувана форма - гідроксид заліза (III), вагова форма - оксид заліза (III).
При гравіметричному визначенні барію його осаджують з водного розчину у формі сульфату: Ва2+ + SO42- = ВаSO4. Осад підсушують і прожарюють при температурі 800-900 ° С. Тут осіджувана і вагова форми - сульфат барію - збігаються.
Прожарювання ведуть в порцелянових тиглях. Тигель попередньо прожарюють до постійної маси в тих же умовах, в яких буде прожарюватися осад. Цю операцію потрібно провести завчасно, щоб підсушений осад можна було відразу перенести в тигель.
Фільтр з підсушеним осадом обережно відокремлюють від воронки, скляним шпателем обережно загинають края фільтру, так щоб осад опинився всередині фільтра, і переносять у тигель. Якщо на воронці залишилися частинки осаду, їх переносять у тигель з допомогою шматочка беззольного фільтра. Всю операцію зручно виконувати над шматком глянсуватого паперу. Просипані частинки осаду струшують з паперу в тигель.
Тигель з осадом поміщають у спеціальний фарфоровий трикутник, покладений на кільце штатива, і газовим пальником нагрівають тигель таким чином, щоб фільтр поступово обвуглився. Тигель з обвугленими фільтром і осадом поміщають у муфельну піч, відрегульовану на задану температуру, і прожарюють протягом 2 г. Потім тигельними щипцями виймають тигель і ставлять його в ексикатор, який захищає вміст тигля від вологи повітря. У ексикаторі тигель поступово охолоджується до кімнатної температури.
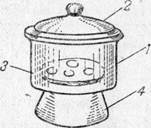
Рис.6. Ексикатор.
1-банку, 2-притерта кришка,
3-решітка для укладання наважок,
4-резервуар для сірчаної кислоти.
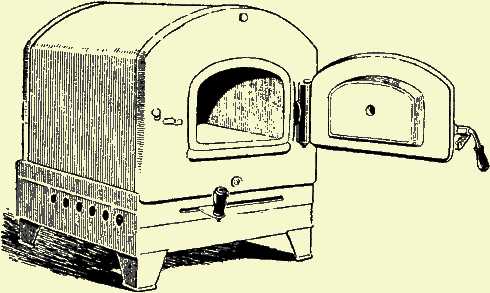
Рис.7. Муфельна піч.
Його зважують, потім знову ставлять в муфель, прожарюють ще 20-30 хв, охолоджують і зважують. Якщо маса при двох послідовних зважуваннях розрізняється не більше ніж на 0,0002 г, прожарювання закінчено. Осад прожарений до постійної маси.
У деяких випадках перед прожарюванням осад відокремлюють від фільтра, останній обзолюють в тиглі, а потім в тигель поміщають осад і ведуть прожарювання, як описано вище. Це необхідно робити, коли в осаді містяться речовини, здатні відновлюватися вуглецем, - окислювачі, з'єднання благородних металів і деякі інші.
