
- •Предмет, задачи, методы и место биохимии среди других медицинских и биологических дисциплин.
- •2.Роль белков в жизнедеятельности организма. Современные представления о структуре белков
- •3.Общая характеристика биологических функций белков (каталитическая, регуляторная, рецепторная, транспортная, структурная, сократительная, генно-регуляторная, трофическая, иммунологическая и т.Д.)
- •6.Принципы организации четвертичной структуры белков. Кооперативные изменения конформации субъединиц. Примеры реализации кооперативных эффектов.
- •7. Денатурация белков. Ренатурация. Факторы.
- •8. Методы выделения и очистки белков
- •9. Физико-химические свойства белков:масса,размеры и форма молекул;растворимость,ионизация,гидратация.Методы исследования белков(качественные и количественные)
- •1. Различия белков по форме молекул
- •2. Различия белков по молекулярной массе
- •3. Суммарный заряд белков
- •4. Соотношение полярных и неполярных
- •5. Растворимость белков
- •10. Структурные компоненты и биологические функции сложных белков(хромопротеины,гемопротеины,флавопротеины,металлопротеины) хромопротеины
- •11. Причины и следствия различного белкового состава органов и тканей. Изменение белкового состава организма при старении и заболеваниях
- •12.Понятие о ферментах. Структурно-функциональная организация ферментов. Отличие ферментативного катализа от неорганического
- •13. Общие принципы ферментативного катализа. Отличие ферментов от неорганических катализаторов. Механизм односубстратной и двусубстратной ферментативной реакции
- •2) Двусубстратные с неупорядоченным механизмом
- •14. Кофакторы и коферменты,их значение для деятельности ферментов. Коферментные функции витаминов.
- •15. Механизм действия ферментов. Специфичность действия ферментов(стереохимическая, реакционная и субстратная:абсолютная,групповая). Структура и роль каталитического центра.
- •16. Классификация ферментов Классификация и номенклатура ферментов
- •Номенклатура ферментов
- •17. Кинетика ферментативных реакций. Зависимость скорости ферментативных реакций от концентрации субстрата,фермента,факторов среды(рН,температуры). Уравнение Михаэлиса- Ментен
- •18. Ингибирование активности ферментов: обратимое и необратимое;конкурентное,неконкурентное и бесконкурентное. Лекарственные препараты- ингибиторы ферментов.
- •20.Методы определения и единицы активности и количества фермента. Понятие об энзимопатологии, энзимодиагностике и энзимотерапии.
Номенклатура ферментов
1) Существует тривиальная номенклатура – названия случайные, без системы и основания, например трипсин, пепсин, химотрипсин.
2) Рабочая номенклатура – название фермента составляется из названия субстрата или продукта реакции, типа катализируемой реакции и окончание –аза, например лактатдегирогеназа.
3) Систематическая, научная - L-лактат-НАД-оксидредуктаза.
4) Все ферменты имеют цифровой шифр, например ЛДГ - 1.1.1.27.
Первая цифра говорит о типе катализируемой реакции, указывая на номер класса.
Вторая уточняет действие фермента – номер подкласса.
Третья указывает природу разрываемой связи в молекуле субстрата - подподкласс.
Четвёртая – порядковый номер фермента.
17. Кинетика ферментативных реакций. Зависимость скорости ферментативных реакций от концентрации субстрата,фермента,факторов среды(рН,температуры). Уравнение Михаэлиса- Ментен
Кинетика ферментативных реакций. Этот раздел энзимологии изучает влияние химических и физических факторов на скорость ферментативной реакции. В 1913 г. Михаэлис и Ментен создали теорию ферментативной кинетики, исходя из того, что фермент (Е) вступает во взаимодействие с субстратом (S) с образованием промежуточного фермент субстратного комплекса (ЕS), который далее распадается на фермент и продукт реакции по уравнению:

Каждый этап взаимодействия субстрата с ферментом характеризуется своими константами скорости. Отношение суммы констант скорости распада ферментсубстратного комплекса к константе скорости образования ферментсубстратного комплекса называется константой Михаелиса (Кm). Она определят сродство фермента к субстрату. Чем ниже константа Михаелиса, тем выше сродство фермента к субстрату, тем выше скорость ка тализируемой им реакции. По величине Кm каталитические реакции можно поделить на быстрые (Кm 106 моль/л и меньше) и медленные ( Кm 102 до 106).
Зависимость скорости ферментативной реакции от концентрации субстрата
Число молекул субстрата, претерпивающих изменение в течение минуты, в расчете на единицу веса фермента при оптимальных условиях его действия называется молекулярной активностью фермента. При увеличении количества ферментов скорость ферментативной реакции повышается до некоторого предела, который характеризуется количеством субстрата, доступным действию фермента. В то же время, при постоянной концентрации фермента увеличение количества субстрата приводит вначале к быстрому, затем к более медленному росту скорости ферментативной реакции, пока не достигается максимальная скорость, остающаяся практически неизменной при дальнейшем увеличении концентрации субстрата.
Зависимость скорости ферментативной реакции от концентрации субстрата может быть описана уравнением:
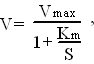
где V -скорость ферментативной реакции, Vmax - максимальная скорость ее при бесконечно большой концентрации субстрата, S - концентрация субстрата в моль/л, Кm - константа Михаэлиса ( она соответствует концентрации субстрата, при которой скорость реакции равна половине максимальной и служит мерой химического сродства меду ферментом и субстратом, мерой их способности образовывать фермент-субстратный комплекс).
Рассмотрим зависимость скорости реакции от количест ва фермента. При условии избытка субстрата скорость реакции пропорциональна количеству фермента, но при избыточном количестве фермента прирост скорости реакции будет сни жаться, поскольку уже не будет хватать субстрата.
Зависимость скорости реакции от температуры. Скорость ферментативных реакций, как и всяких других, зависит от температуры: при повышении температуры на каждые 10 °С скорость увеличивается примерно вдвое (правило Вант-Гоф-фа). Однако для ферментативных реакций это правило справедливо лишь в области низких температур — до 50-60 °С.
Зависимость скорости от температуры.
При более высоких температурах ускоряется денатурация фермента, что означает уменьшение его количества; соответственно снижается и скорость реакции. При 80-90 °С большинство ферментов денатурируется практически мгновенно. Количественное определение ферментов рекомендуется проводить при 25 °С.
Зависимость скорости реакции от рН. Изменение рН приводит к изменению степени ионизации ионогенных групп в активном центре, а это влияет на сродство субстрата к активному центру и на каталитический механизм. Кроме того, изменение ионизации белка (не только в области активного центра) вызывает конформационные изменения молекулы фермента. Колоколообразная форма кривой означает, что существует некоторое оптимальное состояние ионизации фермента, обеспечивающее наилучшее соединение с субстратом и катализ реакции. Оптимум рН для большинства ферментов лежит в пределах от 6 до 8. Однако есть и исключения: например, пепсин наиболее активен при рН 2. Количественное определение ферментов проводят при оптимальном для данного фермента рН.
Зависимость скорости реакции от времени. По мере увеличения времени инкубации скорость реакции снижается .Это может происходить вследствие уменьшения концентрации субстрата, увеличения скорости обратной реакции (в результате накопления продукта прямой реакции), ингибирования фермента продуктом реакции, денатурации фермента. При количественном определении ферментов и кинетических исследованиях измеряют начальную скорость реакции (скорость непосредственно после начала реакции). Время, в течение которого скорость с допустимым приближением можно считать начальной, для каждого фермента и для данных условий подбирается экспериментально, на основе графика, представленного на рис. 2.17, е. прямолинейный участок графика, начинающийся от отметки нулевого времени, соответствует интервалу времени, в течение которого скорость реакции равна начальной скорости или близка к ней (на рисунке этот интервал отмечен пунктирной линией).
