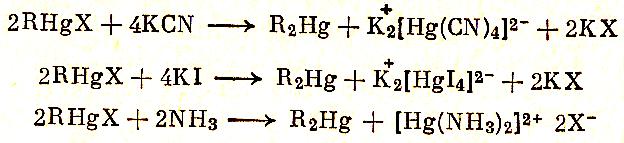- •1.Классификация по типу превращения субстрата
- •2.Классификация по типу активирования.
- •3.Классификация по характеру разрыва связей.
- •4.Одноэлектронные реакции
- •1. Природные источники.
- •4. Способы получения (методы синтеза).
- •5. Химические свойства.
- •2. Перициклические реакции.
- •Металлоорганический синтез.
- •Гидрирование бензола и его гомологов.
- •Пиролиз солей дикарбоновых кислот.
- •Дегалогенирование вицинальных дигалогеналканов.
- •Реакция Виттига.
- •Дегидрирование и крекинг алканов.
- •Дегидратация спиртов (элиминирование).
- •Дегидрогалогенирование галогеналканов.
- •Галогенирование алкенов.
- •Гидрогалогенирование.
- •Гидратация.
- •4. Присоединение спиртов.
- •5. Оксимеркурирование.
- •6. Гидроборирование.
- •7. Присоединение хлорноватистой кислоты.
- •8. Окисление.
- •Карбидный способ.
- •Пиролиз этилена и метана.
- •Дегалогенирование дигалогеннидов и галогеналкенов.
- •Гидролиз
- •1. Галогенангидриды
- •Ацилирование хлорангидридами
- •Восстановление хлорангидридов
- •2.Ангидриды карбоновых кислот
- •3.Сложные эфиры
- •Нитрилы
- •Альдегидо- и кетокислоты.
- •Строение и таутомерия ацетоуксусного эфира
- •Нитросоединения
- •Восстановление нитросоединений
- •2. Действие азотистой кислоты.
- •Реакция анри ( конденсация нитроалканов с альдегидами)
- •Диазосоединения
- •Элементорганические соединения
- •Активные металлоорганические соединения
- •I , II и III групп
- •Вторая группа периодической системы
- •Третья группа периодической системы
- •Четвертая группа периодической системы
- •Пятая группа периодической системы
- •Аминокислоты. Белки.
- •Пятичленные гетероциклы с одним гетероатомом и их производные.
- •Шестичленные и конденсированные гетероциклические соединения. Алкалоиды.
- •Серосодержащие органические соединения
Вторая группа периодической системы
Из производных элементов второй группы следует подробно остановиться на органических соединениях магния, которые часто применяют для синтеза многих органических соединений
МАГНИЙОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ.
Известны два типа магнийорганических соединений- R2Mg и RMgX (где Х-галоген). Полные магнийорганические соединения R2Mg можно получить через ртутноорганические (действием металлического магния) или из соединений типа RMgX. Эти последние (гриньяровы реактивы) получают наиболее часто действием галогенпроизводных углеводородов на металлический магний в растворе диэтилового эфира, который существенно ускоряет реакцию:
RX + Mg → RMgX
Такая реакция называется реакцией Гриньяра ( по имени французского химика, лауреата Нобелевской премии). Эфирные растворы магнийорганических соединений, образующихся в результате этой реакции, называются реактивами Гриньяра. Эфир в этих растворах играет роль растворителя и катализатора.
В последнее время в качестве еще более благоприятной среды для проведения гриньяровой реакции, чем этиловый эфир, предложен тетрагидрофуран.
Из дигалогеналканов димагнийгалогениды образуются только из галогенпроизводных с галогенами, удаленными друг от друга не менее чем на четыре углеродных атома

Галогенпроизводные жирного, алициклического и ароматического рядов, образующие гриньяровы реактивы, не должны иметь реагирующих с реактивом гриньяра заместителей, таких как альдегидная, кетонная, сложноэфирная, нитрильная. В молекуле галогенпроизводного могут присутствовать простые эфирные и третичные группы, но не при том же углероде, с которым соединен галоген, и не при соседнем с ним атоме углерода. Единственным исключением являются сложные эфиры α-галогенкарбоновых кислот, которые вступают в реакцию с магнием

РЕАКЦИИ ГРИНЬЯРОВЫХ РЕАКТИВОВ
Соединения с активным водородом ( все кислоты, вода, спирты и другие гидроксильные производные, аммиак, первичные, вторичные амины реагируют с реактивом Гриньяра по схеме:
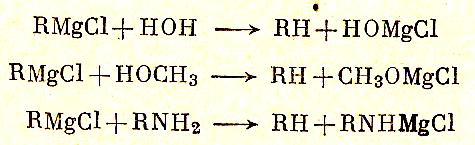
Галогены, кислород, сера разрывают в гриньяровом реактиве связь C-Mg:
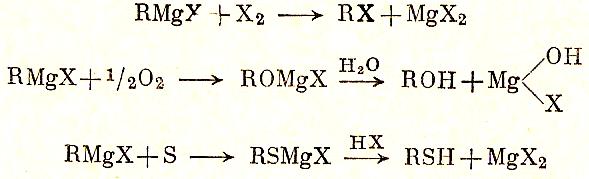
Окисление реактивов Гриньяра:
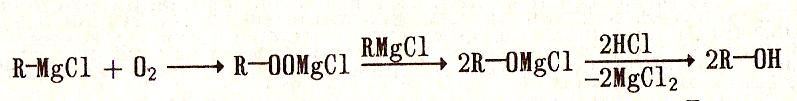
Оксосоединения присоединяют гриньяров реактив:
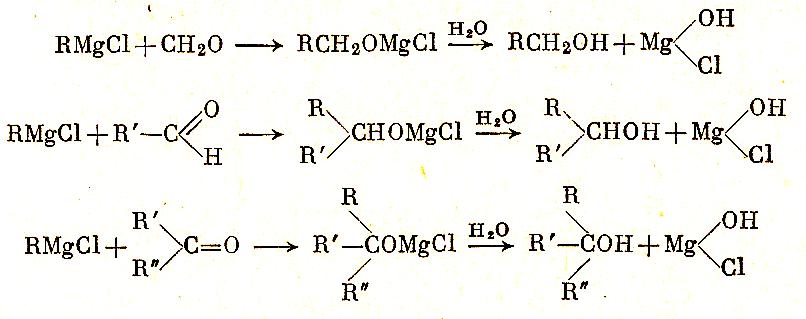
Непредельные кетоны с сопряженной системой π-связей присоединяют гриньяров реактив в 1,4-положение, что после гидролиза приводит к образованию предельного кетона:
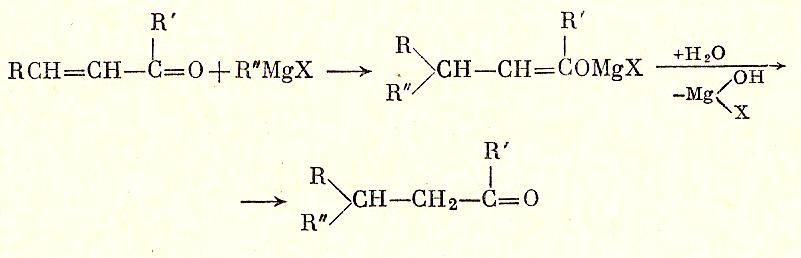
С реактивом Гриньяра аналогично кетонам реагируют нитрилы (это надежный способ получения кетонов).
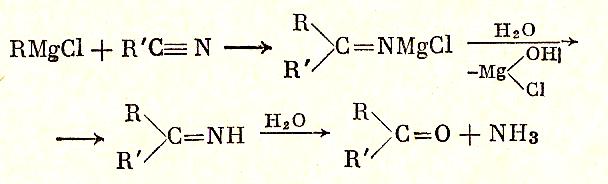
При взаимодействии гриньярова реактива с хлорангидридами кислот при охлаждении также получаются кетоны:
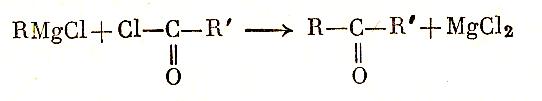
Сложные эфиры реагируют с гриньяровым реактивом с образованием третичных спиртов:
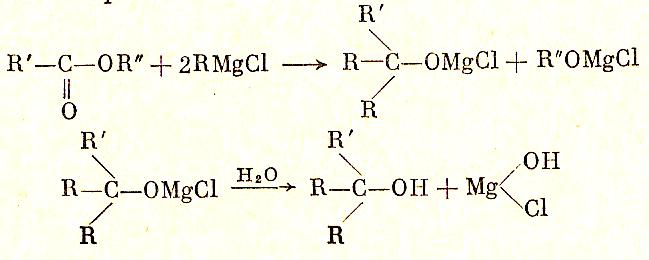
Чрезвычайно важной реакцией является реакция магнийорганических соединений с газообразной или твердой СО2, приводящая к синтезу кислот:
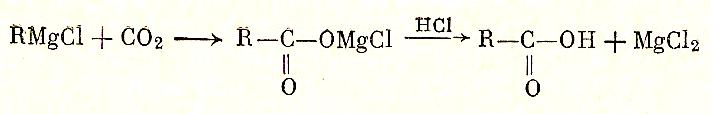
10. С хлорамином, а лучше с эфиром гидроксиламина образуются первичные амины:
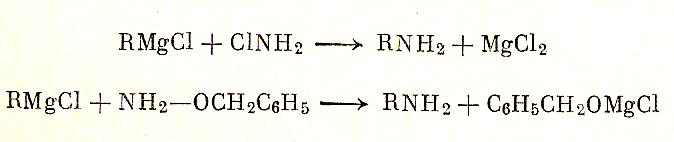
Из шифовых оснований и гриньярова реактива получают вторичные амины (реакция Буша)
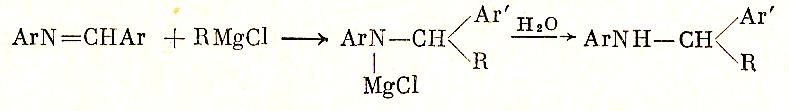
Обменной реакцией соли металла с гриньяровым реактивом получаются металлоорганические соединения:
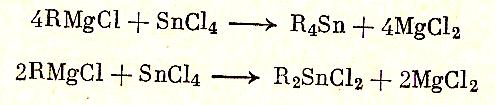
ЦИНКОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Реакции цинкорганических соединений, вполне аналогичны реакциям магниорганических веществ. Третичные спирты, существование которых было предсказано Бутлеровым на основании теории строения, были им открыты именно посредством синтеза с цинкорганическими соединениями.
Цинкорганические соединения, однако, более инертны, чем магнийорганические, и не реагируют с углекислым газом в обычных условиях. После открытия гриньяровых реактивов неудобные в обращении соединения цинка почти не используются. Но надо отдать историческое должное этим веществам:
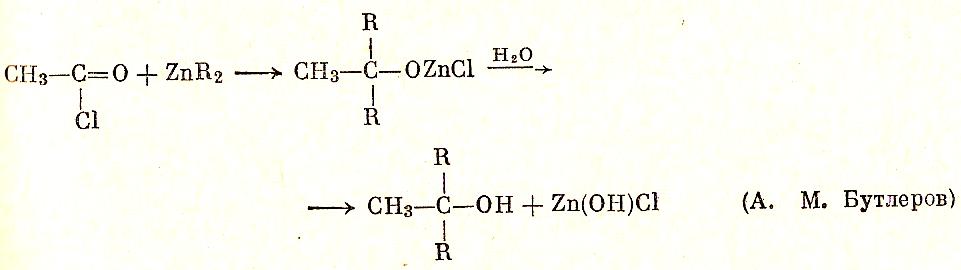
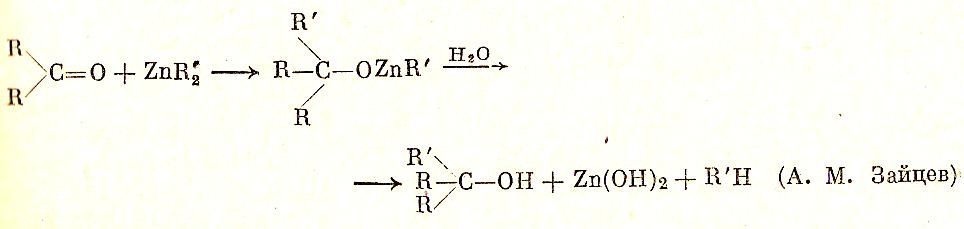
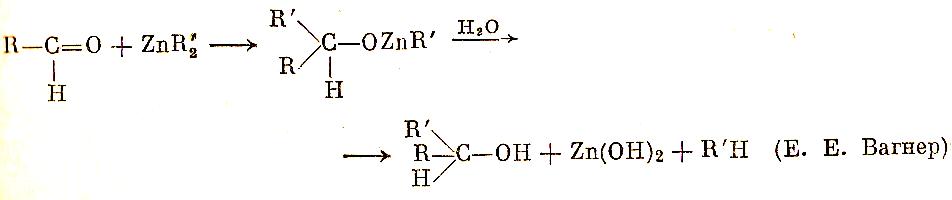
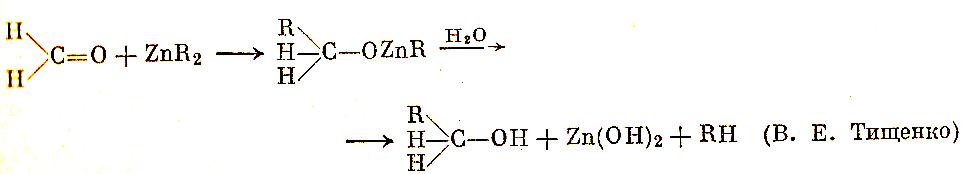
Кадмийорганические соединения по свойствам близки к цинкорганическим. При синтезе кетонов из хлорангидридов карбоновых кислот часто добавляют хлористый кадмий к гриньярову реактиву.
Металлоорганические соединения кальция, стронция и бария до сих пор очень мало изучены. Их с трудом модно получить в чистом виде из-за их реакционной способности. Эти соединения намного более активны, чем магнийорганические.
Бериллийорганические соединения плохо получаются взаимодействием металла с галогенпроизводными углеводородами. По свойствам они ближе к алюминийорганическим соединениям.
РТУТНООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ.
По способам получения и свойствам ртутноорганические соединения резко отличаются от соединений остальный элементов II группы.
Ртутноорганические соединения бывают полные R2Hg и смешанные RHgCl
Их можно получить общей реакцией синтеза металлоорганических соединений- действием гриньярова реактива на соответствующее количество галогенида ртути:
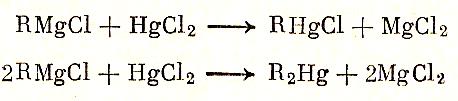
Смешанные ртутноорганические соединения можно превратить в полные реакцией симметризации, вызываемой действием ряда веществ, способных связать соль ртути в комплекс или иное неионное соединение: