- •Структура, свойства и функции белков.
- •Универсальность первичной структуры. Белки, выполняющие одинаковые функции в разных организмах имеют одинаковую или близкую первичную структуру.
- •В природных белках одна и та же аминокислота не встречается подряд больше 3 раз.
- •Структура и свойства ферментов.
- •Для ферментов и неорганических катализаторов характерны общие свойства:
- •Ферменты классифицируют по химической структуре:
- •Функции белковой и небелковой части фермента.
- •Факторы, влияющие на активность ферментов.
- •Анализ уравнения Михаэлиса-Ментен.
- •Km показывает:
- •Зависимость скорости ферментативной реакции от концентрации фермента.
- •Зависимость скорости ферментативной реакции от температуры.
- •Зависимость скорости реакции от рН
- •Влияние рН.
- •Классификация ферментов.
- •Номенклатура ферментов.
- •Аэробные дегидрогеназы – переносят протоны и электроны на кислород.
- •Дегидрирование гидроксильных групп
- •Дегидрирование альдегидных групп (дегидрирование глицеральдегид – 3 – фосфата)
- •Дегидрирование аминогрупп
- •Влияние низкомолекулярных веществ на активность фенрментов.
- •Значение ингибирования активности ферментов.
- •Ингибирование бывает 2-х видов:
- •Необратимое ингибирование
- •Конкурентное
- •Неконкурентное
- •Vmax – одинакова
- •Неконкурентное, обратимое ингибирование.
- •Vmax – уменьшается.
- •Различают три вида регуляторных ферментов:
- •Активация зимогенов.
- •Уровни организации ферментов в клетке.
- •I уровень организации
- •II уровень организации
- •III уровень организации
- •Биологическое окисление.
- •Сходство между окислением в организме и вне организма.
- •Различия между окислением в организме и вне организма.
- •Виды биологического окисления.
- •Строение дыхательной цепи.
- •Пути использования энергии переноса электронов.
- •Энергия переноса электронов используется на синтез атф.
- •Энергия переноса электронов используется для выработки тепла.
- •Причины нарушения биологического окисления.
- •Обмен углеводов.
- •Обмен углеводов.
- •Значение углеводов в организме:
- •Углеводы – это основной энергетический материал.
- •Углеводы выполняют пластическую функцию. К ним относятся пентозы нуклеотидов и гликопротеинов, гетерополисахариды межклеточного вещества.
- •Углеводы могут превращаться в липиды и некоторые аминокислоты.
- •Гликолиз.
- •Стадии гликолиза.
- •1. Фосфорилирование глюкозы: реакция протекает необратимо, катализируется гексокиназой и требует затраты атф:
- •Значение анаэробного гликолиза:
- •II. При достаточном содержании о2 в клетке глю окисляется до конечных продуктов – со2, н2о и этот процесс называется аэробным окислением глю.
- •Глицерофосфатный челночный механизм;
- •Малатно-аспартатный челночный механизм. Глицерофосфатный челночный механизм.
- •Малатный челночный механизм.
- •Баланс аэробного гликолиза:
- •Анаэробный гликолиз – субстратное фосфорилирование – 2атф
- •2Пир 2 сн3соsKoА – окислительное декарбоксилирование 2 надн- 6атф
- •Регенерация 2 надн в челночном механизме - 6 атф
- •Включение в гликолиз других моносахаридов.
- •Пентозофосфатный (апотамический) путь окисления глюкозы.
- •Надфн, d используется как источник восстановительных эквивалентов в процессах биосинтеза жирных кислот, стероидов.
- •Рибозо-5-фосфата (пентозы), d используется для синтеза нуклеиновых кислот.
- •Образование атф.
- •Взаимосвязь пентозного пути и гликолиза.
- •Обмен гликогена.
- •Гликогенолиз – распад гликогена идет путем фосфоролиза.
- •Биосинтез углеводов.
- •Организационные принципы биосинтеза.
- •Фосфоенолпируват ббразуется из пирувата через оксалоацетат.
- •Вторая реакция гликолиза, которая не может использоваться для глюконеогенеза – это реакция фосфорилирования фру-6-ф, катализируемая фосфофруктокиназой.
- •Третьей обходной реакции в синтезе глюкозы является дефосфорилирование глю-6-ф с образованием глю.
- •Алкоголь тормозит глюконеогенез.
- •Окислительное декарбоксилирование пирувата.
- •Цикл трикарбоновых кислот.
- •Патология обмена углеводов.
- •Методы диагностики сахарного диабета.
- •Метод сахарной нагрузки.
- •Особенности обмена глюкозы в клетках опухали.
- •Гликогенозы.
- •Мышечные гликогенозы
- •Гемолитические анемии.
- •Особенности обмена углеводов в различных органах и тканях.
- •1. Обмен углеводов в печени.
- •Роль печени в обмене углеводов.
- •Обмен углеводов в мышцах.
- •Обмен углеводов в мышце.
- •Обмен углеводов в мозге.
- •Обмен углеводов в ткани мозга.
- •Обмен углеводов в эритроцитах.
- •Обмен углеводов в эритроцитах.
- •Регуляция обмена углеводов.
- •Концентрация метаболитов и глюкозы.
- •Воздействие гормонов. Внутриклеточные рецепторы.
- •Регуляция гликолиза.
- •Регуляция пируватдегидрогеназного комплекса.
- •Ингибирование продуктами реакции. Ацетил-КоА и надн ингибируют превращение
- •Регуляция нуклеотидами по принципу обратной связи.
- •Регуляция цтк.
- •2) Изоцитрат -оксоглутарат
- •3) Третьей регуляторной реакцией является реакция, катализируемая -кетоглутаратдегидрогеназой:
- •Регуляция цикла лимонной кислоты.
- •Активация пируваткарбоксилазы.
- •Гормональная регуляция обмена углеводов
- •Функции жирных кислот
- •Насыщенные жирные кислоты в основном энергетический материал (используются и как структурный материал).
- •Полинасыщенные жирные кислоты – эссенциальные соединения. Они не синтезируются в организме (линолевая) или синтезируются в недостаточном количестве.
- •Производные липидов
- •Транспорт липидов
- •Хиломикроны – самые крупные липопротеиды. Имеют низкую плотность (d 0,94 г/см3).Содержат 2% белка, 98% липиды, в основном триглицериды, которые поступают с пищей.
- •Функции аполипопротеинов:
- •Обмен триглицеридов.
- •Обмен триглицеридов.
- •Транспортные формы липидов.
- •Хиломикроны – крупные, рыхлые, 2% белка, 98% тг пищи.
- •Лпнп – 10-15% белка, 50% холестерина. Это основная транспортная форма холестерина и холестеридов.
- •Лпвп – 50% белка, остальные 50% распределены поровну между липидами.
- •Обмен триглицеридов.
- •Значение липидов в организме:
- •Липиды являются одним из компонентов клеточных мембран.
- •Липиды являются источником энергии для организма.
- •Липиды входят в состав водоотталкивающих и термоизоляционных покровов.
- •Переваривание и всасывание липидов
- •Ресинтез жиров в стенке кишечника
- •Промежуточный обмен липидов.
- •Внутриклеточный липолиз
- •Окисление жирных кислот.
- •Активация жирной кислоты происходит в митохондриальной мембране, где она катализируется ацил-КоА-синтетазой:
- •Перенос остатка жирной кислоты через мембрану митохондрий осуществляется карнитином:
- •Этапы -окисления
- •Расчет выхода энергии при окислении жирной кислоты
- •Окисление ненасыщенных жирных кислот
- •Окисление жирных кислот с нечетным числом углеродных атомов
- •Биосинтез жирных кислот
- •Механизм переноса ацетил – КоА через мембрану
- •Синтез ненасыщенных жирных кислот
- •Обмен и биологическое значение холестерина Переваривание и всасывание
- •Биосинтез холестерина
- •Регуляция биосинтеза холестерина
- •Транспорт холестерина
- •Судьба холестерина в клетке
- •Лнп с рецептором подвергается эндоцитозу и включается в лизосомы. Там лнп (аполипопротеиды, холестериды) распадаются. Хлороквин – ингибитор лизосомального гидролиза подавляет эти процессы.
- •Превращение холестерина в организме
- •Эстерификация холестерина
- •Окисление холестерина.
- •Окисление в монооксидазных системах печени и других органов
- •Экскреторные органы Моноокисдазная система.
- •Метаболизм кетоновых тел.
- •Холестерин в патологии.
Значение анаэробного гликолиза:
Окисление глю в условиях недостатка кислорода в тканях позволяет получить энергию клеткой при гипоксии, которая может быть вызвана физической нагрузкой, а также нарушениями со стороны сердечно-сосудистой и дыхательной систем. При ИБС наблюдается анаэробный гликолиз, т.к. нарушается при дефиците О2 работа дыхвтельной цепи, а следовательно окисление глю и жирных кислот, которые является главнейшими источниками энергии.
II. При достаточном содержании о2 в клетке глю окисляется до конечных продуктов – со2, н2о и этот процесс называется аэробным окислением глю.

Конечным продуктом аэробного гликолиза является пируват, а энергетический баланс складывается из 3 молекул АТФ образовавшихся в результате субстратного фосфорилирования и остается еще 2 молекулы восстановленного НАДН, от концентрации которого зависит активность процесса. Для продолжения процесса необходим сброс Н2 на ферменты дыхательной цепи, но сама молекула НАДН через мембрану митохондрий проникнуть не может, для этого используются переносчики и перенос осуществляется с помощью 2-х механизмов:
Глицерофосфатный челночный механизм;
Малатно-аспартатный челночный механизм. Глицерофосфатный челночный механизм.
Цитоплазма |
|
Митохондрии |
|
|
|
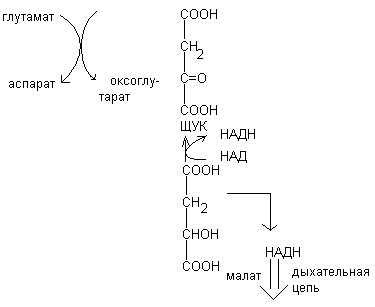
Малатный челночный механизм.
Цитоплазма |
|
Митохондрии |
|
|
|
В процессе гликолиза образуется восстановленная форма НАДН, которая не может непосредственно передавать водород на дыхательную цепь, т.к. митохондриальная мембрана непроницаема для НАДН. Перенос водорода с цитозольного НАДН в митохондрии происходит при участии специальных механизмов, называемых челночными. Суть механизмов сводится к тому, что НАДН в цитозоле восстанавливает какое-то соединение, способное проникать в митохондрию; в митохондрии это соединение окисляется, восстанавливая внутримитохондральный НАД, и вновь переходит в цитозоль.
Баланс аэробного гликолиза:
Анаэробный гликолиз – субстратное фосфорилирование – 2атф
Глю 2пир
2Пир 2 сн3соsKoА – окислительное декарбоксилирование 2 надн- 6атф
Регенерация 2 надн в челночном механизме - 6 атф
ЦТК 2 СН3СОSKoА СО2 24 АТФ
Н2О
38 АТФ
СХЕМА ГЛИКОЛИЗА.

Включение в гликолиз других моносахаридов.
В гликолиз вовлекаются, кроме глюкозы и другие моносахара. Такие как D-фруктоза, манноза и галактоза.
Фруктоза и манноза фосфорилируются с помощью неспецифической гексокиназы с образованием фруктозо-6-фосфата и является метаболитом гликолиза. Маннозо-6-фосфат изомеризуется фосфоманнозоизомеразой во фруктозо-6-фосфат.
Имеется и другой путь включения фруктозы в гликолиз. Фруктоза под действием фруктокиназы печени превращается во фруктозо-1-фосфат, а под действием альдолазы расщепляется на дигидроксиацетонфосфат и глицеральдегид.
Галактоза сначала также фосфорилируется в печени с помощью галактокиназы: D-галактоза + АТФ галактозо-1-Ф +АДФ Затем галактозо-1-фосфат превращается в глюкозо-1-фосфат. Для этой реакции изомеризации необходимы уридиндифосфат-глюкоза (УДФ-глюкоза) и фермент галактозо-1-фосфат-уридилтрансфераза:
Галактозо-1-фосфат + УДФ-глюкозо УДФ-галактоза + глюкозо-1-фосфат
Глюкозо-1-фосфат подключается к гликолизу, а УДФ-галактоза превращается в УДФ-глюкозу с помощью УДФ-глюкозо-эпимеразы.