
- •31.Вынужденное излучение. Лазеры.
- •§ 233. Оптические квантовые генераторы (лазеры)
- •32.Ядерная модель атома. Опыты Резерфорда.
- •33. Теория Бора. Модель атома Бора.
- •34. Квантово-мех модель атома водорода. Квант числа.
- •35.Опыт Эйнштейна и де Гааза. Спин. Полный момент импульса электрона.
- •36. Сложение моментов. Результирующий момент многоэлектронной системы.
35.Опыт Эйнштейна и де Гааза. Спин. Полный момент импульса электрона.
Экспериментальное определение гиромагнитного отношения проведено в опытах Эйнштейна и де Гааза* (1915), которые наблюдали поворот свободно подвешенного на тончайшей кварцевой нити железного стержня при его намагничении во внешнем магнитном поле (по обмотке соленоида пропускался переменный ток с частотой, равной частоте крутильных колебаний стержня). При исследовании вынужденных крутильных колебаний стержня определялось гиромагнитное отношение, которое оказалось равным –(e/m). Таким образом, знак носителей, обусловливающих молекулярные токи, совпадал со знаком заряда электрона, а гиромагнитное отношение оказалось в два раза большим, чем введенная ранее величина g (см. (131.4)). Для объяснения этого результата, имевшего большое значение для дальнейшего развития физики, было предположено, а впоследствии доказано, что кроме орбитальных моментов (см. (131.1) и (131.2)) электрон обладает собственным механическим моментом импульса Les, называемым спином. Считалось, что спин обусловлен вращением электрона вокруг своей оси, что привело к целому ряду противоречий. В настоящее время установлено, что спин является неотъемлемым свойством электрона, подобно его заряду и массе. Спину электрона Les, соответствует собственный (сотовый) магнитный момент рms, пропорциональный Les и направленный в противоположную сторону:
![]() (131.5)
(131.5)
*В. И. де Гааз (1878—1960) — нидерландский физик.
Величина gs называется гиромагнитным отношением спиновых моментов.
Проекция собственного магнитного момента на направление вектора В может принимать только одно из следующих двух значений:
![]()
где ħ=h/(2) (h—постоянная Планка), b—магнетон Бора, являющийся единицей магнитного момента электрона.
36. Сложение моментов. Результирующий момент многоэлектронной системы.
КВАНТОВОЕ СЛОЖЕНИЕ МОМЕНТОВ
- сложение
моментов (орбитальных, спиновых, полных)
независимых частиц (или систем - атомов,
молекул и т. д.) по законам квантовой
механики. Применяется
также назв. векторное сложение моментов.
В случае двух частиц задача состоит в
определении спектра возможных собств.
значений оператора квадрата суммарного
момента ![]() и
его проекции
и
его проекции ![]() на
фиксированную ось и соответствующих
собств. ф-ций
на
фиксированную ось и соответствующих
собств. ф-ций ![]() -
операторы моментов частиц 1,2). Спектр
имеет вид
-
операторы моментов частиц 1,2). Спектр
имеет вид
![]() где
квантовое число суммарного момента j может
принимать значения j=j1+j2, j1+j2-1,
..., | j1-j2 |, а
его проекции т=j,
j -1,
. . ., -j (j1,
m1 и j2,
т2 - квантовые
числа моментов частиц 1 и 2 и их проекций).
При этом каждое из возможных
значений j встречается
только один раз, что легко подтверждается
подсчётом общего числа квантовых
состояний (j,
m):
где
квантовое число суммарного момента j может
принимать значения j=j1+j2, j1+j2-1,
..., | j1-j2 |, а
его проекции т=j,
j -1,
. . ., -j (j1,
m1 и j2,
т2 - квантовые
числа моментов частиц 1 и 2 и их проекций).
При этом каждое из возможных
значений j встречается
только один раз, что легко подтверждается
подсчётом общего числа квантовых
состояний (j,
m):
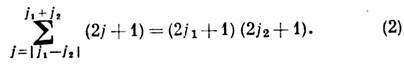 На
матeм. языке рассматриваемая задача
соответствует разложению прямого
(тензорного) произведения двух неприводимых
представлений
На
матeм. языке рассматриваемая задача
соответствует разложению прямого
(тензорного) произведения двух неприводимых
представлений ![]() группы
вращений трёхмерного пространства
SO(3) на неприводимые компоненты, что
символически записывается в виде
группы
вращений трёхмерного пространства
SO(3) на неприводимые компоненты, что
символически записывается в виде
![]() (ряд
Клебша - Гордана). Все значения j либо
целые (когда j1 и j2 одновременно
целые или полуцелые), либо полуцелые
(когда один из складываемых моментов
целый, а другой - полуцелый). В частности,
для отд. электрона в атоме j всегда
полуцелое: j=l+s, где
квантовое число орбитального момента l=0,
1, 2, . . ., а спинового: s=1/2.Сложение
произвольного числа N моментов
(ряд
Клебша - Гордана). Все значения j либо
целые (когда j1 и j2 одновременно
целые или полуцелые), либо полуцелые
(когда один из складываемых моментов
целый, а другой - полуцелый). В частности,
для отд. электрона в атоме j всегда
полуцелое: j=l+s, где
квантовое число орбитального момента l=0,
1, 2, . . ., а спинового: s=1/2.Сложение
произвольного числа N моментов
J=j1+j2+...+jN(4)
может
быть выполнено последоват. применением
операции (1). В частности, наиб.
значение J=j1+j2+...+jN имеет
кратность, равную единице (т. е. встречается
в разложении прямого произведения ![]() только
один раз). В теории атомов применяются
след. схемы сложения моментов: 1) связь
Расселла - Саундерса (LS-связъ),в
к-рой сначала складываются орбитальные
и спиновые моменты отд. электронов:
только
один раз). В теории атомов применяются
след. схемы сложения моментов: 1) связь
Расселла - Саундерса (LS-связъ),в
к-рой сначала складываются орбитальные
и спиновые моменты отд. электронов:
![]() а
затем L и S складываются
в полный момент атома J;
2) jj -связь,
в к-рой орбитальный и спиновый моменты i -го
электрона складываются в полный момент
электрона ji=li+si,
после чего полный момент атома J определяется
по ф-ле (4). Условием применимости LS- связиявляется
малость релятивистских взаимодействий
по сравнению с эл.-статическим
(кулоновским), поэтому она хорошо работает
в лёгких атомах. По мере увеличения
атомного номера Z роль
релятивистских эффектов возрастает и
происходит переход от LS -связи
к jj- связи(однако
в чистом виде последний тип связи
фактически не встречается даже в самых
тяжёлых атомах).Следует подчеркнуть,
что только J и Jz -строго
сохраняющиеся величины (соответствующие
операторы коммутируют с гамильтонианом),
в то время как li, L и S в
схеме LS- связи, ji в
схеме jj -связи
сохраняются лишь приближённо. <Для
построения волновой ф-ции yjm,
отвечающей собств. значениям (1), из
волновых ф-ций отд. частиц yj1m1 и
yj2m2 используются Клебша
- Гордана коэффициенты (или
Вигнера 3j -символы).
При сложении большего числа моментов
применяются Вигнера6j-символы (или
связанные с ними Рака
коэффициенты )или
3nj -символы
(при n/2).
а
затем L и S складываются
в полный момент атома J;
2) jj -связь,
в к-рой орбитальный и спиновый моменты i -го
электрона складываются в полный момент
электрона ji=li+si,
после чего полный момент атома J определяется
по ф-ле (4). Условием применимости LS- связиявляется
малость релятивистских взаимодействий
по сравнению с эл.-статическим
(кулоновским), поэтому она хорошо работает
в лёгких атомах. По мере увеличения
атомного номера Z роль
релятивистских эффектов возрастает и
происходит переход от LS -связи
к jj- связи(однако
в чистом виде последний тип связи
фактически не встречается даже в самых
тяжёлых атомах).Следует подчеркнуть,
что только J и Jz -строго
сохраняющиеся величины (соответствующие
операторы коммутируют с гамильтонианом),
в то время как li, L и S в
схеме LS- связи, ji в
схеме jj -связи
сохраняются лишь приближённо. <Для
построения волновой ф-ции yjm,
отвечающей собств. значениям (1), из
волновых ф-ций отд. частиц yj1m1 и
yj2m2 используются Клебша
- Гордана коэффициенты (или
Вигнера 3j -символы).
При сложении большего числа моментов
применяются Вигнера6j-символы (или
связанные с ними Рака
коэффициенты )или
3nj -символы
(при n/2).
Каждый электрон в атоме обладает орбитальным моментом импульса и собственным моментом Механические моменты связаны с соответствующими магнитными моментами, вследствие чего между всеми имеется взаимодействие.
Моменты складываются в результирующий момент атома При этом возможны два случая.
1. Моменты взаимодействуют между собой сильнее, чем с которые в свою очередь сильнее связаны друг с другом, чем с Вследствие этого все складываются в результирующую моменты складываются в а затем уже дают суммарный момент атома Такой вид связи встречается чаще всего и называется связью Рёссель — Саундерса или вязью.
2. Каждая пара взаимодействует между собой сильнее, чем с другими вследствие чего образуются результирующие для каждого электрона в отдельности, которые затем уже объединяются в атома. Такой вид связи, называемый вязью, наблюдается у тяжелых атомов.
Сложение моментов осуществляется по квантовым законам (см. § 24). Рассмотрим подробнее сложение моментов в случае связи Рёссель — Саундерса.
Орбитальные квантовые числа U всегда бывают целыми. Соответственно квантовое число L суммарного орбитального момента также бывает целым (либо нулем).
Квантовое число S результирующего спинового момента атома может быть целым или полуцелым в зависимости от того, каким является число электронов в атоме — четным или нечетным. При четном числе электронов N квантовое число S принимает все целые значения от «параллельны» друг другу) до нуля (все попарно компенсируют друг друга). Так, например, при может иметь значения 2, 1, 0. При нечетном N квантовое число S принимает все полуцелые значения от «параллельны» друг другу) до кроме одного, попарно компенсируют друг друга). Например, при возможными значениями S будут:
При данных квантовое число J результирующего, момента может иметь одно из следующих значений:
![]()
Следовательно, будет целым, если S — целое (т. е. при четном числе электронов в атоме), и полуцелым, если S — полуцелое (т. е. при нечетном числе электронов).
Так, например,
1) в случае возможные значения J равны 3, 2, 1;
2) в случае возможные значения равны
Энергия атома зависит от взаимной ориентации моментов (т. е. от квантового числа L), от взаимной ориентации моментов (от квантового числа S) и от взаимной ориентации квантового числа l). Условно терм атома записывается следующим образом:
![]()
где под L подразумевается одна из букв S, Р, D, F и т. д. в зависимости от значения числа L. Например, термы
![]()
относятся к состояниям с одинаковыми одинаковыми но различными J, равными 0, 1, 2.
Символ (32.1) содержит в себе сведения о значениях трех квантовых чисел L, S и . В случае, когда , стоящее слева вверху число дает мультиплетность терма, т. е. количество подуровней, отличающихся значением числа J (см. (32.2)). В случае, когда фактическая мультиплетность равна Однако символ терма все равно пишут в виде (32.1), иначе он не содержал бы сведений о значении квантового числа
Обозначениями типа (32.1) мы уже пользовались в § 29 применительно к атомам щелочных металлов. Однако для этих элементов характерно то, что S атома, совпадая с s валентного электрона, равно Теперь же мы познакомились с символическими обозначениями термов для любых случаев.
