
- •1. Кинематика материальной точки.
- •2. Скорость и ускорение
- •3. Криволинейное движение тела
- •4. Динамика материальной точки. Законы Ньютона
- •5. Импульс тела
- •6. Импульс системы материальных точек.
- •8. Кинетическая и потенциальная энергия. Механическая энергия. Консервативные силы.
- •9. Закон сохранения механической энергии
- •10. Связь консервативной силы с потенциальной энергией
- •11. Центральный удар шаров. Абсолютно упругий удар.
- •12. Центральный удар шаров. Абсолютно неупругий удар. Частично неупругий удар. Коэффициент восстановления относительной скорости при ударе.
- •13. Кинематика вращательного движения. Угловая скорость, угловое ускорение. Связь с линейными величинами: линейной скоростью, тангенциальным(касательным) ускорением и нормальным ускорением.
- •14. Динамика вращательного движения. Момент силы. Момент инерции. Основное уравнение динамики вращательного движения.
- •15. Момент импульса. Закон сохранения момента импульса.
- •16.Кинетическая энергия вращающегося тела.
- •17.Движение в неинерциальных системах отсчета. Кинематика относительного движения.Абсолютные,Относительные,переносные скорости и ускорения, кориолисово ускорение.
- •18. Движение в неинерциальных системах отсчета. Динамика относительного движения. Основное уравнение деинаики относительного движения материальной точки.
- •19. Преобразование Галилея. Экспериментальные факты подтверждающие, теорию относительности.
- •20. Постулаты Эйнштейна. Преобразования Лоренца
- •Следствия из преобразований Лоренца
- •24. Релятивистский импульс
- •25. Релятивистское выражение для энергии.
- •26. Работа и теплота
- •27. Теплоёмкость идеального газа.Теплоёмкость при постоянном объёме и постоянном давлении.Уравнение Майера.
- •28. Теплоёмкости одноатомных и многоатомных газов
- •30. Изоэнтропийный процесс
- •31. Изотермический процесс
- •32. Обратимые и необратимые процессы.Энтропия.
- •33. Второе начало термодинамики.
- •34. Цикл Карно.
- •35.Основное уравнение кинетической теории газов.
- •37. Барометрическая формула. Распределение Больцмана.
- •38. Средняя длина свободного пробега молекул.
- •39. Явления переноса в газах. Диффузия.
- •40. Явление переноса. Элементарная теория диффузии.
- •41. Явления переноса. Теплопроводность газов.
- •42. Явления переноса. Вязкость газа.
- •43. Механические колебания. Свободные гармонические колебания.
- •44. Свободные затухающие колебания.
- •45. Вынужденные механические колебания.
- •46. Явление механического резонанса.
37. Барометрическая формула. Распределение Больцмана.
Молекулы любого газа всегда находятся в поле тяготения Земли. Совместные действия поля тяготения и теплового движения приводят к такому состоянию атмосферы, при котором концентрация и давление газа убывают с возрастанием высоты над Землей.
Найдем закон изменения давления идеального газа с высотой в однородном поле тяготения. Будем считать, его температура Т всюду одинакова. Выделим на высоте h столб abcd газа высотой dh и площадью основания, равной единице (рис. 10.8). Разность давлений p и p+dp равна гидростатическому давлению pgdh столба abcd газа:
![]()
![]()
![]()
или
![]()
Здесь р0 давление газа на высоте h= 0. Если с помощью барометра измерить давление р0 и р, то по формуле (10.16) можно по изменению давления определить высоту:
![]()
Поэтому (10.16) называется барометрической формулой. Барометр, специально проградуированный для отсчета высоты над уровнем моря, называется альтиметром. Он широко применяется в авиации, при восхождениях на горы и т. п.
3. Барометрическая формула позволяет получить соотношение между концентрациями газа на различных высотах. Используем уравнение состояния идеального газа в форме: р = п0кТ, где п0 концентрация молекул газа. При Т= const имеем
![]()
где п00— концентрация молекул газа при давлении р0(на высоте h = 0). Поэтому уравнение (10.16) можно записать в форме
![]()
Заменяя R/M=k/m0, где m0 — масса молекулы газа, получаем
![]()
Из формулы (10.17') следует, что n0→n00 при T→∞, т. е. повышение температуры приводит к выравниванию концентрации газа по всему предоставленному ему объему. При T→0 К n0→0, т. е. молекулы под действием силы тяжести будут опускаться на дно
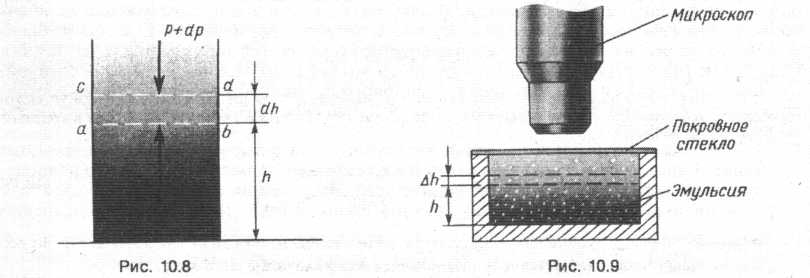
сосуда. Наша атмосфера существует лишь благодаря тепловому движению частиц воздуха.
Если учесть, что mgh= Wn то формулу (10.17') можно переписать в виде
![]()
Заменив в (10.17) M=m0NA, получим
![]()
![]()
38. Средняя длина свободного пробега молекул.
Молекулы непрерывно сталкиваются друг с другом. Между двумя последовательными столкновениями молекулы движутся равномерно и прямолинейно.
Расстояние λ, которое молекула пролетает за время свободного пробега от одного столкновения до следующего, называется длиной свободного пробега. Эти расстояния могут быть самыми разными. Поэтому в кинетической теории вводится понятие средней длины свободного пробега молекул <λ>. Величина <λ> является характеристикой всей совокупности молекул газа при заданных значениях давления и температуры.
Для вычисления <λ> необходимо принять определенную модель молекул газа. Будем считать, что молекулы представляют собой шарики некоторого диаметра d порядка 10-10 м, зависящего от химической природы газа.
Такая модель правильно передает характер сил отталкивания, которые действуют при сильном сближении молекул реальных газов.
Подсчитаем среднее число столкновений, которое испытывает за единицу времени молекула при движении в однородном газе. <Z> - среднее число столкновений; d –диаметр молекул; <u> -средняя скорость движения рассматриваемой молекулы(все остальные молекулы неподвижны); n0 — концентрация молекул газа. Тогда:
![]()
В
действительности все молекулы движутся,
и возможность соударения двух частиц
зависит от их относительной скорости
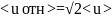 Поэтому значение среднего числа
соударений нужно увеличить в
Поэтому значение среднего числа
соударений нужно увеличить в
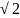 раз:
раз:
![]()
Среднее расстояние, которое пролетает молекула за единицу времени, численно равно <и>. Оно представляет собой произведение <Z> <λ>. средняя длина свободного пробега молекул
![]()
Для данного газа при Т = const и различных давлениях р1 и р2 имеем
![]()
Рассмотрим опыт Борна и Бормана (1921). В этом опыте исследована закономерность убывания интенсивности пучка атомов серебра по мере его распространения в замкнутом сосуде с сильно разреженным воздухом. Пусть N — число атомов, прошедших без рассеяния путь в воздухе, равный х, a |dN| — число атомов, испытывающих столкновения с молекулами воздуха в слое толщиной dx и выбывающих из пучка в этом слое (dN<0). Отношение - dN/N есть вероятность того, что атом серебра, долетевший до рассматриваемого слоя, выйдет в этом слое из пучка. Вероятность такого события равна вероятности столкновения атома с молекулой воздуха в слое толщиной dx, т. е. равна отношению dx/<λ>. Таким образом,
Соотношение (10.23) называется законом распределения свободных пробегов. С его помощью можно найти среднюю длину свободного пробега атомов серебра в воздухе.
если![]() то
то
![]()
![]()
![]()
