
- •Формирование понятия экологический мониторинг. Общие теоретические и методологические принципы, лежащие в основе организации систем мониторинга.
- •Цель и задачи мониторинга. Роль и место экомониторинга в управлении состоянием ос.
- •Классификация видов мониторинга.
- •Экомониторинг на суше. Биотическая и абиотическая составляющая мониторинга.
- •Экомониторинг океана.
- •Биомониторинг. Биоиндикация, критерии выбора биоиндикатора.
- •Климатический мониторинг. Основные разделы.
- •Дистанционный экомониторинг. Системы дистанционного контроля со (пассивные и активные). F системы дистанционного контроля среды обитания
- •1. Пассивные методы дистанционного контроля
- •Дистанционный мониторинг. Аэрокосcмические методы контроля загрязнения ос. Авиационные и вертолетные системы наблюдения.
- •Геоэкологический мониторинг. Задачи, состав и структура системы. Информационное обеспечение.
- •Глобальная система мониторинга окружающей среды (гсмос). Цели программы гсмос.
- •Государственная служба наблюдений (гсн) за состоянием ос. Подсистемы.
- •Единая государственная система экологического мониторинга. Цели и задачи етсэм.
- •Организационное построение етсэм. Субъекты мониторинга.
- •Территориальный информационно-аналитический центр (тиац). Функции тиац.
- •Экоаналитический контроль объектов ос. Отбор проб. Основная цель. Пробоподготовка. Задачи пробоподготовки.
- •Классификация средств измерений. Критерии для выбора подходящего метода количественного определения зв.
- •Хроматографические методы экоконтроля. Классификация методов.
- •Основные элементы хроматограммы. Качественный и количественный анализ.
- •Газовая хроматография. Принцип исполнения метода. Область применения метода.
- •Хроматографические колонки. Описание, виды, основные факторы, влияющие на разделение веществ.
- •Хроматографичесие детекторы. Виды, принцип действия.
- •Высокоэффективная жидкостная хроматография. Область применения метода. Применяемые детекторы.
- •Детекторы для вэжх
- •Электрохимические методы анализа. Прямые и косвенные методы. Потенциометрия. Область применения метода. Качественный и количественный анализ.
- •Электрохимические методы анализа. Полярография и вольтамперометрия. Область применения метода. Качественный и количественный анализ.
- •Электрохимические методы анализа. Кондуктометрия и кулонометрия. Область применения методов. Качественный и количественный анализ.
- •Vfc Кондуктометрия. Кондуктометрическое титрование
- •Спектральные методы анализа. Атомная спектроскопия. Область применения. Качественный и количественный анализ. Закон Бугера-Ламберта-Бера.
- •Спектральные методы анализа. Молекулярная спектроскопия. Область применения. Качественный и количественный анализ.
Детекторы для вэжх
Ультрафиолетовый
Диодно-матричный
Флуоресцентный
Электрохимический
Рефрактометрический
Масс-селективный
g
Электрохимические методы анализа. Прямые и косвенные методы. Потенциометрия. Область применения метода. Качественный и количественный анализ.
d Потенциометрия
Потенциометрия основана на измерении разности электрических потенциалов, возникающих между разнородными электродами, опущенными в раствор с определяемым веществом. Электрический потенциал возникает на электродах при прохождении на них окислительно-восстановительной (электрохимической) реакции. Окислительно-восстановительные реакции протекают между окислителем и восстановителем с образованием окислительно-восстановительных пар, потенциал Е которых определяется по уравнению Нернста концентрациями компонентов пар [ок] и [вос]:
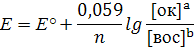
Потенциометрические измерения проводят, опуская в раствор два электрода – индикаторный, реагирующий на концентрацию определяемых ионов, и стандартный электрод или электрод сравнения, относительно которого измеряется потенциал индикаторного. Применяют несколько видов индикаторных и стандартных электродов.
b
Электрохимические методы анализа. Полярография и вольтамперометрия. Область применения метода. Качественный и количественный анализ.
Вольтамперометрия включает совокупность методов исследования вольтамперных кривых и их зависимостей от электродных реакций, концентраций, а также их использование для проведения качественного и количественного анализа. Если вольтамперометрические исследования проводят при помощи капельного ртутного электрода, то этот метод принято называть полярографией. Вольтамперометрию при постоянном токе называется хронопотенциометрией. Метод основан на том, что через ячейку, состоящую из рабочего электрода и электрода сравнения, пропускают постоянный ток и замеряют изменение потенциала рабочего электрода по отношению к электроду сравнения в зависимости от времени. Если рабочий электрод является катодом, постоянный ток вызывает восстановление окисленной формы, что приводит к изменению потенциала во времени в сторону отрицательных значений. Корень квадратный из времени от начала электролиза до резкого изменения потенциала пропорционален общей концентрации раствора
Электрохимические методы анализа. Кондуктометрия и кулонометрия. Область применения методов. Качественный и количественный анализ.
Vfc Кондуктометрия. Кондуктометрическое титрование
Кондуктометрия основана на измерении электрической проводимости раствора. Если в раствор вещества поместить два электрода и подать на электроды разность потенциалов, то через раствор потечет электрический ток. Как и каждый проводник электричества, растворы характеризуются сопротивлением R и обратной ему величиной – электрической проводимостью L:
![]()
![]()
Кондуктометрический анализ проводят с помощью кондуктометров – приборов, измеряющих сопротивление растворов. По величине сопротивления R определяют обратную ему по величине электрическую проводимость растворов L.
Определение концентрации растворов осуществляют прямой кондуктометрией и кондуктометрическим титрованием. Прямая кондуктометрия используется для определения концентрации раствора по калибровочному графику. Для составления калибровочного графика замеряют электр.проводимось серии растворов с известной концентрацией и строят калибровочный график зависимости электр.проводимости от концентрации. Затем измеряют электр.проводимость анализируемого раствора и по графику определяют его концентрацию.
Чаще применяют кондуктометрическое титрование. При этом в ячейку с электродами помещают анализируемый раствор, ячейку помещают на магнитную мешалку и титруют соответствующим титрантом. Титрант добавляют равными порциями. После добавления каждой порции титранта замеряют электр.проводимость раствора и строят график зависимости между электр.проводимостью и объемом титранта. При добавлении титранта происходит изменение электр.проводимости раствора в т.э. наступает перегиб кривой титрования.
b
