
- •1.Химия как раздел естествознания. Понятия: вещество, молекула, атом, моль.
- •2.Законы: сохранения массы и энергии, постоянства состава, Авогадро, кратных отношений, простых объемных отношений, парциальных давлений Дальтона.
- •3.Эквивалент элемента и вещества. Закон эквивалентов.
- •4. Расчет молярной массы эквивалента простого и сложного вещества.
- •2. Квантовые числа: главное, орбитальное, магнитное, спиновое. Понятие атомная орбиталь (ао).
- •1.Свойства ковалентной связи и способы ее образования.
- •2.Основные типы гибридизации ао. Теория локализованных электронных пар.
- •4.Металлическая связь и ее свойства.
- •5.Водородная связь. Силы межмолекулярного взаимодействия.
- •2.Основы термохимии: закон Гесса и его следствия.
- •3.Тепловые эффекты процессов, термохимические уравнения.
- •4.Энтропия и ее изменение при химических реакциях.
- •5.Энергия Гиббса. Критерии определения реакционной способности
- •1.Закон действия масс для химических систем, константа химического равновесия.
- •3. Основной закон химической кинетики. Константа скорости реакции.
- •4.Кинетическая классификация реакций.
- •6.Катализаторы, каталитические системы.
- •1.Окислительно-восстановительная способность веществ. Типы овр.
- •2.Метод электронного баланса.
- •3.Метод ионно-электронных уравнений.
- •4.Эдс окислительно-восстановительного процесса, направление протекания овр.
- •5.Электродный потенциал. Условные электродные потенциалы.
- •6.Гальванические элементы. Эдс гальванического элемента.
- •7. Электролиз. Законы Фарадея.
- •8.Катодные и анодные процессы при электролизе водных растворов.
- •9.Коррозия металлов и ее виды. Показатели скорости коррозии.
- •10.Способы защиты металлов от коррозии.
- •1.Способы выражения состава растворов.
- •2.Закон Рауля для бесконечно разбавленного раствора неэлектролита.
- •3.Осмос, осмотическое давление. Закон Вант-Гоффа для бесконечно разбавленных растворов неэлектролитов.
- •4.Замерзание и кипение бесконечно разбавленных растворов неэлектролитов.
- •5.Электролиты: современная теория диссоциации, классификация, коллигативные свойства, изотонический коэффициент.
- •6.Слабые электролиты: константа и степень диссоциации, закон разбавления Оствальда.
- •7.Произведение растворимости.
- •8.Электролитическая диссоциация воды, ионное произведение воды. Водородный показатель рН, гидроксильный показатель рОн.
- •9.Ионные реакции, смещение ионного равновесия.
- •10.Гидролиз солей. Константа и степень гидролиза.
- •11.Общие понятия о дисперсных системах.
- •12.Коллоидные растворы и методы их получения.
- •13.Оптические и электрические свойства коллоидных растворов.
- •14.Коагуляция, седиментация и пептизация коллоидных растворов.
9.Ионные реакции, смещение ионного равновесия.
Реакции, в которых происходит гетеролитический разрыв связей и образуются промежуточные частицы ионного типа, называются ионными реакциями.
Такие реакции характерны для соединений с полярными связями (C-O, C-N, C-Cl) и связями с высокой поляризуемостью (C=C, C=C-C=C, C=O и т.п.), благодаря их склонности к гетеролитическому разрыву.
Пример
ионной реакции - гидролиз
2-метил-2-хлорпропана. Общая схема
реакции:
(CH3)3C-Cl
+ H2O ![]() (CH3)3C-OH
+ HCl
(CH3)3C-OH
+ HCl
Органические катионы и анионы - неустойчивые промежуточные частицы. В отличие от неорганических ионов, постоянно присутствующих в водных растворах и расплавах, они возникают только в момент реакции и сразу же вступают в дальнейшие превращения.
Условия ионных реакций:-невысокая температура;-полярные растворители, способные к сольватации образующихся ионов.
Действие света или радиоактивного излучения не влияет на скорость ионных реакций. По характеру реагента, действующего на молекулу, ионные реакции делятся на электрофильные и нуклеофильные.
Ионное
равновесие, как и любое другое, смещается
при изменении концентрации одного
из ионов.
Например,
если в раствор уксусной
кислоты, диссоциирующей по
уравнению CH3COOH![]() H+ +
CH3COO–
ввести какую-либо соль этой кислоты и
тем самым увеличить концентрацию
ионов
CH3COO–,
то в соответствии с принципом
Ле-Шателье равновесие
смещается влево. Отсюда следует, что
введение в раствор слабого
электролита одноименных
ионов (т.е. ионов, одинаковых с одним из
ионов электролита)
уменьшает степень
диссоциации этого
электролита.
H+ +
CH3COO–
ввести какую-либо соль этой кислоты и
тем самым увеличить концентрацию
ионов
CH3COO–,
то в соответствии с принципом
Ле-Шателье равновесие
смещается влево. Отсюда следует, что
введение в раствор слабого
электролита одноименных
ионов (т.е. ионов, одинаковых с одним из
ионов электролита)
уменьшает степень
диссоциации этого
электролита.
Аналогично нарушается равновесие в случае малорастворимого электролита (соли). Например, если к насыщенному раствору сульфата кальция CaSO4 добавить другой, хорошо растворимый сульфат (K2SO4), то вследствие увеличения концентрации ионов SO42–равновесие сместится в сторону образования кристаллов (образуется осадок CaSO4). Этот процесс прекратится, когда произведение концентраций [Ca2+] и [SO42–] станет равно произведению растворимости , т.е. установится новое состояние равновесия.
На основании рассмотренных примеров можно сделать следующий вывод: реакции врастворах электролитов всегда идут в сторону образования наименее диссоциированных или наименее растворимых веществ. Из этого, в частности, следует, что сильные кислоты вытесняют слабые из растворов их солей: CH3COONa + HCl = CH3COOH + NaCl
Суть этой реакции более точно отражается ионно-молекулярным уравнением, где формулы слабых электролитов записаны в виде молекул, а сильных – в виде ионов: CH3COO– + Na+ + H+ + Cl– = CH3COOH + Na+ + Cl– или в сокращенном виде: CH3COO– + H+ = CH3COOH. Аналогично протекают реакции между сильными основаниями и солями слабых оснований. Например: FeSO4 + 2 NaOH = Na2SO4 + Fe(OH)2
10.Гидролиз солей. Константа и степень гидролиза.
Гидролиз соли – это взаимодействие соли с молекулами воды, приводящее к образованию малодиссоциироваииых соединений.
Процесс гидролиза заключается в переходе протона от молекулы воды к данному иону (СO32- + НОН * НСO3–+ ОН- ) или от данного иона, в том числе от гидратированного катиона металла, к молекуле воды.
В зависимости от природы соли вода выступает либо как кислота, либо как основание, а соль является соответственно сопряженным основанием или сопряженной кислотой.
Возможны четыре варианта гидролиза в зависимости от типа соли.
1.
Соли, образованные сильной кислотой и
слабым основанием:
![]()
2. Соли, образованные сильным основанием и слабой кислотой: CH3COONa + НОН > СН3СOOН + NaOH.
3. Соли, образованные слабой кислотой и слабым основанием.
Цианид
аммония гидролизуется по реакции:
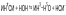
4. Соли, образованные сильной кислотой и сильным основанием.
NaCl, KNO3 гидролизу не подвергаются. Механизм гидролиза солей заключается в поляризационном взаимодействии ионов соли с их гидратной оболочкой. Чем сильнее это взаимодействие, тем интенсивнее протекает гидролиз.
Все рассмотренные случаи гидролиза касались солей, образованных однокислотными основаниями и одноосновными кислотами. Соли многоосновных кислот и многокислотных оснований гидролизуются ступенчато, образуя при этом кислые и основные соли.
Под степенью гидролиза подразумевается отношение части соли, подвергающейся гидролизу, к общей концентрации её ионов в растворе. Обозначается α (или hгидр); α = (cгидр/cобщ)·100 % где cгидр — число молей гидролизованной соли, cобщ — общее число молей растворённой соли. Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие.
Является количественной характеристикой гидролиза. Степень гидролиза зависит от природы соли, ее концентрации и температуры. Согласно закону действующих масс степень гидролиза возрастает с разбавлением раствора.
В общем случае справедливы следующие закономерности.
1. Гидролиз соли должен усиливаться с повышением температуры и разбавлением раствора.
2. При обратимом гидролизе в соответствии с принципом Ле Шателье процесс должен подавляться при подкислении (если эта соль образована сильной кислотой и слабым основанием, накапливаются ионы Н) или при подщелачивании (если соль образована слабой кислотой и сильным основанием, накапливаются ионы ОН).
3. Гидролиз солей, в результате которого образуются малорастворимые или газообразные продукты, удаляющиеся из сферы реакции (принцип смещения равновесия), необратим.
Константа гидролиза — константа равновесия гидролитической реакции. Так константа гидролиза соли равна отношению произведения равновесных концентраций продуктов реакции гидролиза к равновесной концентрации соли с учетом стехиометрических коэффициентов.
