
- •Возможен ли данный процесс при данных условиях?
- •Если процесс возможен, то в каком направлении он пойдет?
- •Чем процесс закончится?
- •1. Вступительная часть 1-2 мин
- •4. Закрепление 5 мин
- •1. Вступительная часть 1-2 мин
- •4. Закрепление 5 мин
- •1. Вступительная часть 1-2 мин
- •4. Закрепление 5 мин
- •1. Вступительная часть 1-2 мин
- •4. Закрепление 5 мин
- •1. Вступительная часть 1-2 мин
- •1. Вступительная часть 1-2 мин
- •3. Лекция 25 мин
- •1. Вступительная часть 1-2 мин
- •Из физика лирик всегда получится (движение от порядка к беспорядку), а из лирика физик никогда (надо много работать).
- •Энтропия
- •1. Вступительная часть 1-2 мин
- •Созидательный хаос
- •1. Вступительная часть 1-2 мин
- •4. Закрепление 5 мин
- •Кпд цикла Карно
- •1. Вступительная часть 1-2 мин
- •Уроки - блоки
- •Примерные темы рефератов
- •Лабораторный практикум
- •Дополнительные задачи и вопросы
"Теория оказывается тем более впечатляющей, чем проще ее предпосылки,
чем значительнее разнообразие охватываемых ею явлений и чем шире
область ее применения. Именно поэтому классическая термодинамика
произвела на меня очень глубокое впечатление. Эта единственная общая
физическая теория, и я убежден, что в рамках применимости
своих основных положений она никогда не будет опровергнута".
А. Эйнштейн.



Выполнил Найдин А. А.
г. Новокузнецк, 2005 г.
"Вследствие малости частичек вещества
движение скрывается от взоров".

Урок 1. ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ
ЦЕЛЬ УРОКА: Дать общее представление о термодинамическом методе исследования тепловых явлений. Познакомить учащихся с алгоритмом (планом) изучения термодинамики. Ввести и дать определение понятия "Внутренняя энергия".
ТИПУРОКА: лекция.
ОБОРУДОВАНИЕ: Диафильм "Закон сохранения энергии в тепловых процессах", насос вакуумный, сосуд с пробкой, молоток, наковальня, кусок свинца, цифровой электрический термометр, зачетные папки по молекулярно – кинетической теории газов.
ПЛАН УРОКА:
1. Вступительная часть 1-2 мин
2. Обобщающее повторение 10 мин
3. Лекция 25 мин
4. Закрепление 5 мин
5. Задание на лом 2-3 мин
II. Обобщающее повторение по зачетной палке "Молекулярно-кинетическая теория газов", лист: "Выбери верный ответ".
III. Мы начинаем знакомиться с еще одной теорией тепловых явлений - термодинамикой ("терме" - теплота, "динамис" - сила). Возникновение термодинамики, как науки о процессах, происходящих в тепловых машинах, т.е. как науки о превращении тепла в работу. Ныне ее объектом являются практически любые процессы превращения материи, связанные с поглощением или выделением энергии, совершением работы, переносом вещества и т.д. Термодинамика изучает процессы расширения и сжатия, нагрева и охлаждения, плавления и отвердевания, испарения и конденсации. При этом она не вдается во внутреннее строение тел (вещество обладает такими свойствами, которые можно понять, не вдаваясь глубоко в его строение и не зная свойств его атомов). Термодинамические свойства - это свойства большой совокупности частиц, то есть объектом термодинамики является равновесная термодинамическая система. Термодинамика изучает тепловые явления, не вдаваясь во внутреннее строение тел.
По отношению ко всем этим процессам термодинамика отвечает на три главных вопроса:
Возможен ли данный процесс при данных условиях?
Если процесс возможен, то в каком направлении он пойдет?
Чем процесс закончится?
Пример с двумя макроскопическими телами, имеющими разные температуры и находящимися в тепловом контакте друг с другом.
Возможна передача энергии.
Направление передачи энергии от горячего тела к холодному.
Установление теплового равновесия.
Однако логичность и внутренняя согласованность термодинамики будет неполной до тех пор, пока не будет установлена ее связь с атомной моделью строения вещества. Эту связь надо установить.
Как мы будем изучать термодинамику?
Наблюдения и эксперименты → основные понятия → основные законы → формулы - следствия → практические применения.
Одно из основных понятий термодинамики - внутренняя энергия.
Тела обладают внутренней энергией. Она может увеличиваться или уменьшаться. Примеры. Вся энергия тела состоит из двух частей: макроскопической энергии и микроскопической. Макроскопическая энергия - механическая энергия. Микроскопическая энергия - "скрытая". Пример с двумя движущимися с одинаковой скоростью спичечными коробками, в одном из которых шарики неподвижны относительно коробка, а в другом - движутся с равными скоростями относительно коробка в противоположных направлениях.

![]()
![]()
Вывод не изменится, если будет отсутствовать корреляция между движениями шариков. Внутренняя энергия тела с точки зрения молекулярно-кинетических представлений:
![]()
Внутренняя энергия идеального одноатомного газа:
![]()
В общем случае внутренняя энергия включает в себя:
1. Суммарную кинетическую энергию поступательного и вращательного движения молекул;
2. Суммарную потенциальную энергию взаимодействия молекул;
3. Энергию колебательного движения атомов;
4. Энергию электронных оболочек атомов;
5. Внутриядерную энергию;
6. Энергию электромагнитного излучения, обеспечивающего тепловое равновесие между отдельными участками тела.
Полная энергия, запасенная в теле, измеряется произведением массы тела на квадрат скорости света в вакууме (СТО).
Внутренняя энергия (U) - свойство тела совершать работу или передавать количество теплоты окружающим телам при определенных условиях, измеряемое произведением массы тела на квадрат скорости света.
U=m∙c2 с = 3∙108 м/с
В термодинамике под внутренней энергией тела понимают ту часть его полной внутренней энергии, которая связана с движением и взаимодействием его частиц.
Энергия
распределяется равномерно по степеням
свободы, поэтому на одну степень свободы
приходится
![]() .
Молекулы идеального одноатомного газа
имеют i
= 3,
поэтому
.
Молекулы идеального одноатомного газа
имеют i
= 3,
поэтому
![]() ,
а средняя
энергия молекулы идеального двухатомного
газа
,
а средняя
энергия молекулы идеального двухатомного
газа
![]() (i
= 5),
так как молекула может еще и вращаться
относительно двух взаимно перпендикулярных
осей.
(i
= 5),
так как молекула может еще и вращаться
относительно двух взаимно перпендикулярных
осей.
У
твердых тел и многоатомных газов
![]() (i
= 6,
за исключением СО2,
у которого i
= 5).
(i
= 6,
за исключением СО2,
у которого i
= 5).
В
общем случае:
![]() .
.
Тепловое равновесие.
Температура (Т) - свойство равновесной термодинамической системы иметь одинаковую среднюю энергию, приходящуюся на одну степень свободы молекулы, прямо пропорциональное ей, измеряемое термометром в Кельвинах.
В каких случаях внутренняя энергия тела может изменяться? Демонстрации: нагревание куска свинца ударами молота, образование тумана при быстром расширении воздуха в сосуде и т.д.
Работу газа, или работу над газом, как и количество теплоты, можно измерить, и, следовательно, определить изменение внутренней энергии газа в конкретном процессе.
Зависимость внутренней энергии от макроскопических параметров тела? U=U (T, V).
У идеального газа: U=U (T).
IV. Задачи:
В баллоне находится аргон массой 5 кг при температуре 300 К. Какая полная энергия запасена в аргоне? Чему равна внутренняя энергия газа? Какую часть составляет внутренняя энергия от полной энергии, запасенной в аргоне?
Вычислите увеличение внутренней энергии 1 моля идеального одноатомного газа при увеличении его температуры на 1 К. Какую энергию необходимо сообщить газу для этого?
В цилиндре, закрытом подвижным поршнем, находится воздух. Во время опыта объем воздуха в цилиндре уменьшили в два раза, а его абсолютную температуру увеличили в два раза. Оказалось, однако, что воздух мог просачиваться сквозь зазор вокруг поршня, и за время опыта его давление в цилиндре повысилось только в 3 раза. Во сколько раз изменилась внутренняя энергия воздуха в цилиндре?
Воздух состоит в основном из азота и кислорода. Концентрация молекул азота при этом в 4 раза больше концентрации молекул кислорода. Чему равна кинетическая энергия вращения молекул азота, содержащегося в комнате объемом 60 м3? Атмосферное давление 105 Па.
Вопросы:
Почему выскакивают искры при ударе кремния о сталь?
Увеличивает ли сильный ветер температуру переносимого им воздуха?
Движущийся сосуд, содержащий некоторую массу идеального газа, внезапно останавливается. Что произойдет с давлением газа в сосуде?
В сосуде находится смесь азота и неона. Одинаковы ли средние кинетические энергии хаотического движения молекул этих газах?
Некий изобретатель объявил, что он придумал машину, которая позволяет из тонны угля получать энергию 9∙1019 Дж. Поверите ли вы этому заявлению?
При движении сосуда с газом относительно некоторой ИСО, в данной системе отсчета средняя скорость его молекул больше. Не означает ли это, что и температура газа в разных ИСО различна?
Внутренняя энергия идеального одноатомного газа определяется формулой
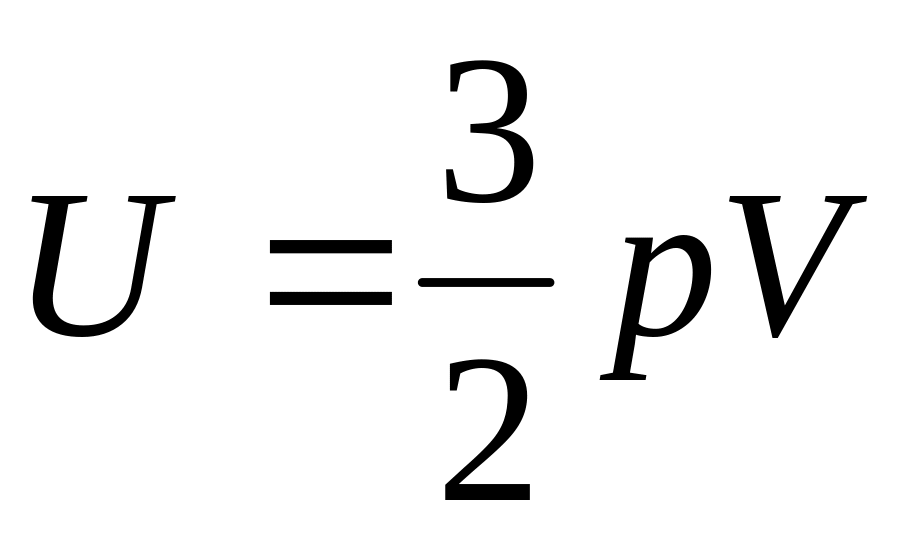 .
Объясните тогда, зачем мы топим печь,
ведь давление и объем газа в комнате
не изменяются, а, следовательно, не
меняется внутренняя энергия газа.
.
Объясните тогда, зачем мы топим печь,
ведь давление и объем газа в комнате
не изменяются, а, следовательно, не
меняется внутренняя энергия газа.Как изменились бы температура и внутренняя энергия двухатомного газа, если бы внезапно прекратилось бы взаимодействие атомов в молекулах?
V.
§ 23. Упр. 6, № 1.
Составьте обобщающую таблицу "Внутренняя энергия", используя рисунки, чертежи и текстовый материал.
Оцените, какую массу воды можно нагреть до кипения, если энергию, равную всей кинетической энергии молекул воздуха в комнате, передать воде, находящейся при комнатной температуре.
Определить на основании молекулярно — кинетической теории скорость изменения внутренней энергии идеального одноатомного газа при квазистатическом (медленном) передвижении со скоростью V поршня в цилиндре площадью S. Считать, что давление газа р известно в любой момент времени.
"И в этот час печальная природа
Лежит вокруг, вздыхая тяжело,
……………………………………..
И снится ей блестящий вал турбины,
И мерный звук разумного труда,
И пенье труб, и зарево платины,
И налитые током провода".
Н.А. Заболоцкий

Урок 2. РАБОТА В ТЕРМОДИНАМИКЕ
ЦЕЛЬ УРОКА: Развить представления учащихся о понятии "работа". Научить учеников определять изменение внутренней энергии термодинамической системы по изменению ее внешних параметров.
ТИП УРОКА: Комбинированный.
ОБОРУДОВАНИЕ: Стеклянный сосуд с пробкой, насос ручной, гальванометр, термопара, диафильм "Закон сохранения энергии в тепловых процессах", обобщающая таблица "Внутренняя энергия".
ПЛАН УРОКА:
