
- •1). Хранение наследственной информации. Наследственная информация – информация о белках организма, т.К. Белки – основа видовой специфичности.
- •Основные положения современной клеточной теории:
- •Строение эукариотической клетки:
- •Свойства мембран:
- •2. Немембранные органоиды:
- •Современные представления о возникновении жизни.
- •Химическая эволюция:
- •Аннотация
ТЕМА.
ХИМИЧЕСКИЙ СОСТАВ КЛЕТКИ.
Все клетки, независимо от уровня организации, сходны по химическому составу и строению. Это свидетельствует о единстве их происхождения.
УРОК №
ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ КЛЕТОК. НЕОРГАНИЧЕСКИЕ ВЕЩЕСТВА КЛЕТКИ.
ЦЕЛЬ: сформировать знания о химическом составе клеток
ЗАДАЧИ: дать характеристику химическому составу клетки: группам элементов, входящих в состав клетки; раскрыть значение воды, роль важнейших катионов и анионов в клетке.
ХОД УРОКА: изучение нового материала
Химические элементы клетки
В составе клетки обнаруживают 80 химических элементов периодической системы Д. И. Менделеева, функции 27 из них изучены. По количественному содержанию их подразделяют на 3 группы.
1. Макроэлементы, которые составляют основную массу вещества:
-- O, C, H, N – органогены, составляют 98% от общей массы
-- K, Na ,Ca, Mg, S, P, Cl, Fe составляют 1% от общей массы
2. Микроэлементы: Zn, Mn, Cu, Co, Mo, Br, I , составляют от 0,001 до 0,000001%
3. Ультрамикроэлементы : Au, U, Ra, Pb, Be и др., концентрация их не превышает 0,000001%. Их физиологическая роль не изучена.
Все химические элементы участвуют в построении организмов в виде ионов и соединений, которые подразделяются на неорганические и органические вещества.
Неорганические вещества клетки
Неорганические вещества клетки - вода и минеральные соли.
Вода составляет 70-80% от массы клетки, т.к. обладает уникальными физическими и химическими свойствами:
1. Основа внутренней (кровь, лимфа, межклеточная жидкость у животных) и внутриклеточной среды.
2. Вода - хороший растворитель (благодаря полярности молекул), различают:
– гидрофильные вещества – хорошо растворимые в воде (соли, сахара и спирты, имеющие ОН группу)
– гидрофобные вещества – нерастворимые в воде
3.Вода транспортирует вещества и у животных и у растений (благодаря оптимальному значению силы поверхностного натяжения, определяемого силами межмолекулярного сцепления) и внутри клетки.
4. Вода хороший реагент, она участвует в реакциях гидролиза (т.к. вода – диполь, т.е. имеет полюса с различными зарядами: О-, Н+ и это обуславливает расщепление молекул на анионы и катионы), а также метаболит ( реакции фотосинтеза)
5 Вода участвует в терморегуляции благодаря высокой теплоемкости и высокой теплопроводности (транспирация у растений и потоотделение у животных). Она сглаживает резкие температурные колебания внешней среды.
6.
Расширение при замерзании (благодаря
образованию каждой молекулой четырех
водородных связей). Максимальная
плотность при +
![]() С,
поэтому лед легче воды и образуется на
поверхности водоемов и выполняет функцию
теплоизоляции.
С,
поэтому лед легче воды и образуется на
поверхности водоемов и выполняет функцию
теплоизоляции.
7. Вода практически несжимаема (благодаря силам межмолекулярного сцепления), за счет этого поддерживается форма организмов (тургор, гидростатический скелет).
8. Вязкость воды (за счет водородных связей) обеспечивает смазывающие свойства воды (синовиальная жидкость, плевральная жидкость и др.)
Минеральные соли составляют 1-1,5%, входят в состав клеток, в основном, в виде ионов:
Важнейшие
катионы: K+,
Na+,
Ca2+,
Mg2+,
![]()
Ионы натрия и калия участвуют в создании и поддержании биоэлектрического потенциала на мембране (калий-натриевый насос). Причем на внешней поверхности мембран всегда много натрия, а внутри клетки много калия, это необходимейшее условие для нормальной жизнедеятельности клеток. Ионы натрия влияют на работу почек, поддерживают сердечный ритм, участвуют в поддержании осмотического потенциала клеток растений, что обеспечивает поглощение воды из почвы и др. Ионы калия участвуют в проведении нервного импульса, входят в состав ферментов, участвующих в фотосинтезе. Ионы кальция участвуют в синаптической передаче нервного импульса, процессе свертывания крови. Активируют ферменты при сокращении мышечных волокон, участвуют в формировании срединной пластинки между клетками и др. Магний входит в состав хлорофилла, образует пектиновые вещества, входит в состав ферментов, необходимых для работы мышечной, нервной и костной тканей.
Важнейшие
анионы:
![]() ,
,
![]() ,
,
![]() ,
,
![]()
Буферность- способность клетки сохранять определенную концентрацию ионов водорода , в клетке поддерживается слабощелочная реакция рН 7,2. Она поддерживается анионами слабых кислот и слабыми кислотами.
Анионы хлора поддерживают электронейтральность клетки, участвуют в формировании осмотического потенциала плазмы, входят в состав желудочного сока, регулируют тургорное давление.
УРОК №
ОРГАНИЧЕСКИЕ ВЕЩЕСТВА КЛЕТКИ. БЕЛКИ.
Цель: сформировать знания о химическом составе клеток
Задачи: продолжить расширение и углубление знаний о строении и функциях белков и их важной роли в органическом мире.
Ход урока: изучение нового материала
Органические вещества клетки – соединения, в которые входит углерод, образующий углеродный скелет; они встречаются только в живых системах или являются продуктами их жизнедеятельности. Это:
1. белки—10-20%
2. липиды – 1-5%
3. углеводы – 0,2 – 2,0%
4. нуклеиновые кислоты – 1,0—2,0%
5. низкомолекулярные органические вещества 0,1—0,5%
Многие органические соединения имеют большой размер молекул и называются макромолекулами. Среди них много биополимеров, это молекулы, которые состоят из повторяющихся сходных по структуре низкомолекулярных соединений, ковалентно связанных между собой – мономеров. Природные полимеры бывают:
-- регулярные, они состоят из мономеров одного вида (крахмал, гликоген, клетчатка, хитин и др.)
-- нерегулярные, они состоят из мономеров одного типа, но разных видов (белки, нуклеиновые кислоты)
Свойства полимеров зависят от количества, качества мономеров и пространственной структуры молекулы.
БЕЛКИ.
Белки – протеины (состоят только из аминокислот) и протеиды (сложные белки, содержащие и небелковую группу). Они получили свое название от греческого слова protos – первый, главный, т.к. составляют 10-20% от сырой массы и 50-80% от сухой массы клетки и имеют первостепенное значение для живых систем (табл. определение жизни).
Белки – это нерегулярные полимеры, мономерами которых являются аминокислоты, их 20 (Н.Н.Любавин, 1871г.). Некоторые из них не синтезируются в организме человека и поступают только с пищей животного происхождения. Они называются незаменимыми: валин, метионин, треонин, лейцин, изолейцин, фенилаланин, триптофан, лизин; а у детей – аргинин и гистидин. Поэтому строгое вегетарианство (полное исключение животной пищи) очень опасно для здоровья людей, особенно детей, т.к. роль белка не ограничивается только пластическими функциями; нарушается образование ферментов, гормонов, деятельность ЦНС. Поэтому наблюдается отставание в физическом и интеллектуальном развитии. Из растений только соя содержит все необходимые аминокислоты.
Общая формула аминокислот:

СООН – карбоксильная группа, обладающая кислотными свойствами
![]() --
аминнная группа,
обладающая свойствами оснований.
--
аминнная группа,
обладающая свойствами оснований.
Следовательно, аминокислоты – амфотерные соединения, совмещающие свойства кислот и оснований, этим обусловлена их способность взаимодействовия друг с другом. Аминокислоты легко соединяются и образуют связи между углеродом кислотной и азотом основной групп. Эти связи называются ковалентными или пептидными и поэтому термин «белки» часто заменяют термином «полипептиды».
Уровни организации белковой молекулы:
Первичная структура – цепь из аминокислот, соединенных ковалентной связью. Она еще не способна выполнять специфические функции.
Вторичная структура – спираль, образованная водородными связями между остатками карбоксильной группы одной аминокислоты и остатком аминной группы другой аминокислоты, удаленной от первой на 4 аминокислотных остатка. В этой структуре работают только некоторые сократительные белки.
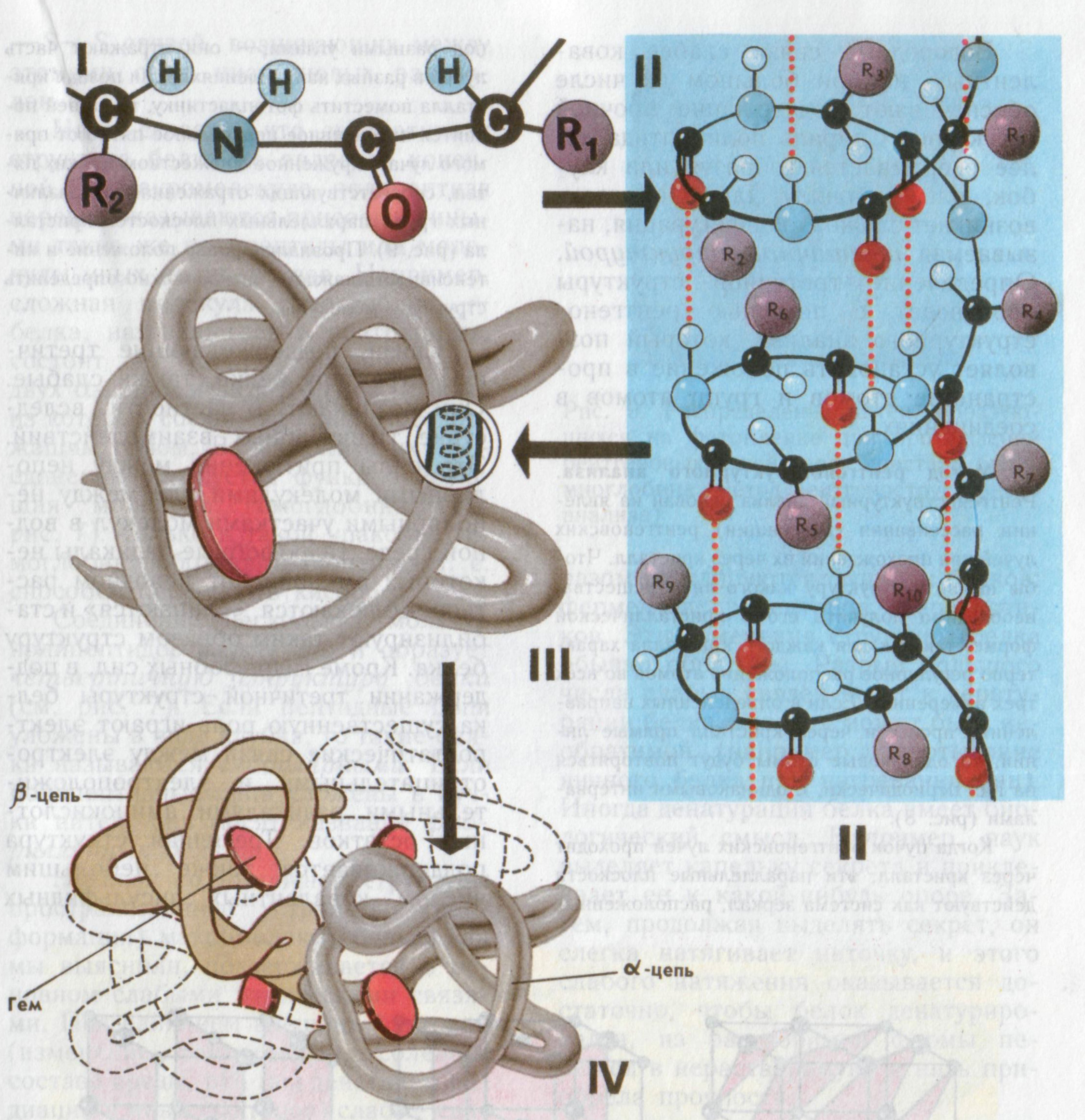 Третичная
структура
– глобула
(шар),
образованная гидрофобным взаимодействием
между радикалами некоторых аминокислот
и дисульфидными связями между атомами
серы, которые входят в состав радикалов
цистеина и метионина.
Третичная
структура
– глобула
(шар),
образованная гидрофобным взаимодействием
между радикалами некоторых аминокислот
и дисульфидными связями между атомами
серы, которые входят в состав радикалов
цистеина и метионина.
Четвертичная структура – молекула, состоящая из 2-4 глобул, образованная межмолекулярным притяжением (ковалентные, водородные и ионные связи), если полипептидные цепи уложены в пучки нитей, то они называются фибриллярными белками (гемоглобин, состоящий из 4 глобинов; инсулин, состоящий из 2 молекул коллаген – фибриллярный белок.)
Структура белковых молекул была изучена с помощью метода рентгеноструктурного анализа.
Из-за сложности строения белковых молекул, малейшие изменения в структуре приводят к значительным изменениям свойств белков.
Свойства белка:
1. Белки гидрофильны и проявляют свою функциональную активность только в растворах.
2. Они несут большой поверхностный заряд.
3 Белки термолабильны, т.е. проявляют свою активность только в узких температурных рамках.
.Денатурация (лат. denatyrate – лишить природных свойств) – утрата белком своей структурной организации идет от четвертичной структуры до первичной из-за изменения температуры, рН, обезвоживания и др. причин. Если параметры вернулись к физиологической норме, а первичная структура не успела разрушиться ( из-за прочности ковалентных связей требуется больше времени на их разрушение), то возможна ренатурация- воссоздание структуры молекулы и ее функций.
Функции белков:
1 Структурная, строительная или пластическая, т.к. белки - это основной строительный материал клетки. Входят в состав капсидов вирусов и клеточных мембран; коллаген – компонент соединительной ткани; кератин, который входит в состав волос, шерсти, перьев, рогов, копыт, ногтей, когтей; склеротин, входящий в состав наружного скелета насекомых и др.
2. Каталитическая, т.к. все природные ферменты являются белками. Они обладают высочайшей специфичностью и работают только в очень узком диапазоне параметров, соответствующем физиологическим нормам. В состав многих ферментов входят витамины – кофакторы. У ферментов работает только активный центр, который в момент осуществления реакции приобретает определенную пространственную структуру - «замок». Его конфигурация точно соответствует какой – либо молекуле – «ключ» (Фишер, 1890г., гипотеза «ключа и замка») Вначале реакции происходит соединение фермента с субстратом и образуется фермент – субстратный комплекс, далее субстрат преобразуется и образуется комплекс фермента с видоизмененным субстратом. Далее происходит в активном центре собственно реакция и образуется фермент – продуктный комплекс. После окончания реакции комплекс распадается и освобождается продукт, а фермент восстанавливается. Молекула фермента не вступает в реакцию, не разрушается; она слегка видоизменяется в момент осуществления реакции, а затем восстанавливает свою структуру. Скорость ферментативных реакций зависит, в основном, от количества фермента. На скорость реакции и активность фермента влияет температура (оптимальная от25 до 40 С), рН среды и различные низкомолекулярные вещества, одни из которых повышают активность фермента (ионы металлов), другие (ингибиторы) замедляют (некоторые яды). Большинство ферментов имеют в своем названии окончание – аза.
3. Регуляторная или рецепторная (все гормоны, кроме половых, имеют белковую природу; гликопротеины мембран, родопсин и йодопсин – светочувствительные пигменты, фитохром растений, отвечающий за фотопериодизм у растений)
4. Транспортная (активный транспорт и облегченная диффузия через мембраны, гемоглобин и гемоцианин переносят кислород и углекислый газ у позвоночных и беспозвоночных животных).
5. Двигательная (тубулины микротрубочек, флагеллин обеспечивает движение жгутиков прокариот; актин и миозин обеспечивают сокращение поперечнополосатых мышц)
6. Защитная (антитела, интерфероны – универсальные противовирусные белки; тромбопластин, протромбин, тромбин и фибриноген обеспечивают свертываемость крови).
7. Запасающая (миоглобин содержит запас кислорода в мышцах позвоночных; альбумин запасает воду в яичном желтке; белки семян растений семейства бобовых – источник питания для зародыша)
8. Энергетическая, т.к. 1 гр. белка при распаде выделяет 17 кДж
9. Токсины микробов (ботулинический, столбнячный, дифтерийный, холерный); токсины змей, пауков, скорпионов; токсины грибов, пчел являются белками.
УРОК №
УГЛЕВОДЫ.
Цель: сформировать знания о химическом составе клеток
Задачи: продолжить расширение и углубление знаний о строении и функциях углеводов и их важной роли в органическом мире.
Ход урока: изучение нового материала
Углеводы – органические вещества, в состав которых входят углерод,
кислород и водород, при этом Н:О = 2:1 как в молекуле воды. Общая формула углеводов Сn (Н2 О)n , где n не меньше 3. Отсюда термин «углеводы», который впервые ввел К.Шмид в 1844г. В животных клетках углеводы составляют 2 – 5% от массы, а в растительных клетках до 90%.
Углеводы подразделяются на две группы:
1. Моносахариды или монозы, простые сахара Сn (Н2 О)n. Это кристаллы, хорошо растворимые в воде и сладкие на вкус. В зависимости от числа углеродных атомов, различают:
а) триозы, где n= 3 (глицерин и его производные: молочная и пировиноградная кислоты; они оптические изомеры.)
б)
тетрозы, где n=
4 (эритроза – один из промежуточных
продуктов фотосинтеза.)![]()
в) пентозы, где n= 5 (рибоза и дезоксирибоза, входящие в состав мономеров нуклеиновых кислот.).
г) гексозы, где n= 6 (глюкоза, фруктоза, галактоза – оптические изомеры, они широко распространены в природе).
11. Полисахариды – полимеры, мономерами которых являются моносахариды. Их подразделяют на две группы:
-- гомополосахариды – имеют моносахариды одного вида
-- гетерополисахариды – имеют моносахариды различных типов и их производных.
Общая
форм
![]() Сn
(Н2О)n
m,
где m
– число мономеров и, в зависимости от
их числа , различают:
Сn
(Н2О)n
m,
где m
– число мономеров и, в зависимости от
их числа , различают:
1) полисахариды первого порядка или олигосахариды, они имеют от 2 до 10 остатков моносахаридов, соединенных ковалентной связью. Они еще сладкие на вкус и хорошо растворимы в воде. В природе особенно распространены дисахариды:
а) сахароза = глюкоза + фруктоза, тростниковый или свекловичный сахар, играет огромную роль в питании человека и животных.
б) лактоза = глюкоза + галактоза, молочный сахар, источник питания для детенышей млекопитающих.
в) мальтоза = глюкоза + глюкоза, солодовый сахар, основной структурный компонент крахмала и гликогена.
2) полисахариды второго порядка – высокомолекулярные углеводы, состоящие из большого числа моносахаридов. Они плохо или вообще не растворимы в воде и не сладкие на вкус. Эти свойства углеводов изменяются в зависимости от числа мономеров. Широко распространены в природе следующие полисахариды:
а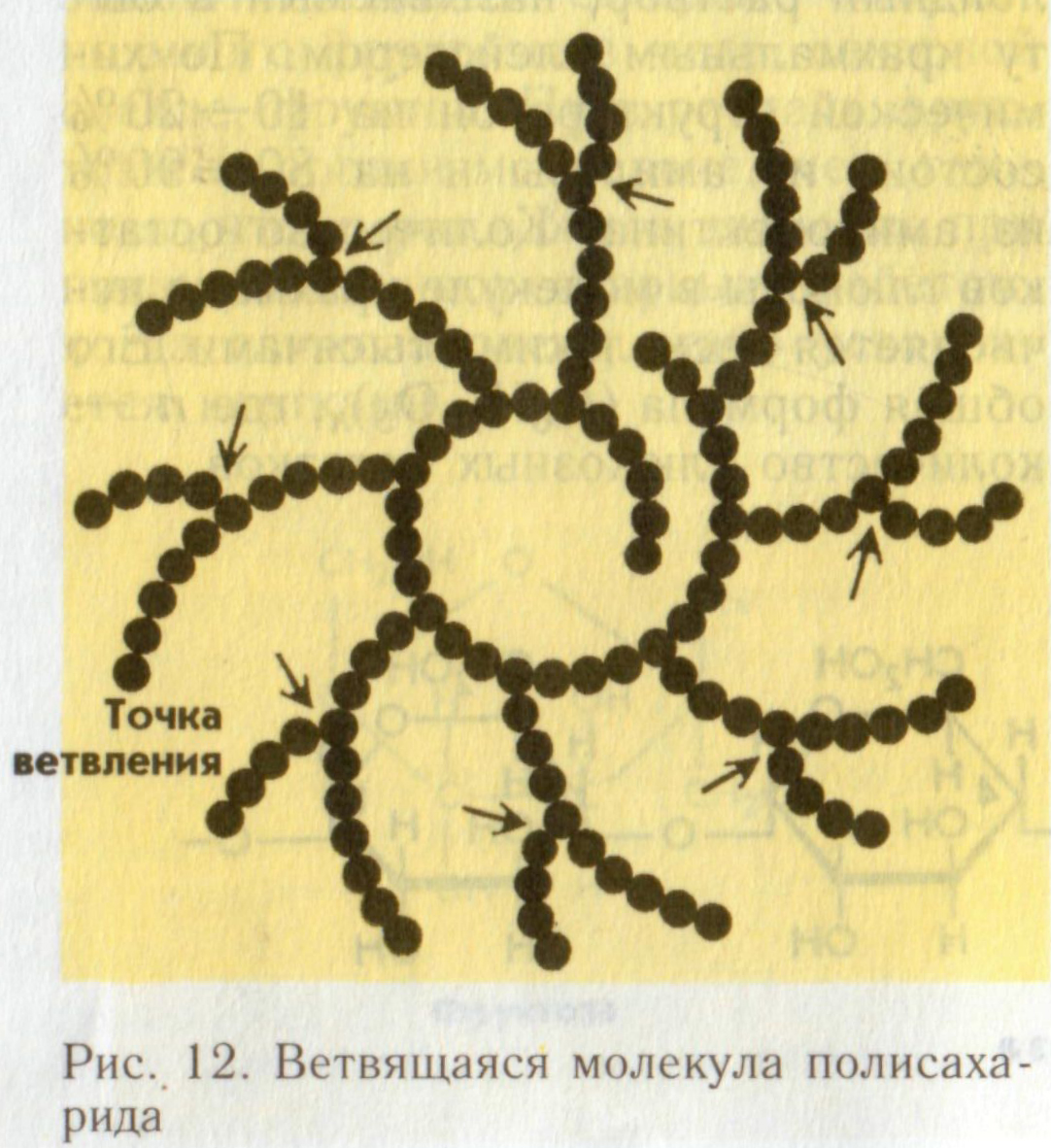 )
крахмал – разветвленный резервный
гомополисахарид растений
)
крахмал – разветвленный резервный
гомополисахарид растений
б) гликоген – разветвленный резервный гомополисахарид животных , грибов, бактерий, по структуре напоминает крахмал, но разветвлен сильнее.
в) клетчатка или целлюлоза – линейный, структурный гомополисахарид растений, клеточная стенка растений, в ней аккумулировано более 50% всего углерода биосферы.
г) хитин – линейный, структурный гомополисахарид животных и грибов
д) муреин – сеть гетерополисахаридных цепей, соединенных белковыми молекулами, клеточная стенка бактерий.
е) групповые вещества крови человека (агглютинины и агглютиногены) – олигосахаридные цепочки, соединенные с белком, придают специфичность эритроцитам и препятствуют агглютинации.
Функции углеводов:
1. Энергетическая (глюкоза является одним из наиболее распространенных дыхательных субстратов).
2. Структурная, пластическая или строительная (углеводы входят в состав оболочек клеток и субклеточных образований, у растений выполняют и опорную функцию).
3. Резервная или запасающая (сахароза, фруктоза, глюкоза запасаются в клеточном соке; крахмал, гликоген, клетчатка запасаются в клетках и при необходимости гидролизуются до глюкозы).
4. Защитная (вязкие слизи – муцины защищают стенки полых органов).
УРОК №
ЛИПИДЫ.
Цель: сформировать знания о химическом составе клеток
Задачи: продолжить расширение и углубление знаний о строении и функциях липидов и их важной роли в органическом мире.
Ход урока: изучение нового материала
![]() Липиды –
органические соединения с различной
структурой, но общими свойствами. Они
нерастворимы в воде, но хорошо растворимы
в органических растворителях: эфире,
бензине, хлороформе и др. В живых клетках
липиды распределены неравномерно, есть
клетки жировой ткани, в которых их
содержится до 90%, а в других их 5% от сухой
массы.
Липиды –
органические соединения с различной
структурой, но общими свойствами. Они
нерастворимы в воде, но хорошо растворимы
в органических растворителях: эфире,
бензине, хлороформе и др. В живых клетках
липиды распределены неравномерно, есть
клетки жировой ткани, в которых их
содержится до 90%, а в других их 5% от сухой
массы.
Липиды подразделяются на две группы:
1. Жиры
2. Липоиды
Жиры – сложные соединения трехатомного спирта глицерина и высокомолекулярных жирных кислот. Общая формула:
О
СН2 – О – С – R |
| О
СН – О – С – R
| О
СН2 – О – С – R
Молекула жира состоит из гидрофильной глицериновой «головки» и трех «хвостов» жирных кислот, которые обладают гидрофобными свойствами. Поэтому жиры образуют пленку на воде: глицерин обращается к воде, а жирные кислоты от воды. Жирные кислоты имеют линейную структуру и все начинаются с карбоксильной группы. Все жирные кислоты подразделяются на две группы:
1. насыщенные – не содержат двойные связи
2. ненасыщенные – содержат двойные связи
Свойства жиров определяются качественным составом жирных кислот и их количественным соотношением. В зависимости от этого все жиры подразделяются на следующие группы:
1) твердые животные жиры теплокровных животных содержат только насыщенные жирные кислоты, они имеют высокую температуру плавления и при комнатной температуре находятся в твердом состоянии. У хладнокровных животных помимо насыщенных жирных кислот могут быть и ненасыщенные, причем их сочетание может изменяться в зависимости от температуры окружающей среды: зимой – ненасыщенные, летом – насыщенные.
2) жидкие растительные жиры или масла содержат только ненасыщенные жирные кислоты, они имеют низкую температуру плавления и при комнатной температуре жидкие. Замерзают (переходят в твердое состояние) только при очень низкой температуре.
3) мягкий человеческий жир содержит одну ненасыщенную жирную кислоту, этим объясняется необходимость употребления жиров и животного и растительного происхождения. Тогда синтез жира, который идет и в эпителии тонкого кишечника и в полостях гладкой ЭПС идет без лишних энергозатрат на перестройку жирных кислот.
Липоиды – жироподобные вещества, подразделяются на следующие группы:
1.Простые липиды, в их состав вообще не входят жирные кислоты. К ним относятся:
-- стероиды – производные холестерина
-- терпены
-- жирорастворимые витамины К,Е, Д,А
2.Воски
3. Фосфолипиды, которые содержат две молекулы жирных кислот и один остаток фосфорной кислоты. Они основные компоненты клеточных мембран.
4. Гликолипиды = липид + углевод, входят в состав нервной ткани.
5. Липопротеиды = липид + белок
Функции липидов:
1. Структурная, пластическая или строительная (фосфолипиды, холестерин, липопротеины и гликолипиды входят в состав мембран; зрительный пурпур является липопротеином; пигменты каратиноиды, участвующие в фотосинтезе, являются терпенами)
2. Энергетическая, т.к. 1 гр. жира при распаде выделяет 38,9 кДж.
3. Резервная или запасающая (жиры – основные запасные вещества животных и растений; жиры – источник метаболической воды).
4. Регуляторная (половые гормоны – производные холестерина; жирорастворимые витамины; терпены – душистые вещества растений, привлекающие насекомых).
5. Терморегуляторная (жир обладает низкой теплопроводностью, бурый жир играет роль биологического подогревателя.)
6 Защитная (жир является амортизатором, воски обладают водоотталкивающим свойством и защищают растения от ожогов).
УРОК №
НУКЛЕИНОВЫЕ КИСЛОТЫ. ДНК.
Цель: сформировать знания о химическом составе клеток
Задачи: продолжить расширение и углубление знаний о строении и функциях ДНК и их важной роли в органическом мире
Ход урока: изучение нового материала
Нуклеиновые кислоты – природные высокомолекулярные органические соединения, обеспечивающие хранение и передачу наследственной (генетической) информации в живых организмах. Были открыты Ф. Мишером в 1869 г., он назвал выделенное из гноя вещество нуклеином, полагая, что оно содержится лишь в ядре. В природе существуют нуклеиновые кислоты двух типов: ДНК и РНК.
ДНК
Д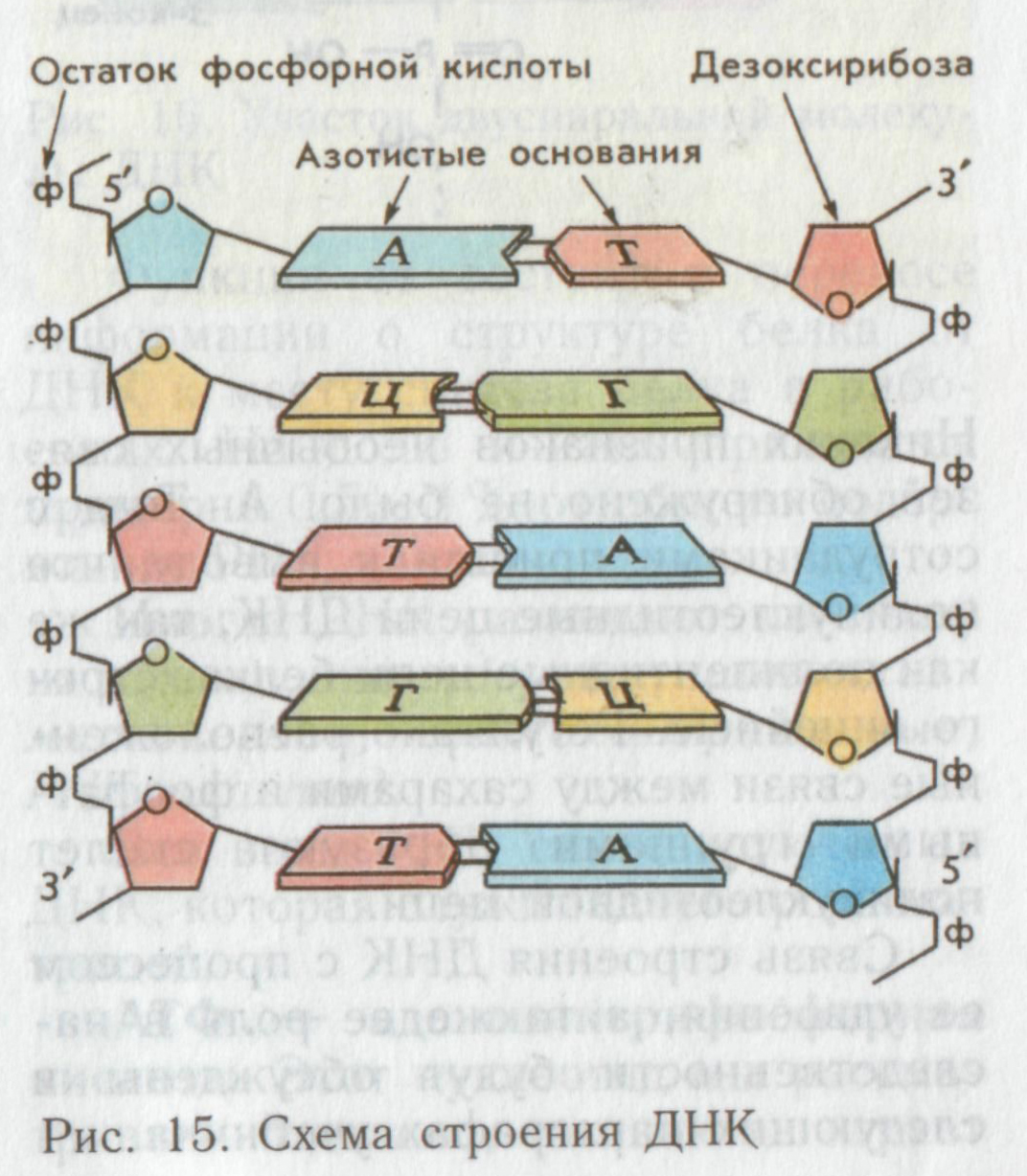 НК
– дезоксирибонуклеиновая кислота
– полимер, состоящий из мономеров –
нуклеотидов, которые состоят из трех
компонентов:
НК
– дезоксирибонуклеиновая кислота
– полимер, состоящий из мономеров –
нуклеотидов, которые состоят из трех
компонентов:
1. дезоксирибоза С5Н10О4 - обезкислороженная рибоза
2. одно из четырех возможных азотистых оснований:
а) А – аденин
б) Г – гуанин А, Г – пуриновые основания
в) Т – тимин
г) Ц – цитозин Т, Ц – пиримидиновые основания
3. остаток фосфорной кислоты Н3 РО4
Нуклеотид состоит из трех разных веществ, которые соединены ковалентной связью. Между собой нуклеотиды тоже соединены ковалентной связью в длинные цепи. Цепь – это первичная структура ДНК.
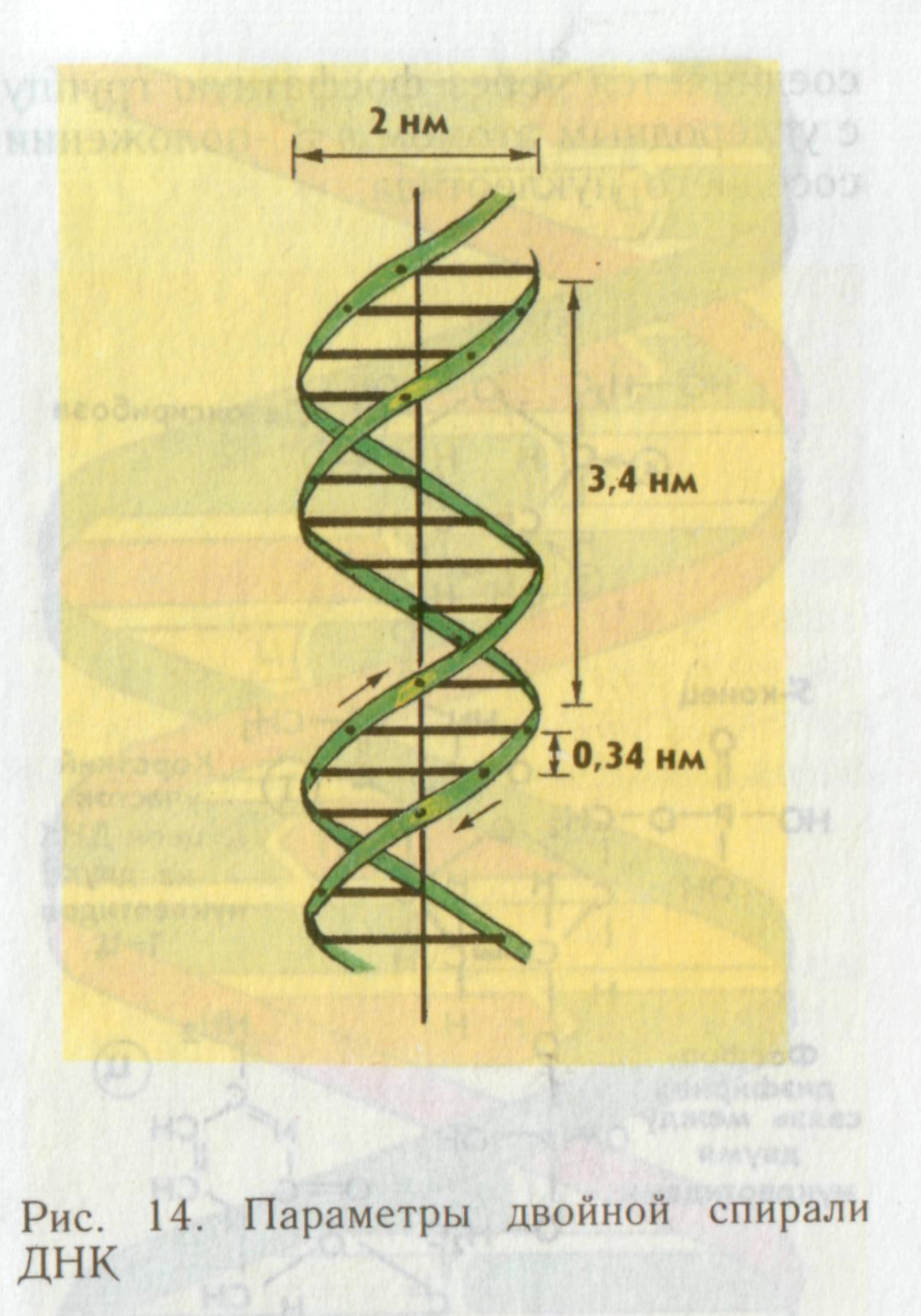
ДНК – двойная правозакрученная спираль, состоящая из двух цепей; закрученных относительно друг друга и общей оси (Дж. Уотсон и Ф. Крик, 1953г.). Это вторичная структура. Цепи всегда ориентированы т.о., что сахаро – фосфатный остов - кнаружи; а азотистые основания – кнутри. Это объясняется тем, что цепи удерживаются относительно друг друга водородными связями, которые возникают между азотистыми основаниями по принципу комплементарности (дополнительности) А- - Т (двойная водородная связь), Г- - Ц (тройная водородная связь). Принцип комплементарности объясняет правило Э. Чаргаффа (1905г.):
-- число пуриновых оснований равно числу пиримидиновых,
- -
количесто аденина всегда равно количеству
тимина, количество гуанина – количеству
цитозина.
-
количесто аденина всегда равно количеству
тимина, количество гуанина – количеству
цитозина.
Правильную пространственную взаимную ориентацию азотистых оснований обеспечивает противоположная полярность двух цепей: одна из них ориентирована в 3-5 – направлении, вторая в 5-3 – направлении; т.е. цепи ДНК антипараллельны. Двойная спираль ДНК – это ее вторичная структура.
Третичная структура ДНК – нуклеопротеины – соединение нуклеиновых кислот с белками. При соединении ДНК с определенными белками (гистонами) степень спирализации молекулы повышается – возникает суперспираль ДНК, толщина которой существенно возрастает, а длина сокращается – это хромосома.
Хромосомный материал в покоящихся неделящихся клетках называется хроматин. Он содержит 60% белка (гистоновой -35% и остальные негистоновой природы), 35% ДНК и 5% РНК. Взаимодействие белков с нуклеиновыми кислотами электростатическое: положительно заряженные аминокислоты и отрицательно заряженные фосфатные группы ДНК.
Функции ДНК:
1). Хранение наследственной информации. Наследственная информация – информация о белках организма, т.К. Белки – основа видовой специфичности.
Триплет или кодон – три последовательно соединенных нуклеотида, каждый триплет кодирует одну аминокислоту. Их 43 = 64, из них 61 являются кодирующими, а 3 – «знаками препинания».
Ген – участок молекулы ДНК, несущий информацию о первичной структуре одного белка.
Т.к. информация о первичной структуре белка записана в гене, она называется генетической. ДНК – материальный носитель генетической информации и она записана в виде генетического кода.
Генетический код – система записи информации о последовательности расположения аминокислот в белках с помощью последовательности расположения нуклеотидов в нуклеиновых кислотах (ДНК, РНК). Он обладает следующими свойствами:
1. Код триплетен (число нуклеотидов кратно 3).
2. Код вырожден (избыточен), т.к. одна аминокислота кодируется несколькими триплетами.
3. Код однозначен, т.к. каждый триплет кодирует только одну аминокислоту.
4. Код универсален, т.е. един для всего живого на Земле.
5. Между генами имеются «знаки препинания».
5. Внутри генов нет «знаков препинания.
2) Передача наследственной информации реализуется в трех типах реакций матричного синтеза (биосинтез белка – реализация наследственной информации):
-- репликация (удвоение) или редупликация (самоудвоение) ДНК
-- транскрипция (списывание, считывание) – синтез РНК по матрице ДНК
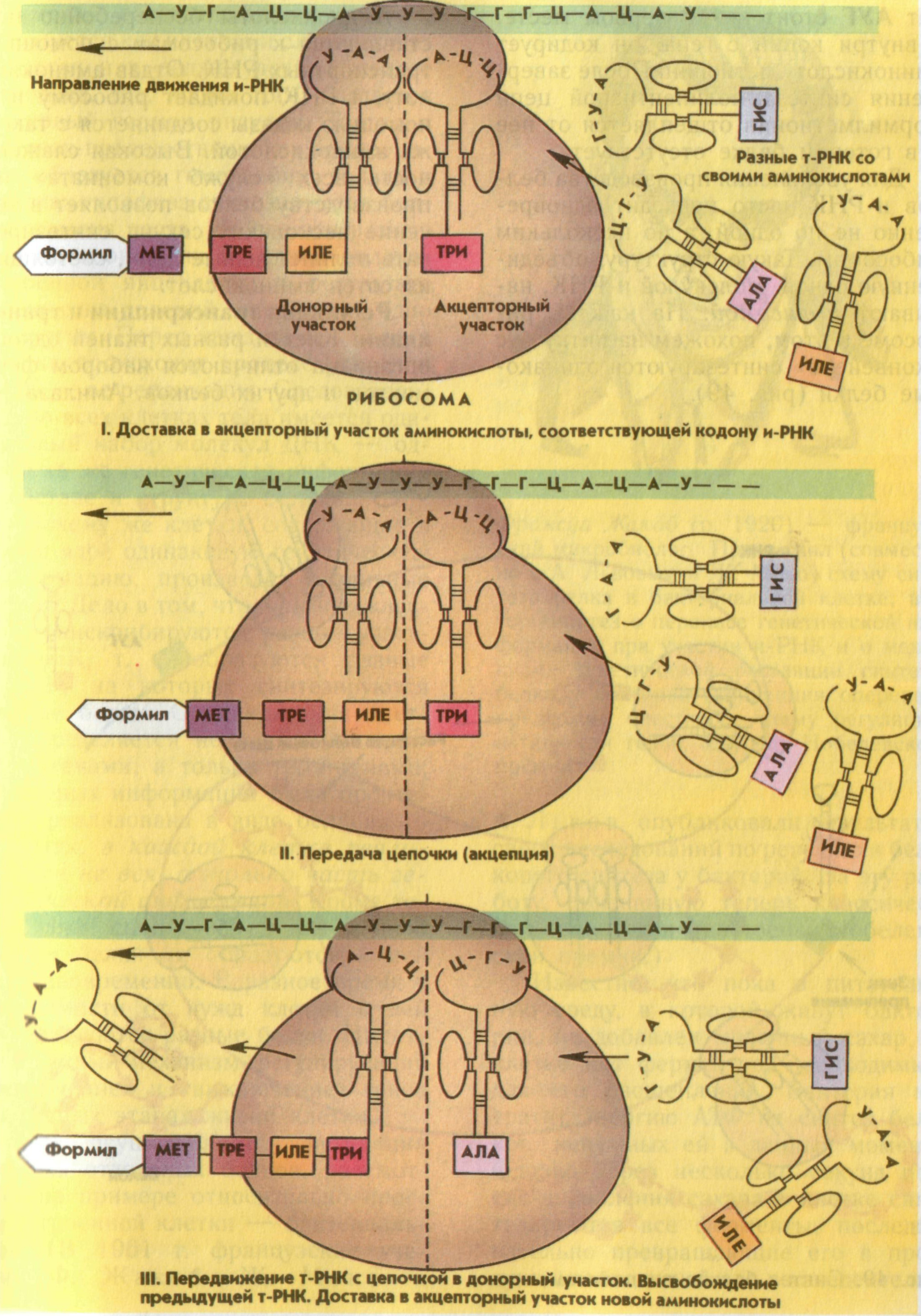
-- трансляция (передача, перевод) – синтез белка по матрице иРНК.
Процесс репликации протекает в три стадии:
Стадия 1 – инициация, начинается с того, что цепи ДНК раскручиваются с помощью ферментов – хеликаз и между ними рвутся водородные связи с помощью ферментов - гидраз. Образуются репликативные вилки – это цепи ДНК, которые разошлись в стороны. К каждой из цепей присоединяются ДНК – связывающие белки (ДСБ), которые препятствует образованию комплементарных пар и обратному воссоединению цепей.
Под действием ДНК- зависимой РНК- полимеразы синтезируются РНК- «затравки» (праймеры), которые после завершения синтеза отделяются от ДНК.
Стадия 2 – элонгация. На этой стадии происходит собственно синтез ДНК. По принципу комплементарности на каждой цепи ДНК выстраиваются нуклеотиды. Самокопирующий фермент ДНК-полимераза, передвигаясь по репликационной вилке, соединяет между собой нуклеотиды в направлении от 5 к 3 – концу. Движение фермента идет только в одном направлении. Т.к. цепи ДНК антипараллельны, то по другой цепи ДНК – полимераза движется в обратном направлении. Репликационная вилка оказывается несимметричной, Одна из дочерних ДНК (ведущая) строится непрерывно, а другая (отстающая) – синтезируется прерывисто, в виде отдельных фрагментов, которые позже сшиваются с помощью фермента ДНК-лигазы.
В ходе всего процесса синтеза репликативная вилка перемещается вдоль молекулы и при этом расплетаются новые участки родительской ДНК до тех пор, пока вилка не дойдет до точки окончания синтеза – точки терминации. Скорость наращивания составляет 1500 нуклеотидов в секунду.
Стадия3 – терминация. С вновь синтезированной молекулы ДНК снимаются все белковые факторы, ферменты, Две дочерние молекулы ДНК расходятся, спирализуются и приобретают соответствующую структуру.
Т. к. при образовании новых молекул ДНК используется «старая» цепь и одна «новая» достраивается по принципу комплементарности, то гипотеза, .сформулированая Дельбруком и Стентом в 1957г. получила название полуконсеративной репликации
Весь процесс репликации происходит за счет энергии АТФ.
УРОК№
РНК.
Цель: сформировать знания о химическом составе клеток
Задачи: продолжить расширение и углубление знаний о строении и функциях РНК и их важной роли в органическом мире
Ход урока: изучение нового материала
РНК – рибонуклеиновая кислота – одноцепочный полимер, состоящий из мономеров – нуклеотидов, которые в отличие от нуклеотидов ДНК содержат нормальную рибозу С5Н10О5, а вместо тимина – урацил. По выполнению функций выделяют три вида РНК:
1. иРНК - информационные или мРНК – матричные содержится в ядре и цитоплазме. Она переносит информацию о первичной структуре белка из ядра в цитоплазму, к рибосомам, т.е. является матрицей для синтеза белка в процессе трансляции. Этих РНК меньше всего в клетке по количеству, т.к. каждая из них используется многократно; но они разнообразнее остальных.
2. тРНК – транспортные РНК содержится в основном в цитоплазме клеток. Это короткие РНК, состоят из 80-100нуклеотидов. Осуществляют свои функции только во вторичной структуре, образованной водородными связями, имеет три петли – «трилистник». В центре средней петли имеется триплет – антикодон, который образует водородные связи с кодонами РНК в процессе трансляции. К свободному концу тРНК присоединяется только та аминокислота, которая соответствует антикодону. По числу аминокислот существует 20 видов тРНК, а по числу антикодонов – 61. Функция тРНК состоит в переносе аминокислот в рибосомы, к месту синтеза белка.
3. рРНК – рибосомные РНК, содержатся в ядре и цитоплазме. Это крупные РНК, входят в состав рибосом. Этих рибосом больше всего в клетке, они составляют 90% от общего числа, но они наименее разнообразные. Их функция состоит в том, чтобы в процессе трансляции соединять аминокислоты друг с другом и отделять их от тРНК.
Иногда РНК выделяют по месту их нахождения: ядерные, цитоплазматические, митохондриальные, РНК пластид.
Все виды РНК транскрибируются (списываются, считываются), т.е. синтезируются с матрицы ДНК в ядре, а затем через поры в ядерной оболочке выводятся в цитоплазму.
Транскрипция осуществляется у прокариот и у эукариот примерно одинаково. Существуют следующие современные представления о гене:
 Элементарной
единицей транскрипции является оперон
(у прокариот) или транскриптон (у
эукариот). Он состоит из промотора
– посадочной площадки для фермента
РНК- полимеразы. Только присоеденившись
к промотору, РНК- полимераза способна
начать синтез РНК. Дальше расположен
оператор
– участок ДНК, к которому присоеденены
белки – репрессоры. Синтез РНК возможен
только в том случае, если белки, связанные
с молекулой субстрата, отделяются от
оператора и освобождают дорогу РНК –
полимеразе. Далее в опероне расположена
структурная
зона, которая состоит из чередующихся
экзонов (Э) и интронов (И). Интроны, не
несущие информацию, в процессе синтеза
удаляются («вырезаются»), а экзоны –
несущие информацию, сшиваются (сплайсинг).
В процессе транскрипции можно выделить
четыре стадии:
Элементарной
единицей транскрипции является оперон
(у прокариот) или транскриптон (у
эукариот). Он состоит из промотора
– посадочной площадки для фермента
РНК- полимеразы. Только присоеденившись
к промотору, РНК- полимераза способна
начать синтез РНК. Дальше расположен
оператор
– участок ДНК, к которому присоеденены
белки – репрессоры. Синтез РНК возможен
только в том случае, если белки, связанные
с молекулой субстрата, отделяются от
оператора и освобождают дорогу РНК –
полимеразе. Далее в опероне расположена
структурная
зона, которая состоит из чередующихся
экзонов (Э) и интронов (И). Интроны, не
несущие информацию, в процессе синтеза
удаляются («вырезаются»), а экзоны –
несущие информацию, сшиваются (сплайсинг).
В процессе транскрипции можно выделить
четыре стадии:
1. связывание РНК – полимеразы с промотором
2. инициация – начало синтеза, она заключается в образовании фосфодиэфирной связи между АТФ и вторым нуклеотидом синтезирующейся молекулы РНК.
3. элонгация – рост цепи РНК, т.е. последовательное присоединение нуклеотидов друг к другу в соответствии с принципом комплементарности (50 нуклеотидов в сек.)
4. терминация – завершение или окончание синтеза РНК.
Т.о. функция РНК – передача наследственной информации.
АТФ – аденозинтрифосфорная кислота – адениловый нуклеотид РНК, который содержит вместо одного три остатка фосфорной кислоты, соединенных макроэргическими (энергоемкими) связями. АТФ – универсальный аккумулятор энергии. При отщеплении одного остатка фосфорной кислоты под действием фермента АТФ- азы освобождается 419 кДж\ моль и образуется АДФ – аденозиндифосфорная кислота, при отщеплении второго - образуется АМФ – аденозинмонофосфорная кислота. Реакции обратимы, основной синтез АТФ происходит в митохондриях.
Д.з. В.Н.Фросин, в.И.Сивоглазов «Химический состав клетки»,стр. 4
УРОК№
КЛЕТОЧНАЯ ТЕОРИЯ.
ЦЕЛЬ: сформировать представление о единстве всего живого
ЗАДАЧИ: познакомить учащихся с краткой историей изучения клетки; раскрыть основные положения современной клеточной теории; закрепить умение применять эти положения для доказательства материального единства органического мира; показать роль научно – технических достижений в изучении клеток. ХОД УРОКА: изучение нового материала.
Проверка знаний и умений: анализ зачета «Химический состав клетки», выставление оценок (10 мин.).
Изучение нового материала:
Создание клеточной теории. История изучения клетки неразрывно связана с развитием микроскопической техники.
1590 - Янсен изготовил первый микроскоп.
1665г.- физик Р. Гук изучал под микроскопом срез пробки бузины и увидел множество мелких образований (ячеек), которые он назвал клетками.
Естествоиспытатель – самоучка, голландец А. ван Левенгук, исследуя настой (лат.infusum) сена (инфузории), семенную жидкость («анималькусы») зубной налет, кровь лягушки, скелетные мышцы с помощью микроскопа, обнаружил микроскопически малые биологические объекты («Тайны природы, открытые при помощи микроскопа»). В 1674г. были открыты бактерии и простейшие. В 1676 г. описаны пластиды и хроматофоры. В 1677г. впервые увиден сперматозоид человека.
Микроскопические исследования были продолжены. Появление микроскопа в России связывают с путешествием Петра 1 по Европе в 1698г. М.В. Ломоносов широко применял микроскоп в своих исследованиях и внес свой вклад в дело усовершенствования этого прибора.
Лишь в девятнадцатом веке ученые обратили внимание на полужидкое студенистое содержимое, заполняющее клетку. Появились хорошие микроскопы, были разработаны методы фиксации и окраски клеток.
1831г. – Р. Броун открыл клеточное ядро.
В 1838г. ботаник М. Шлейден пришел к выводу, что ткани растений состоят из клеток, Зоолог Т. Шванн показал, что из клеток состоят и ткани животных и в 1839г. он сформулировал клеточную теорию:
-- клетка – элементарная структурная единица строения всех живых существ;
-- клетки растений и животных самостоятельны.
Дополнениями к клеточной теории являются следующие открытия:
1827г. открытие К. Бэром яйцеклетки млекопитающих и того факта, что все организмы начинают свое развитие с оплодотворенной яйцеклетки;
1858г. Р. Вирхов сформулировал положение «Каждая клетка от клетки»
Это привело к осознанию того факта, что рост и развитие организмов связаны с делением клеток и их дальнейшей дифференцировкой
