
- •Атмосферный воздух. Классификация, история и
- •1.1. Атмосферный воздух и его компоненты
- •1.2. Стандарты основных продуктов разделения воздуха
- •1.3. Области применения продуктов разделения воздуха
- •1.4. Классификация воздухоразделительных установок (вру)
- •1.5. Основные элементы и блоки вру
- •1.6. Краткая история развития воздухоразделительных установок
- •1.7. Особенности современных воздухоразделительных установок (вру)
- •2.2. Потери холода в криогенных циклах
- •2.3. Криогенные циклы
- •2.3.1. Криогенный дроссельный цикл
- •Криогенный дроссельный цикл с предварительным внешним охлаждением
- •2.3.3. Детандерный криогенный цикл высокого давления Гейляндта
- •2.3.4. Детандерный криогенный цикл среднего давления Клода
- •2.6. Детандерный криогенный цикл низкого давления Капицы
- •2.7. Детандерный криогенный цикл двух давлений
- •2.8. Детандерный криогенный цикл низкого давления с совмещенным циркуляционным контуром
- •2.9. Примеры расчета эффективности работы различных криогенных циклов
- •2.10. Анализ результатов расчета различных криогенных циклов
- •3.2. Физические основы разделения воздуха.
- •3.2.1. Упругость насыщенных паров кислорода и азота
- •3.2.2. Экспериментальные кривые равновесия
- •3.2.3. Диаграмма равновесных кривых х-у смеси кислород – азот при различных давлениях
- •3.2.4. Номограмма т-p-I-х-у Герша-Цеханского для системы кислород – азот
- •3.2.5. Диаграмма I - X для системы кислород-азот
- •3.3. Ректификация воздуха, принцип ректификации
- •3.4. Колонны для разделения воздуха
- •Колонна однократной ректификации
- •Колонна двукратной ректификации
- •3.5. Расчет числа теоретических тарелок в ректификационных колоннах
- •Методом Мак-Кэба и Тиле
- •3.6. Графические расчеты процессов ректификации и определение числа теоретических тарелок при помощи I -х диаграммы (метод Пуаншона)
- •В колонне в I-х диаграмме
- •Пример расчета числа теоретических тарелок в колонне двукратной ректификации с помощью у-х и I-х диаграмм
- •4. Принципиальные технологические схемы современных вру
- •4.1. Особенности разработки технологических схем современных вру
- •4.2. Вру большой производительности низкого давления нового поколения
- •4.3. Вру среднего давления
- •4.4. Вру двух давлений
- •4.5. Вру высокого давления
- •4.6. Вру низкого давления малой и средней производительности с совмещенным циркуляционном контуром для выдачи жидких продуктов или газообразных под высоким давлением
- •4.7. Технологическая схема аргонного блока вру с получением чистого аргона методом низкотемпературной ректификации
- •4.8. Получение чистых криптона и ксенона в вру
- •5. Основные блоки и аппараты вру
- •5.1. Блок очистки и осушки воздуха
- •5.1.1. Методы очистки и осушки воздуха
- •5.1.2. Очистка воздуха от двуокиси углерода с помощью сорбентов
- •5.1.3. Очистка воздуха от примесей ацетилена
- •5.1.4. Комплексная очистка воздуха от примесей , и
- •5.1.5. Схема и устройство блока комплексной осушки и очистки воздуха (бкоо)
- •5.1.6. Методика расчета адсорбционного блока осушки и очистки воздуха от примесей паров влаги, углекислоты и ацетилена
- •Расчет процесса десорбции
- •5.2. Определение основных конструктивных размеров ректификационных колонн вру
- •Бинарной смеси
- •Тарелки; 3 – наружная обечайка; 4 - люк
- •Устройствами различных типов:
- •5.3. Определение основных конструктивных размеров конденсаторов-испарителей
- •С внутритрубным кипением
- •Р ис. 5.9. Зависимость кратности циркуляции от различных факторов:
3.6. Графические расчеты процессов ректификации и определение числа теоретических тарелок при помощи I -х диаграммы (метод Пуаншона)
Графический метод расчета разделительных колонн в диаграмме х-у, несмотря на его наглядность и простоту, не учитывает изменения многих весьма важных факторов в процессе ректификации. Он лишь дает возможность фиксировать изменение концентрации нижекипящего компонента (азота) в жидкости и паре при условии постоянства количества пара и флегмы по высоте колонны.
Расчет ректификационных колонн при помощи i-х диаграммы, помимо наглядного изображения термодинамического процесса, позволяет проследить влияние отдельных факторов на процесс ректификации, в частности изменение отношений количество флегмы и пара, количество передаваемого тепла при испарении вышекипящего компонента (кислорода) и конденсации нижекипящего компонента (азота) и изменение их концентрации.
Изображение основных процессов в i-х диаграмме
Смешение.
Пусть
![]() ,
кг смеси
с концентрацией
и энтальпией
,
кг смеси
с концентрацией
и энтальпией
![]() смешивается
с
смешивается
с
![]() кг
смеси с
концентрацией
и энтальпией
кг
смеси с
концентрацией
и энтальпией
![]() ,
тогда
состояние после смешения определяется
следующим образом.
,
тогда
состояние после смешения определяется
следующим образом.
На
рис. 3.14 состояние первой смеси изображается
точкой 1,
второй смеси
– точкой 2. Соединив точки 1 и 2, приняв
отрезок 1-2 за единицу и разделив его в
отношении
![]() ,
найдем точку М, которая представляет
собой состояние смеси после смешения.
,
найдем точку М, которая представляет
собой состояние смеси после смешения.
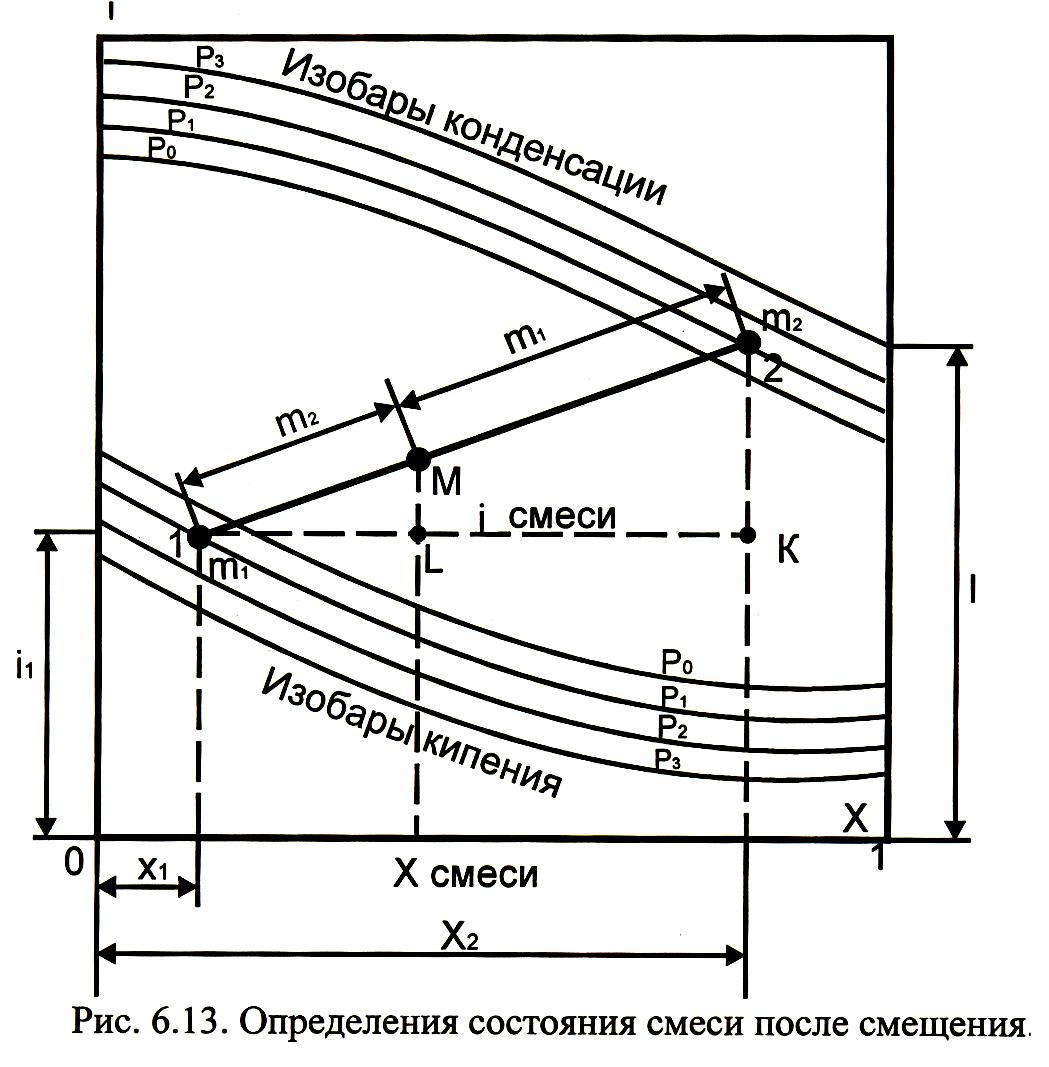
Рис. 3.14. Определения состояния смеси после смещения
Учитывая, что
|
(3.33) |
запишем
|
(3.34) |
|
(3.35) |
Из последних уравнений найдем
|
(3.36) |
|
(3.37) |
Откуда получим
|
(3.38) |
Из уравнений (3.35-3.37) найдем
|
(3.39) |
Из подобия треугольников l-M-L и 1-2-К можно легко доказать, что точка М действительно представляет собой состояние смеси после смешения.
Кипение. Процесс кипения в i-х диаграмме изображен на рис. 3. 15.
Точки
А и В характеризуют процесс кипения
при давлении
![]() в замкнутом объеме. При кипении суммарная
концентрация жидкой и паровой фаз
остается постоянной. Так как х = const, то
процесс кипения изобразится вертикальной
линией АВ.
в замкнутом объеме. При кипении суммарная
концентрация жидкой и паровой фаз
остается постоянной. Так как х = const, то
процесс кипения изобразится вертикальной
линией АВ.
В
промежуточном состоянии, точка М - смесь
состоит из двух фаз: жидкость К с
концентрацией
![]() и
пар N с концентрацией
и
пар N с концентрацией
![]() .
.
Количество
жидкости
![]() равно BМ, а количество пара
равно BМ, а количество пара
![]() - отрезку МA. Если считать, что общее
количество смеси равно отрезку АВ = l,
то
- отрезку МA. Если считать, что общее
количество смеси равно отрезку АВ = l,
то
|
(3.40) |
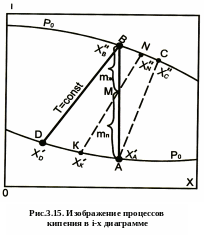
При кипении непрерывно уменьшается концентрация нижекипящего компонента в жидкости и одновременно понижается концентрация равновесного пара.
В
точке В жидкость полностью превращается
в пар с первоначальной концентрацией
жидкости,
![]() .
.
Последняя
капля кипящей жидкости имеет концентрацию
,
а первые
испарившиеся пузырьки пара - концентрацию
![]() .
.
Конденсация. При охлаждении насыщенного пара происходит его конденсация. Процесс конденсации в замкнутом пространстве при давлении на диаграмме i-х, как и процесс кипения, изображается вертикальной линией ВА, с той лишь разницей, что все промежуточные состояния будут происходить в обратном порядке: от точки В до точки А.
При
конденсации концентрация нижекипящего
компонента в паре и равновесной
жидкости увеличивается. В конце процесса,
когда пар полностью конденсируется,
концентрация жидкости будет равна
первоначальной концентрации пара:
![]() .
Первая
сконденсированная капля имеет
концентрацию
,
последняя
сконденсированная порция пара -
концентрацию
.
Первая
сконденсированная капля имеет
концентрацию
,
последняя
сконденсированная порция пара -
концентрацию
![]() .
.
Процесс ректификации в i-х диаграмме
Процесс ректификации, который протекает в ректификационной колонне, позволяет разделить смесь, например воздух, на отдельные технически чистые компоненты, например азот и кислород. При ректификации жидкость и пар, не находящиеся между собой в равновесии, приходят в соприкосновение и претерпевают изменения до тех пор, пока не будет достигнуто равновесие.
Если при данном составе пара жидкость взята более богатой нижекипящем компонентом, то в результате соприкосновения, когда наступит равновесие между жидкой и газовой фазами, концентрация нижекипящего компонента в парах увеличится, а в жидкости уменьшится. Подобный процесс, повторяемый многократно, и составляет сущность ректификации.
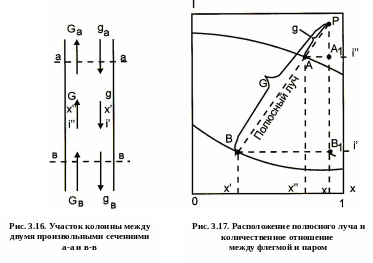
Процесс ректификации в колонне
Выделим произвольный участок в ректификационной колонны между двумя сечениями а-а и в-в (рис. 3. 16).
При установившемся процессе в колонне должны соблюдаться следующие соотношения.
Материальный баланс
|
(3.41) |
или
|
(3.42) |
Откуда можно записать для любого сечения:
|
(3.43) |
Эта постоянная величина равна количеству полученного пара D:
|
(3.44) |
Материальный баланс по нижекипящему компоненту
Для любых двух сечений в колонне можно записать балансовое уравнение и по нижекипящему компоненту:
|
(3.45) |
или |
|
|
(3.46) |
Тогда для любого сечения
|
(3.47) |
Тепловой баланс
Если колонна хорошо изолирована, то для любых сечений можно записать уравнения теплового баланса
|
(3.48) |
|
(3.49) |
Или для любого сечения:
|
(3.50) |
Приведенные концентрация и энтальпия
Если разделить уравнение (3.47) на (3.49), то получим
|
(3.51) |
Также разделив (3.50) на (3.43), найдем
|
(3.52) |
Полученные значения х и i соответственно называют “приведенная концентрация” и “приведенная энтальпия”.
Уравнения (3.51) и (3.52) показывают, что приведенная концентрация х и приведенная энтальпия i остаются величинами постоянными для всех сечений колонны.
Точка с координатами приведенных концентрации х и энтальпией i называется полюсом.
Полюс колонны обладает рядом свойств:
- если через две точки, характеризующие состояние пара и жидкости в любом сечении колонны, провести прямую линию, то она пройдет через полюс (рис.3.17).
Это видно из следующих соотношений:
Из (3.51) имеем
|
(3.53) |
или
|
(3.54) |
Откуда
|
(3.55) |
Точно таким же образом из (3.52) получим
|
(3.56) |
Из
подобия треугольников
![]() следует:
следует:
|
(3.57) |
Учитывая, что
|
|
получим
|
(3.58) |
То есть точки А и В представляют собой состояние пара и жидкости в сечении колонны.
Линия,
проведенная через полюс
![]() (линия
РАВ),
называется
полюсным лучом.
(линия
РАВ),
называется
полюсным лучом.
Из уравнений (3.55), (3.56) и (3.57) следует
|
(3.59) |
То есть отношение отрезков РА и РВ представляют собой отношение количества флегмы и пара, выходящих с тарелки колонны.
Определение изменения концентраций пара и жидкости на тарелках ректификационной колонны с помощью i-х диаграммы
Если известна концентрация жидкости или пара на какой-либо тарелке, то, зная положение полюса, можно определить изменение концентраций пара и жидкости, как выше, так и нижерасположенных тарелках.
Н а
рис. (3.18) и (3.19) показаны часть колонны и
графическое построение для определения
концентраций жидкости и пара на
нижележащих тарелках
1, 2 и 3.
а
рис. (3.18) и (3.19) показаны часть колонны и
графическое построение для определения
концентраций жидкости и пара на
нижележащих тарелках
1, 2 и 3.
Пусть
известны положение полюса Р
и концентрация
пара
![]() на верхней тарелке 1. Для определения
концентрации жидкости
на верхней тарелке 1. Для определения
концентрации жидкости
![]() на первой тарелке 1 проведем полюсной
луч через точку 1 (Р-1-1'). Точка
на первой тарелке 1 проведем полюсной
луч через точку 1 (Р-1-1'). Точка
![]() на изобаре кипения покажет состояние
жидкости
,
стекающей с первой тарелки. Ниже
расположена тарелка 2, жидкость на
которой находится в равновесии с паром,
наступающим на тарелку 1. То есть,
концентрация жидкости на тарелке 2-
на изобаре кипения покажет состояние
жидкости
,
стекающей с первой тарелки. Ниже
расположена тарелка 2, жидкость на
которой находится в равновесии с паром,
наступающим на тарелку 1. То есть,
концентрация жидкости на тарелке 2-![]() лежит на изотерме 1-2', проведенной из
точки 1. Полюсной луч Р-2-2' определяет в
точке 2 концентрацию пара на тарелке
2-
лежит на изотерме 1-2', проведенной из
точки 1. Полюсной луч Р-2-2' определяет в
точке 2 концентрацию пара на тарелке
2-![]() .
Проведя изотерму 2-3', найдем состояние
жидкости на тарелке 3-
.
Проведя изотерму 2-3', найдем состояние
жидкости на тарелке 3-
![]() .
А концентрация пара, поступающего
на тарелку 3, определяется точкой
пересечения полюсного луча Р-3-3' с
изобарой конденсации.
.
А концентрация пара, поступающего
на тарелку 3, определяется точкой
пересечения полюсного луча Р-3-3' с
изобарой конденсации.
Отношение
отрезков
![]() ,
представляет собой отношения количеств
флегмы и пара на соответствующей тарелке.
,
представляет собой отношения количеств
флегмы и пара на соответствующей тарелке.
Процесс ректификации будет продолжаться до тех пор, пока полюсной луч, проведенный через полюс Р, не совпадает с изотермой. Для процесса ректификации необходимо, чтобы полюсной луч пересекал изотерму. Положение полюса определяет минимальную концентрацию нижекипящего компонента в остатке.
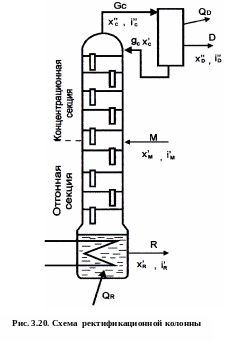
Определение полюсов в ректификационной колонне,
состоящей из концентрационной и отгонной секций
На рис. 3.20 показана схема колонны, состоящей из концентрационной и отгонной секций (верхняя колонна).
Смесь
М
поступает
в среднюю часть колонны с концентрацией
![]() и энтальпией
и энтальпией
![]() .
Пары G
из отгонной
секции поступают в концентрационную.
Флегма
.
Пары G
из отгонной
секции поступают в концентрационную.
Флегма
![]() из
концентрационной секции присоединяется
к смеси М
и стекает в
отгонную секцию. В результате флегмы
в отгонной секции больше, чем
концентрационной. Из куба отгонной
секции выходит остаток R
с концентрацией
из
концентрационной секции присоединяется
к смеси М
и стекает в
отгонную секцию. В результате флегмы
в отгонной секции больше, чем
концентрационной. Из куба отгонной
секции выходит остаток R
с концентрацией
![]() и энтальпией
и энтальпией
![]() .
В кубе колонны
подводится количество тепла
.
В кубе колонны
подводится количество тепла![]() .
В результате
ректификации из колонны отводятся пары
D с
концентрацией
.
В результате
ректификации из колонны отводятся пары
D с
концентрацией
![]() и энтальпией
и энтальпией
![]() .
.
Для
образования флегмы в концентрационной
секции в дефлегматоре отводится тепло
![]() .
.
Из баланса всей колонны можно записать уравнения:
|
(3.60) |
|
(3.61) |
Откуда можно записать
|
(3.62) |
Или
|
(3.63) |
Тепловой баланс колонны.
Обозначим:
![]() .
.
Тогда уравнение (3.63) можно представить как
|
(3.64) |
Или
|
(3.65) |
Подставляя
в последнее уравнение значения
![]() из (3.62) и (3.63), получим уравнение
из (3.62) и (3.63), получим уравнение
|
(3.66) |
Это
уравнение прямой, переходящей через
три точки М,
![]() и
и
![]() (рис. 3.21).
(рис. 3.21).
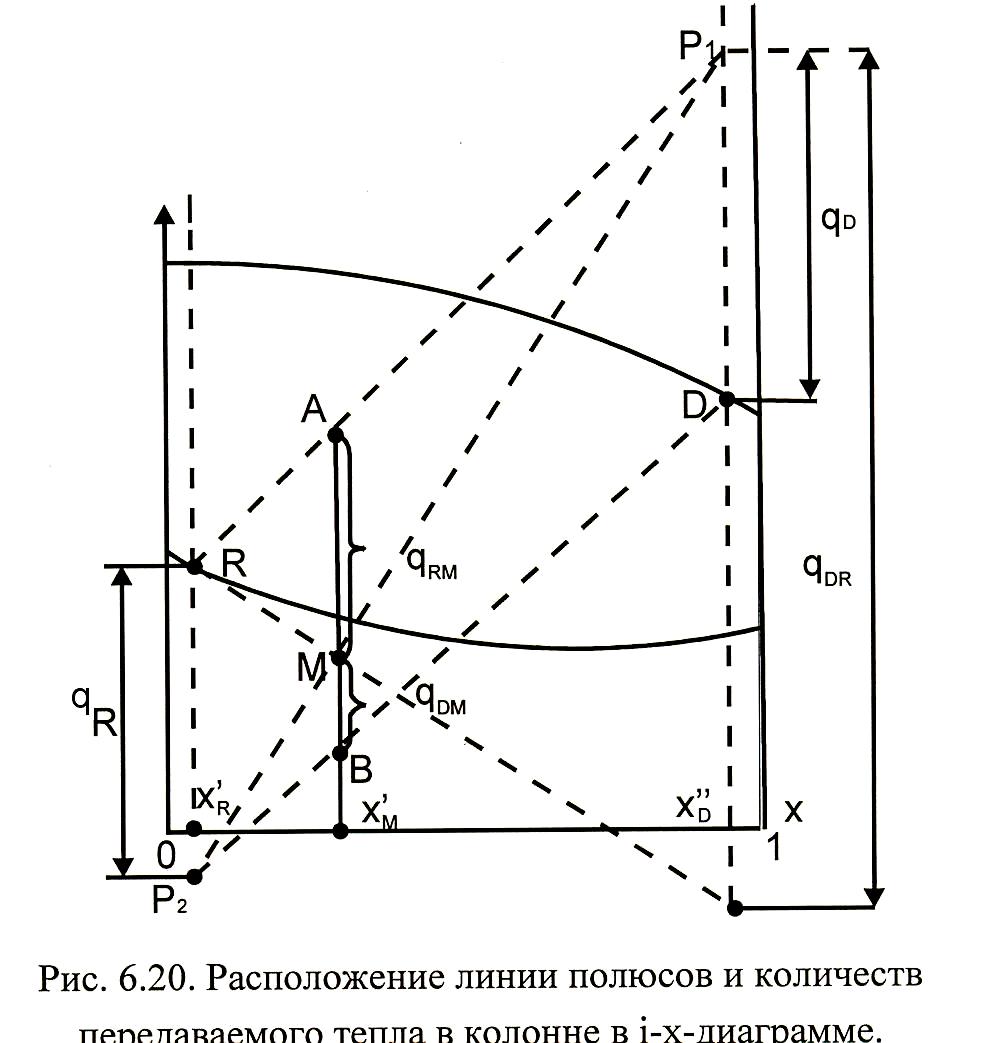
Рис. 3.21. Расположение линии полюсов и количеств передаваемого тепла

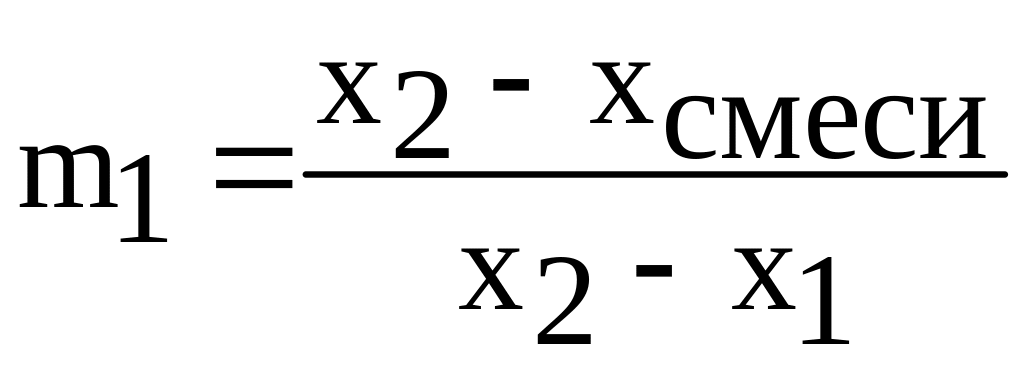 ,
, .
. ,
,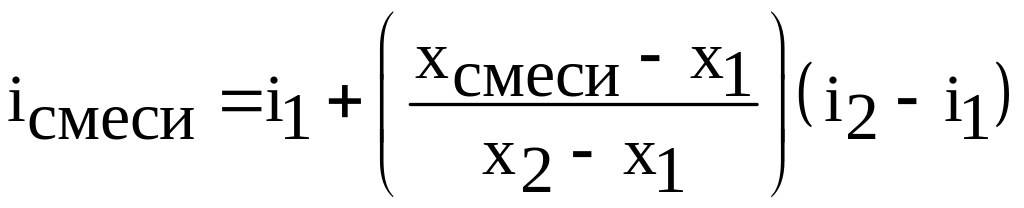 ,
,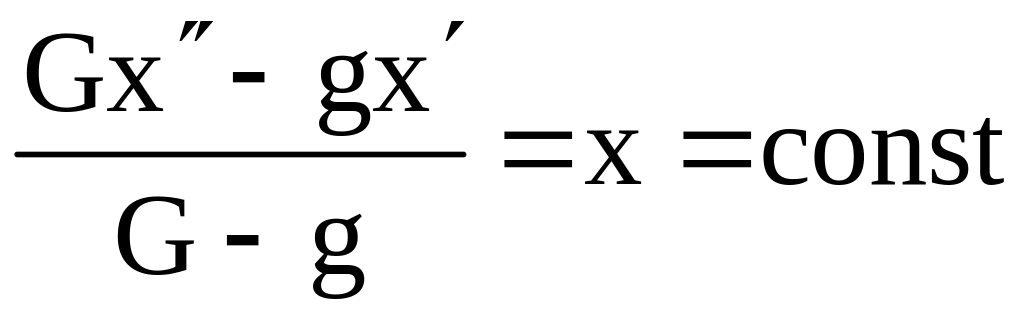 .
.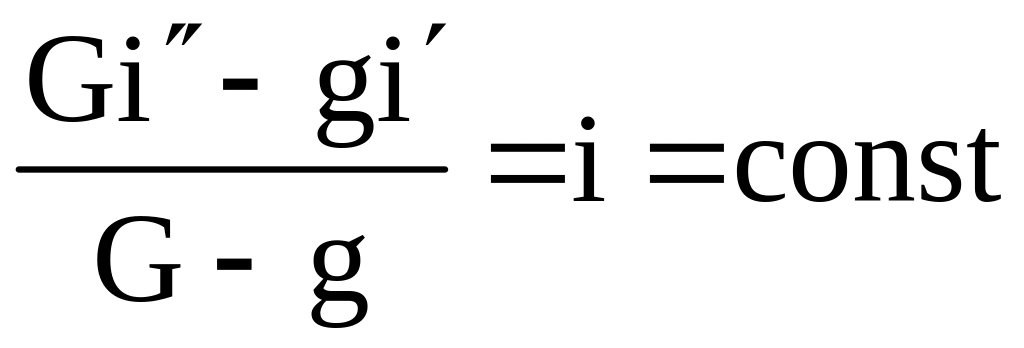 .
.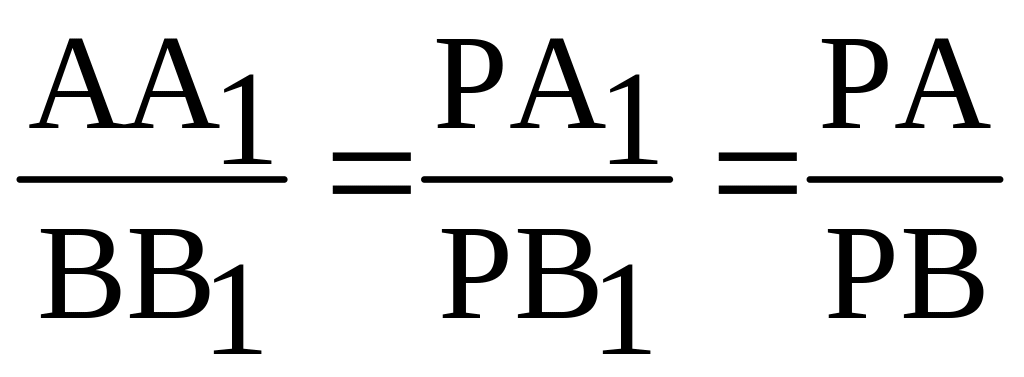 .
.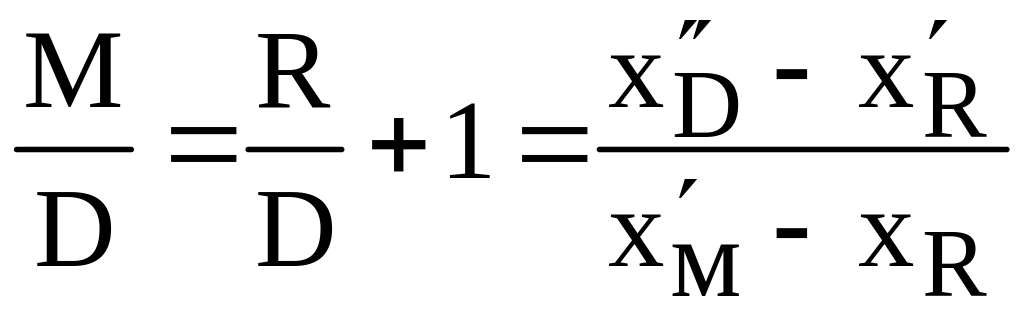 .
.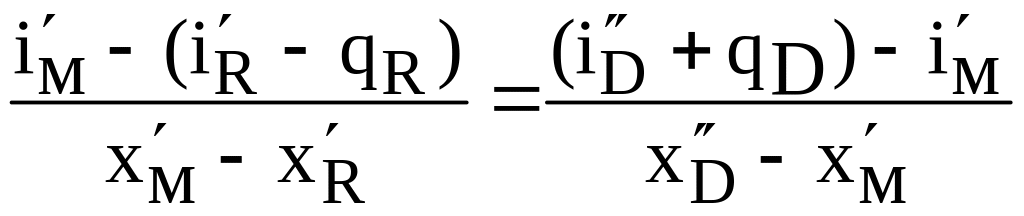 .
.