- •Атмосферный воздух. Классификация, история и
- •1.1. Атмосферный воздух и его компоненты
- •1.2. Стандарты основных продуктов разделения воздуха
- •1.3. Области применения продуктов разделения воздуха
- •1.4. Классификация воздухоразделительных установок (вру)
- •1.5. Основные элементы и блоки вру
- •1.6. Краткая история развития воздухоразделительных установок
- •1.7. Особенности современных воздухоразделительных установок (вру)
- •2.2. Потери холода в криогенных циклах
- •2.3. Криогенные циклы
- •2.3.1. Криогенный дроссельный цикл
- •Криогенный дроссельный цикл с предварительным внешним охлаждением
- •2.3.3. Детандерный криогенный цикл высокого давления Гейляндта
- •2.3.4. Детандерный криогенный цикл среднего давления Клода
- •2.6. Детандерный криогенный цикл низкого давления Капицы
- •2.7. Детандерный криогенный цикл двух давлений
- •2.8. Детандерный криогенный цикл низкого давления с совмещенным циркуляционным контуром
- •2.9. Примеры расчета эффективности работы различных криогенных циклов
- •2.10. Анализ результатов расчета различных криогенных циклов
- •3.2. Физические основы разделения воздуха.
- •3.2.1. Упругость насыщенных паров кислорода и азота
- •3.2.2. Экспериментальные кривые равновесия
- •3.2.3. Диаграмма равновесных кривых х-у смеси кислород – азот при различных давлениях
- •3.2.4. Номограмма т-p-I-х-у Герша-Цеханского для системы кислород – азот
- •3.2.5. Диаграмма I - X для системы кислород-азот
- •3.3. Ректификация воздуха, принцип ректификации
- •3.4. Колонны для разделения воздуха
- •Колонна однократной ректификации
- •Колонна двукратной ректификации
- •3.5. Расчет числа теоретических тарелок в ректификационных колоннах
- •Методом Мак-Кэба и Тиле
- •3.6. Графические расчеты процессов ректификации и определение числа теоретических тарелок при помощи I -х диаграммы (метод Пуаншона)
- •В колонне в I-х диаграмме
- •Пример расчета числа теоретических тарелок в колонне двукратной ректификации с помощью у-х и I-х диаграмм
- •4. Принципиальные технологические схемы современных вру
- •4.1. Особенности разработки технологических схем современных вру
- •4.2. Вру большой производительности низкого давления нового поколения
- •4.3. Вру среднего давления
- •4.4. Вру двух давлений
- •4.5. Вру высокого давления
- •4.6. Вру низкого давления малой и средней производительности с совмещенным циркуляционном контуром для выдачи жидких продуктов или газообразных под высоким давлением
- •4.7. Технологическая схема аргонного блока вру с получением чистого аргона методом низкотемпературной ректификации
- •4.8. Получение чистых криптона и ксенона в вру
- •5. Основные блоки и аппараты вру
- •5.1. Блок очистки и осушки воздуха
- •5.1.1. Методы очистки и осушки воздуха
- •5.1.2. Очистка воздуха от двуокиси углерода с помощью сорбентов
- •5.1.3. Очистка воздуха от примесей ацетилена
- •5.1.4. Комплексная очистка воздуха от примесей , и
- •5.1.5. Схема и устройство блока комплексной осушки и очистки воздуха (бкоо)
- •5.1.6. Методика расчета адсорбционного блока осушки и очистки воздуха от примесей паров влаги, углекислоты и ацетилена
- •Расчет процесса десорбции
- •5.2. Определение основных конструктивных размеров ректификационных колонн вру
- •Бинарной смеси
- •Тарелки; 3 – наружная обечайка; 4 - люк
- •Устройствами различных типов:
- •5.3. Определение основных конструктивных размеров конденсаторов-испарителей
- •С внутритрубным кипением
- •Р ис. 5.9. Зависимость кратности циркуляции от различных факторов:
3.2.3. Диаграмма равновесных кривых х-у смеси кислород – азот при различных давлениях
При расчете необходимого числа теоретических тарелок в ректификационной колонне широко применяется диаграмма равновесных кривых х-у при различных давлениях (рис. 3.3). На оси абсцисс откладываются мольные концентрации х низкокипящего компонента – азота в жидкости, а по оси ординат мольные концентрации у того же азота, но в паре. Кривые на диаграмме являются изобарами, показывающие зависимости мольной концентрации равновесного состояния азота в паре у от мольной концентрации равновесного состояния азота в жидкости х при данном давлении.
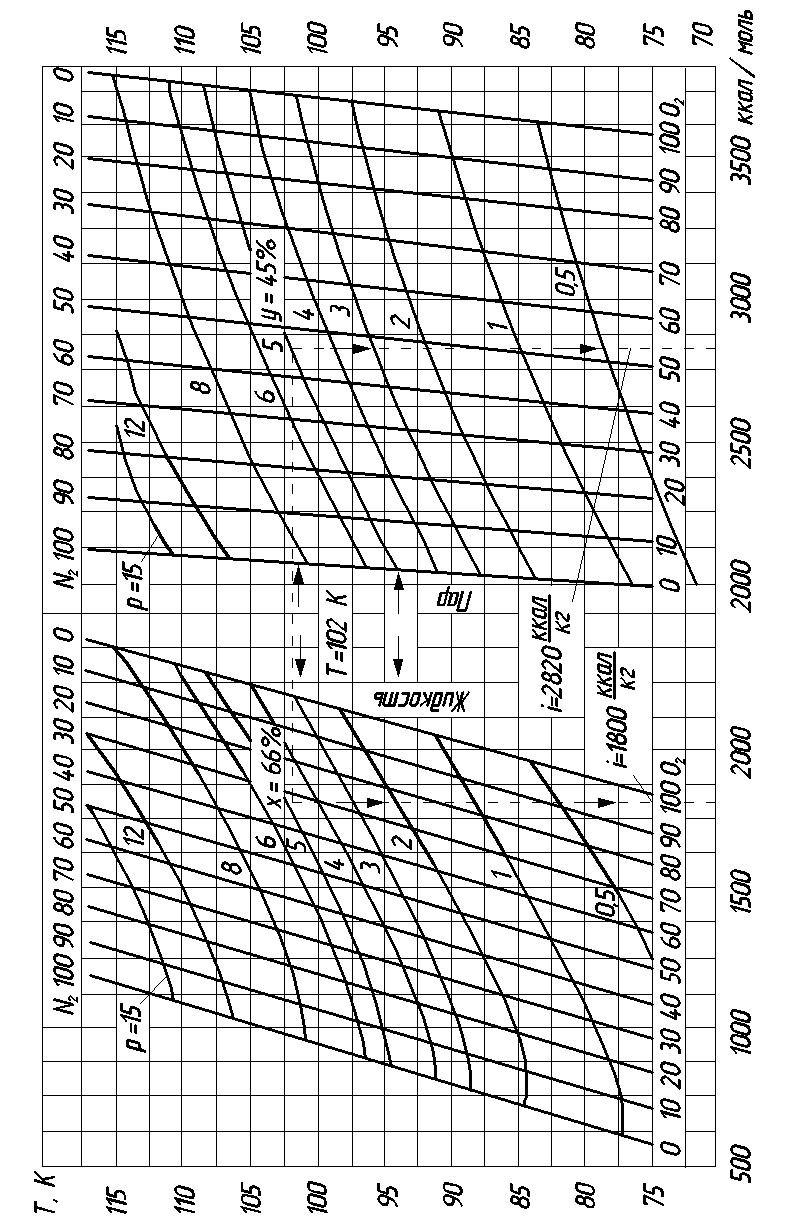
3.2.4. Номограмма т-p-I-х-у Герша-Цеханского для системы кислород – азот
При расчете процессов разделения воздуха широко применяется также номограмма Т-p-i х-у системы кислород – азот (рис. 3.4). Номограмма позволяет определить сразу пять параметров равновесных состояний пара и жидкости системы
|
Рис. 3.4. Номограмма Т-p-i-х-у Герша-Цеханского для системы кислород – азот |
кислород-азот: температуру, давление, энтальпию и концентрацию равновесных состояний кислорода и азота и в паре, и в жидкости.
Номограмма разделяется на две части: область равновесных состояний жидкости – слева и область равновесных состояний пара – справа. На номограмме нанесены изобары и сетка концентрации кислорода , % и азота , %.
На номограмме показано определение отдельных параметров смеси - (пунктирные линии) для заданных давлений и температуры.
3.2.5. Диаграмма I - X для системы кислород-азот
Диаграмма
![]() для системы кислород
и азот
,
введенная
в технику Пуаншоном, имеет большое
значение при расчете процессов
ректификации (кипения и конденсации) и
числа теоретических тарелок в
разделительных колоннах (рис. 3.5).
для системы кислород
и азот
,
введенная
в технику Пуаншоном, имеет большое
значение при расчете процессов
ректификации (кипения и конденсации) и
числа теоретических тарелок в
разделительных колоннах (рис. 3.5).
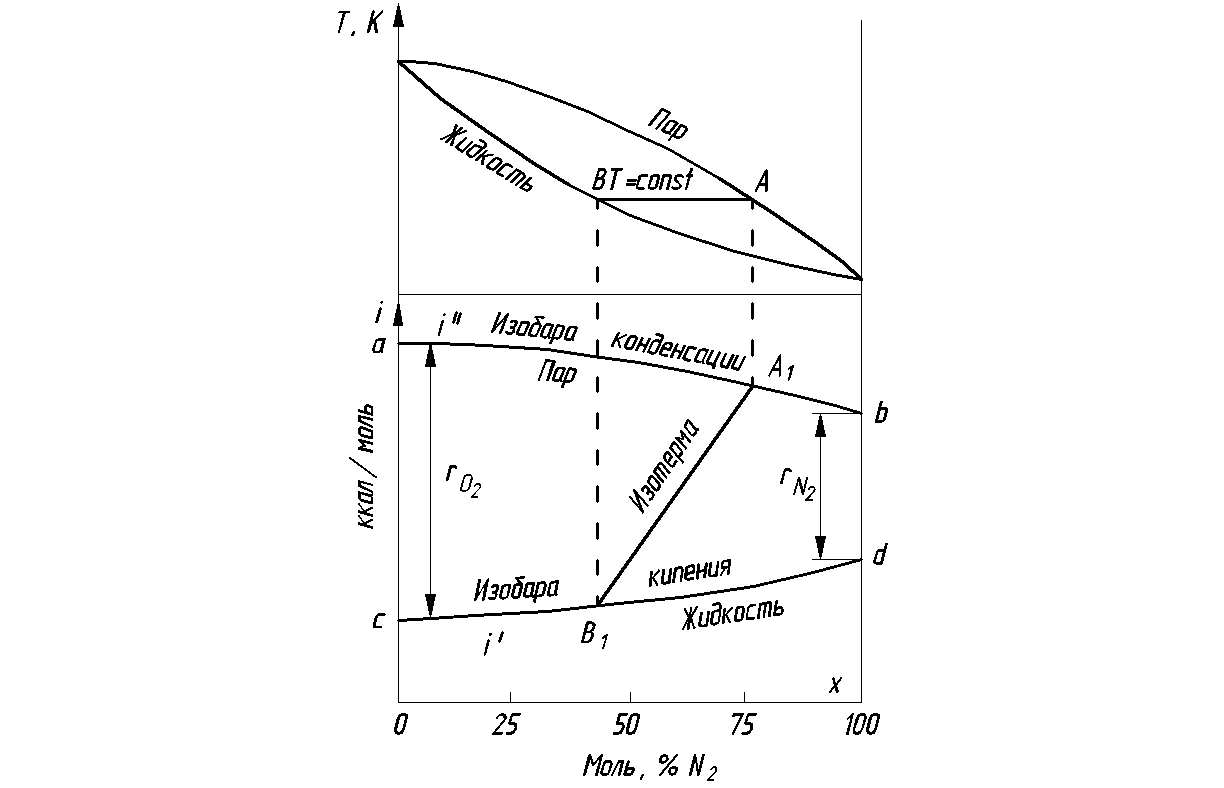
Рис. 3.5. i
- х диаграмма для воздуха
В
диаграмме
по оси ординат откладывается энтальпия
![]() ,
а по оси абсцисс – концентрация
нижекипящего компонента х (для
воздуха-азот) в жидкости и паре. На
диаграмме нанесены две кривые линии:
верхняя
а-b
- изобара конденсации, нижняя с-d
– изобара кипения. Изобара конденсации
представляет собой кривую состояния
пара, соответствующего началу конденсации.
Кривая с-d
представляет собой состояние жидкости
в начале кипения. Эти две кривые не
сходятся в одной точке при концентрации
азота от 0 до 100 % , как это имеет место
для равновесных кривых в Т-х-у диаграмме.
Разность ординат соответствует разности
энтальпий пара и жидкости: для х = 0 %
она равна скрытой теплоте испарения
кислорода -
,
а по оси абсцисс – концентрация
нижекипящего компонента х (для
воздуха-азот) в жидкости и паре. На
диаграмме нанесены две кривые линии:
верхняя
а-b
- изобара конденсации, нижняя с-d
– изобара кипения. Изобара конденсации
представляет собой кривую состояния
пара, соответствующего началу конденсации.
Кривая с-d
представляет собой состояние жидкости
в начале кипения. Эти две кривые не
сходятся в одной точке при концентрации
азота от 0 до 100 % , как это имеет место
для равновесных кривых в Т-х-у диаграмме.
Разность ординат соответствует разности
энтальпий пара и жидкости: для х = 0 %
она равна скрытой теплоте испарения
кислорода -
![]() ;
для х = 100 %
- скрытой теплоте испарения азота -
;
для х = 100 %
- скрытой теплоте испарения азота -
![]() .
Между пограничными кривыми диаграммы
находится двухфазная область: жидкость-пар.
Выше кривой конденсации находится
область перегретого пара, ниже кривой
кипения – область жидкости. В верхней
части диаграммы
(рис. 3.5) приведены изобары в координатах
Т-х-у и показан способ построения изотерм
в i
-
x
диаграмме. Изотерма
А-В в Т-х-у диаграмме легко переносится
на диаграмму i
-
x.
Точка А на диаграмме Т-х-у соответствует
точке
.
Между пограничными кривыми диаграммы
находится двухфазная область: жидкость-пар.
Выше кривой конденсации находится
область перегретого пара, ниже кривой
кипения – область жидкости. В верхней
части диаграммы
(рис. 3.5) приведены изобары в координатах
Т-х-у и показан способ построения изотерм
в i
-
x
диаграмме. Изотерма
А-В в Т-х-у диаграмме легко переносится
на диаграмму i
-
x.
Точка А на диаграмме Т-х-у соответствует
точке
![]() на диаграмме i
-
x,
а точка В соответствует точке
на диаграмме i
-
x,
а точка В соответствует точке
![]() .
Линия
-
представляет собой изотерму на диаграмме
i
-x.
В
диаграмме i
-x
х является концентрация нижекипящего
компонента, т.е. азота. Концентрация
жидкости обозначается через
.
Линия
-
представляет собой изотерму на диаграмме
i
-x.
В
диаграмме i
-x
х является концентрация нижекипящего
компонента, т.е. азота. Концентрация
жидкости обозначается через
![]() ,
а пара – через
,
а пара – через
![]() .
Энтальпия жидкости обозначается
соответственно через
.
Энтальпия жидкости обозначается
соответственно через
![]() ,
а пара – через
,
а пара – через
![]() .
.