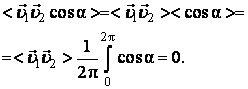- •2) Основное уравнение молекулярно-кинетической теории идеального газа.
- •3) Уравнение состояния идеального газа
- •4) Закон распространения молекул по скоростям
- •6) Явление переноса в газах. Средняя длина свободного пробега.
- •7)Внутреннее трение газов. Крэффициент внутреннего трения.
- •8) Теплопроводность газов. Распределение энергии по степеням свободы.
- •9) Коэффициент теплопроводности газов
- •10) Стационарная диффузия
- •11) Нестационарное диффузия. Термодинамический метод описания явлений.
- •12) Термодинамические параметры
- •13) Внутренняя энергия и температура термодинамической системы
- •14) Внутренняя энергия. Работа. Теплота
- •15) Первый закон термодинамики
6) Явление переноса в газах. Средняя длина свободного пробега.
Явления переноса в газах |
|
||||||||||||||
В состоянии равновесия температура Т и концентрация n во всех точках системы одинакова. При отклонении плотности от равновесного значения в некоторой части системы возникает движение компонент вещества в направлениях, приводящих к выравниванию концентрации по всему объему системы. Связанный с этим движением перенос вещества обусловлен диффузией. Диффузионный поток будет пропорционален градиенту концентрации:
В процессе диффузии при теплопроводности и электропроводности происходит перенос вещества, а при внутреннем трении – перенос энергии. В основе этих явлений лежит один и тот же механизм – хаотическое движение молекул. Общность механизма, обуславливающего все эти явления переноса, приводит к тому, что их закономерности должны быть похожи друг на друга. |
|||||||||||||||
Средняя длина свободного пробега молекул
Под средней длиной свободного пробега понимают среднее расстояние, которое проходит молекула между двумя последовательными соударениями. За секунду
молекула в среднем проходит расстояние,
численно равное ее средней скорости
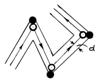
Предположим, что все молекулы, кроме рассматриваемой, неподвижны. Молекулы будем считать шарами с диаметром d. Столкновения будут происходить всякий раз, когда центр неподвижной молекулы окажется на расстоянии меньшем или равном d от прямой, вдоль которой двигается центр рассматриваемой молекулы. При столкновениях молекула изменяет направление своего движения и затем движется прямолинейно до следующего столкновения. Поэтому центр движущейся молекулы ввиду столкновений движется по ломаной линии (рис. 1).
Молекула
столкнется со всеми неподвижными
молекулами, центры которых находятся
в пределах ломаного цилиндра диаметром
2d. За секунду молекула проходит путь,
равный
.
Поэтому число происходящих за это
время столкновений равно числу молекул,
центры которых попадают внутрь ломаного
цилиндра, имеющего суммарную длину
и
радиус d. Его объем примем равным объему
соответствующего спрямленного
цилиндра, т. е. равным
В действительности движутся все молекулы. Поэтому число столкновений за одну секунду будет несколько большим полученной величины, так как вследствие движения окружающих молекул рассматриваемая молекула испытала бы некоторое число соударений даже в том случае, если бы она сама оставалась неподвижной. Предположение
о неподвижности всех молекул, с которыми
сталкивается рассматриваемая молекула,
будет снято, если в формулу (3.1.2) вместо
средней скорости
представить
среднюю скорость относительного
движения
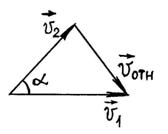
Предположим,
что скорости молекул до столкновения
были
Так
как углы
от произведения этих величин равно произведению их средних. Поэтому
С учетом последнего равенства формулу (3.1.4) можно переписать в виде:
так
как
т.
е. Поэтому соотношение (3.1.6) можно представить так:
С учетом последнего выражения формула для средней длины свободного пробега приобретает вид:
Для
идеального газа
Отсюда видно, что при изотермическом расширении (сжатии) средняя длина свободного пробега растет (убывает). Как было отмечено во введении, эффективный диаметр молекул убывает с ростом температуры. Поэтому при заданной концентрации молекул средняя длина свободного пробега увеличивается с ростом температуры. Вычисление
средней длины свободного пробега для
азота (d = 3•10-10 м),
находящегося при нормальных условиях
(р = 1,01•105 Па,
Т = 273,15 К) дает: |