
- •1.Понятие об идеальном газе, Законы и уравнения состояния идеального газа
- •2.Внутренняя энергия, работа и теплота в термодинамике. Теплоёмкость вещ-ва. Работа расширения газа
- •3. Вероятность и флюктуации. Распределение Максвелла и его Зависимость от температуры. Среднее значение скоростей и наиболее вероятная скорость
- •4.Распределение числа частиц по высоте.Распределение Больцмана.Распределение Максвелл-Больцмана
- •5. Реальные газы. Уравнение Ван-дер-Вальса. Критическое состояние. Эффект Джоуля-Томсона
- •6.Изотермы Эндрюса и Ван-Дер-Ваальса. Метастабильные сотояния. Физический смысл критического сотояния
- •7.Фазы и компоненты. Условие равновесия фаз. Фазовые переходы первого и второго уровня
- •8.Уравнение Клапейрона-Клаузиуса. Фазовые диаграммы. Тройная точка
- •9. Понятие о физической кинетике. Время релаксации. Эффективное сечение рассеяния. Средняя длина свободного пробега
- •10. Строение кристаллов. Точечные дефекты в кристаллах:вакансии.Примеси внедрения,замещения
- •11. Элементы зонной теории кристаллов.Заполнение зон:металлы,диэлектрики,полупроводники
- •12.Полупроводники.Понятие дырочной проводимости.Собственные и примесные полупроводники
- •13. Электрический ток в вакууме.Термоэлектронная эмиссия
8.Уравнение Клапейрона-Клаузиуса. Фазовые диаграммы. Тройная точка
Клапейрона-Клаузиуса
термодинамическое уравнение относится
к процессам перехода вещества из одной
фазы в другую (испарение, плавление,
сублимация, полиморфное превращение и
др.). Согласно К.-К. у., теплота фазового
перехода (например, теплота испарения,
теплота плавления) при равновесно
протекающем процессе определяется
выражением
![]() ,
(1) где Т-темп-ра перехода (процесс
изотермический), dp/dT-значение производной
от давления по температуре при данной
температуре перехода, (V2-V1)-измен-е объёма
вещества при переходе его из первой
фазы во вторую. Первоначально уравнение
было получено из анализа Карно цикла
для конденсирующегося пара, находящегося
в тепловом равновесии с жидкостью.
Клаузиус усовершенствовал уравнение
и распространил его на др. фазовые
переходы. К.- К. у. применимо к любым
фазовым переходам, сопровождающимся
поглощением или выделением теплоты (т.
н. фазовым переходом 1 рода), и является
прямым следствием условий фазового
равновесия.В частности, с его помощью
рассчитывают теплоты испарения,
экспериментальное опред-е которых
сопряжено со значительными трудностями.К.-К.
у. является дифференциальным уравнением
кривой фазового равновесия в переменных
р,Т.Фазовая
диаграмма,
графическое изображение соотношений
между параметрами состояния
темп-ры(давлением и др.) и её составом.
В простейшем случае, когда сис-ма состоит
только из одного компонента, ф. д.
представляет собой трёхмерную
пространственную фигуру, построенную
в трёх прямоугольных координатных осях,
по которым откладывают температуру
(Т), давление (p) и мольный объём (v).
Пользование объёмной ф.д. неудобно
вследствие её громоздкости; поэтому на
практике применяют проекцию ф.д. на одну
из координатных плоскостей, обычно на
плоскость p-Т. Тройная
точка в термодинамике,
точка на диаграмме состояния,
соответствующая равновесному
сосуществованию трёх фаз вещества.
,
(1) где Т-темп-ра перехода (процесс
изотермический), dp/dT-значение производной
от давления по температуре при данной
температуре перехода, (V2-V1)-измен-е объёма
вещества при переходе его из первой
фазы во вторую. Первоначально уравнение
было получено из анализа Карно цикла
для конденсирующегося пара, находящегося
в тепловом равновесии с жидкостью.
Клаузиус усовершенствовал уравнение
и распространил его на др. фазовые
переходы. К.- К. у. применимо к любым
фазовым переходам, сопровождающимся
поглощением или выделением теплоты (т.
н. фазовым переходом 1 рода), и является
прямым следствием условий фазового
равновесия.В частности, с его помощью
рассчитывают теплоты испарения,
экспериментальное опред-е которых
сопряжено со значительными трудностями.К.-К.
у. является дифференциальным уравнением
кривой фазового равновесия в переменных
р,Т.Фазовая
диаграмма,
графическое изображение соотношений
между параметрами состояния
темп-ры(давлением и др.) и её составом.
В простейшем случае, когда сис-ма состоит
только из одного компонента, ф. д.
представляет собой трёхмерную
пространственную фигуру, построенную
в трёх прямоугольных координатных осях,
по которым откладывают температуру
(Т), давление (p) и мольный объём (v).
Пользование объёмной ф.д. неудобно
вследствие её громоздкости; поэтому на
практике применяют проекцию ф.д. на одну
из координатных плоскостей, обычно на
плоскость p-Т. Тройная
точка в термодинамике,
точка на диаграмме состояния,
соответствующая равновесному
сосуществованию трёх фаз вещества.
9. Понятие о физической кинетике. Время релаксации. Эффективное сечение рассеяния. Средняя длина свободного пробега
Физическая
кинетика -
микроскопическая теория процессов в
неравновесных средах. В кинетике методами
квантовой или классической статистической
физики изучают процессы переноса
энергии, импульса, заряда и вещества в
разл-х физических сис-мах (газах, плазме,
жидкостях, твёрдых телах) и влияние на
них внешних полей. Процесс самопроизвольного
перехода сис-мы в равновесное состояние
называется релаксацией, а время этого
процесса - временем
релаксации.
До истечения времени релаксации состояние
сис-мы остается неравновесным, а сам
процесс релаксации является неравновесным.
Молекулы газа,
находясь в состоянии хаотического
движ-я, непрерывно сталкиваются друг с
другом. Между двумя последовательными
столкновениями молекулы проходят
некоторый путь l,
который называется длиной
свободного пробега.
В общем случае длина пути между
последовательными столкновениями
различна, но так как мы имеем дело с
огромным числом молекул и они находятся
в беспорядочном движ-и, то можно говорить
о средней
длине свободного пробега молекул
![]() Эффективное
сечение-
величина, характеризующая вероятность
перехода сис-мы 2 сталкивающихся частиц
в результате их рассеяния (упругого или
неупругого) в определённое конечное
состояние. Э.с. равно отношению числа
dN таких переходов в единицу времени к
плотности nv потока рассеиваемых частиц,
падающих на мишень.Э.с. имеет размерность
площади; обычно оно измеряется в см2.В
часто встречающемся случае упругого
рассеяния пучка частиц, движущихся с
одинаковой скоростью, на некотором
центре, используется дифференциальное
эффективное поперечное сечение
(dσ/dΩ)(определённый телесный угол
dΩ).Интегрирование по полному телесному
углу даёт полное поперечное сечение,
для рассеяния на любые углы:
Эффективное
сечение-
величина, характеризующая вероятность
перехода сис-мы 2 сталкивающихся частиц
в результате их рассеяния (упругого или
неупругого) в определённое конечное
состояние. Э.с. равно отношению числа
dN таких переходов в единицу времени к
плотности nv потока рассеиваемых частиц,
падающих на мишень.Э.с. имеет размерность
площади; обычно оно измеряется в см2.В
часто встречающемся случае упругого
рассеяния пучка частиц, движущихся с
одинаковой скоростью, на некотором
центре, используется дифференциальное
эффективное поперечное сечение
(dσ/dΩ)(определённый телесный угол
dΩ).Интегрирование по полному телесному
углу даёт полное поперечное сечение,
для рассеяния на любые углы:
![]() При наличии
неупругих взаимодействий полное сечение
складывается из сечения для упругих и
неупругих рассеяний. Для каждого типа
неупругих взаимодействий может быть
введено отдельное эффективное сечение.
При наличии
неупругих взаимодействий полное сечение
складывается из сечения для упругих и
неупругих рассеяний. Для каждого типа
неупругих взаимодействий может быть
введено отдельное эффективное сечение.
Общий механизм явлений переносов. Диффузия и теплопроводность в газах, жидкостях и твердых телах. Интегральные уравнения диффузии, теплопроводности и вязкости
В газе, находящемся
в неравновесном состоянии, возникают
необратимые процессы, называемые
явлениями
переноса.В
ходе этих процессов происходит
пространственный перенос вещества
(диффузия), энергии (теплопроводность),
импульса направленного движ-я (вязкое
трение). Если течение процесса не
изменяется со временем, то такой процесс
называется стационарным.Диффузия,
теплопроводность, вязкость являются
необратимыми процессами, возникающими
самопроизвольно вследствие теплового
движ-я при отклонении вещества (газа)
от равновесного состояния.Диффузия-взаимопроникновение
вещества в разл-х смесях, сопровождающееся
направленным переносом массы вещества
из мест с высокой плотностью в места с
меньшей плотностью. Перенос массы
вещества подчиняется закону
Фика:
 где
D – коэф-т диффузии. Масса М
вещества,
перенесенная в результате стационарной
диффузии через площадь S
за время t:
где
D – коэф-т диффузии. Масса М
вещества,
перенесенная в результате стационарной
диффузии через площадь S
за время t: .Согласно
кинетической теории газов,
.Согласно
кинетической теории газов,
 Наиболее
быстро процесс протекает в газе, если
он неоднороден по составу. Значительно
медленнее протекают подобные процессы
в жидкостях. Взаимопроникновение двух
разнородных жидкостей друг в друга,
растворение твердых веществ в жидкостях
(например, сахара в воде) – примеры
диффузионных процессов в жидкостях.
Наиболее медленно процесс диффузии
протекает в твердых телах. Однако, опыты
показывают, что при контакте хорошо
очищенных поверхностей двух металлов
через длительное время в каждом из них
обнаруживается атомы другого
металла.Теплопроводность.Если
в одной области газа средняя кинетическая
энергия молекул больше, чем в другой,
то с течением времени вследствие
постоянных столкновений молекул темп-ра
выравнивается. Процесс передачи энергии
в форме тепла подчиняется закону
Фурье.
Наиболее
быстро процесс протекает в газе, если
он неоднороден по составу. Значительно
медленнее протекают подобные процессы
в жидкостях. Взаимопроникновение двух
разнородных жидкостей друг в друга,
растворение твердых веществ в жидкостях
(например, сахара в воде) – примеры
диффузионных процессов в жидкостях.
Наиболее медленно процесс диффузии
протекает в твердых телах. Однако, опыты
показывают, что при контакте хорошо
очищенных поверхностей двух металлов
через длительное время в каждом из них
обнаруживается атомы другого
металла.Теплопроводность.Если
в одной области газа средняя кинетическая
энергия молекул больше, чем в другой,
то с течением времени вследствие
постоянных столкновений молекул темп-ра
выравнивается. Процесс передачи энергии
в форме тепла подчиняется закону
Фурье.
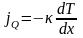 ,где
- коэф-т теплопроводности.Количество
тепла, переносимое в стационарном
процессе теплопроводности через площадь
S
за время t
,где
- коэф-т теплопроводности.Количество
тепла, переносимое в стационарном
процессе теплопроводности через площадь
S
за время t
 .Для
идеального газа
.Для
идеального газа где
cv
– удельная теплоемкость газа при
постоянном объеме,
- плотность газа. Выразим от сюда коэ-т
вязкости
где
cv
– удельная теплоемкость газа при
постоянном объеме,
- плотность газа. Выразим от сюда коэ-т
вязкости .
.
