
- •1. Высокомолекулярные соединения: основные понятия и определения.
- •1. Первичные:
- •2. Вторичные:
- •2. Количественные характеристики длины полимерных молекул.
- •3. Свойства высокомолекулярных соединений, обусловленные цепным строением макромолекул.
- •Высокая вязкость растворов полимеров
- •4) Классификация вмс
- •5) Основные этапы развития полимерной науки и производства. Производство полимеров в Беларуси.
- •6) Структура полимерной цепи. Регулярные и нерегулярные полимеры. Уровни конфигурации макромолекулы.
- •7. Уровни иерархии конформации макромолекулы.
- •Сегмент макромолекулы. Определение понятия. Факторы, определяющие длину статистического сегмента. Методы определения длины статистического сегмента. Жесткоцепные и гибкоцепные вмс.
- •Агрегатные, фазовые и релаксационные состояния полимеров.
- •Релаксационные состояния аморфных вмс. Анализ термомеханической кривой аморфного линейного вмс.
- •13. Высокоэластическое состояние вмс.
- •14. Стеклообразное состояние вмс
- •15. Вязкотекучее состояние вмс
- •Радикальная сополимеризация. Уравнение состава сополимера. Схема Алфея-Прайса (q-e).
- •Кинетика радикальной полимеризации при малых степенях превращения.
- •Мономеры и элементарные реакции радикальной полимеризации.
- •1. Инициирование.
- •2. Рост цепи.
- •3. Обрыв цепи.
- •4. Реакции передачи цепи.
- •19)Цепные процессы образования вмс
- •20) Кинетика поликонденсации
- •21)Особенности синтеза полимеров методом поликонденсации.
- •1. Линейная поликонденсация
- •1 Поликонденсация в расплаве.
- •2 Поликонденсация в растворе.
- •3 Межфазная поликонденсация
- •Полимераналогичные превращения целлюлозы.
- •Реакционная способность мономеров и радикалов в радикальной полимеризации. Гель-эффект.
- •25. Классификация и гидродинамические свойства полиэлектролитов.
- •26. Деструкция и деполимеризация макромолекул. Принципы стабилизации высокомолекулярных соединений.
- •27.Прививочная сополимеризация
- •28. Классификация реакций сшивания макромолекул и особенности сшитых вмс.
- •29) Полимераналогичные превращения полиэтилена.
- •30).Классификация реакций вмс.
- •31) Надмолекулярные, конформационные и конфигурационные эффекты в реакциях вмс
- •32) Способы проведения полимеризации
- •33) Анионная полимеризация
- •34. Кинетика катионной полимеризации
- •35. Катионная полимеризация.
- •36. Необходимые и достаточные условия кристаллизации вмс. Основные структурные элементы Кристаллических вмс.
- •37. Способы ориентации и свойства ориентированных вмс.
- •38. Термодинамические понятия, используемые в теории растворов полимеров.
- •39. Особенности термодинамики полимерных растворов. Энергетика растворения полимеров. Набухание полимеров. Фазовые диаграммы систем полимер-растворитель.
- •40) Вязкость растворов полимеров. Определение молекулярной массы и среднеквадратичного расстояния между концами цепи методом вискозиметрии.
- •Характеристика и применение полимерных материалов: пластомеры, эластомеры, волокна, пленки, клеи.
- •1. Полиэтилен:
- •2 Изотактический полипропилен
- •3) Поливиниловый спирт
- •4) Метилметакрилат.
- •5 Фенолформальдегидные олигомеры
- •6 Полимеры и сополимеры акрилонитрила
- •7 Бутадиен
- •8 Полиизопрен
- •9 Хлоропрен
- •10 Полиэтилентерефталат (пэт)
- •11 Поликапролактам
- •12 Белки
- •13 Полиимиды
- •14 Полиуретан
- •15 Целлюлоза и ее производные
- •16 Полистирол
- •17 Полисилоксан
- •18 Поливинилхлорид
40) Вязкость растворов полимеров. Определение молекулярной массы и среднеквадратичного расстояния между концами цепи методом вискозиметрии.
Вязкость (внутреннее трение жидкости) обусловлена взаимодействием молекул жидкости и проявляется при ее течении. Течение жидкости в капилляре диаметром x характеризуется градиентом скорости dυ/dx вследствие того, что молекулярный слой, непосредственно примыкающий к стенке капилляра, остается неподвижным, а слой, находящийся в центре капилляра, движется с максимальной скоростью. Ламинарное течение жидкости описывается законом Ньютона, согласно которому напряжение сдвига τ, вызывающее течение жидкости, пропорционально градиенту скорости течения:
τ=η*( dυ/dx) Коэффициент пропорциональности η называется коэффициентом вязкости или просто вязкостью.
Вязкость можно рассматривать как меру энергии, рассеиваемой в форме теплоты в процессе течения жидкости. Растворы полимеров обладают более высокой вязкостью по сравнению с низкомолекулярными жидкостями.
Измерение
вязкости жидкостей проводят чаще всего
в капиллярных вискозиметрах. Оно основано
на использовании уравнения
Пуазейля
Q= (III.15)
(III.15)
где Q – количество жидкости, протекающей через капилляр за время t; r, l – радиус и длина капилляра соответственно; ∆Р – разность давлений на концах капилляра.
Если жидкость течет под действием собственного веса, то ∆Р=∆h*ρ*g (здесь ∆h – высота столба жидкости в приборе; ρ – плотность жидкости; g – ускорение свободного падения): η=К*ρ*t, где К=(πr4∆hg)/8Ql называется постоянной вискозиметра
При исследовании разбавленных растворов полимеров определяют обычно вязкость относительную при условии, что плотности разбавленного раствора и чистого растворителя практически совпадают, равно ηотн=η/η0=t/t0, где t и t0 – времена истечения соответственно раствора и чистого растворителя. Отношение (η – η0)/η0 показывает относительный прирост вязкости вследствие введения в растворитель полимера и называется удельной вязкостью ηуд, отношение ηуд/С – приведенной вязкостью ηпр и limηуд/С при С→0 называется характеристической вязкостью [η].
Вязкость разбавленного раствора непроницаемых сплошных невзаимодействующих сферических частиц описывается формулой Эйнштейна: η/η0=1+ 2,5φ
где φ – объемная доля растворенного вещества; 2,5 – коэффициент, учитывающий гидродинамическое взаимодействие жесткой сферической частицы со средой.
Уравнение Энштейна означает, что характеристическая вязкость раствора сплошных невзаимодействующих частиц (не обязательно сферических, тогда коэффициент 2,5 будет другим) определяется только плотностью вещества и не зависит от молекулярной массы и размеров частиц. Это происходит вследствие того, что масса таких частиц строго пропорциональна их объему.
Допустим для простоты, что макромолекулярный клубок в θ-растворителе имеет форму шара радиуса Rе (радиус эквивалентной сферы), который примем равным R¯g (среднему радиусу инерции). Считая эти частицы непроницаемыми для растворителя в потоке, можно применить к ним уравнение Энштейна, причем объемная доля вещества в этом случае учитывает не собственный объем макромолекул, а их эффективный объем в растворе вместе с включенным в них растворителем. Тогда, учитывая, что в θ-условиях R¯g2=ћ2θ/6, преобразуем уравнение (III.16) к виду
[η]=2,5 π(ћ2θ/6)3/2
π(ћ2θ/6)3/2
 =Ф*((ћ2θ)3/2
/М)
(III.17)
=Ф*((ћ2θ)3/2
/М)
(III.17)
Это формула Флори-Фокса для вязкости полимера в θ-растворителе. Здесь Ф – постоянная Флори, в первом приближении не зависящая от свойств полимера.
В условиях, отличных от θ-условий, например в хороших растворителях, молекулярный клубок дополнительно набухает. Принимая, что формула Флори-Фокса справедлива также для раствора «полимер в хорошем растворителе» и подставляя значение (h2)1/2 из выражения (III.11) в уравнение (III.17), получим:
[η]=Ф Сопоставляя
это уравнение с уравнением (III.17)
и пренебрегая зависимостью Ф
от
качества растворителя (что, вообще
говоря, не вполне справедливо), можно
оценить коэффициент набухания
макромолекулы:
Сопоставляя
это уравнение с уравнением (III.17)
и пренебрегая зависимостью Ф
от
качества растворителя (что, вообще
говоря, не вполне справедливо), можно
оценить коэффициент набухания
макромолекулы:
α= (III.18)
(III.18)
Большинство полимеров в растворах ведут себя отлично от эйнштейновских частиц, и для них наблюдается зависимость характеристической вязкости от молекулярной массы полимера. Эта зависимость обусловлена тем, что либо эффективный объем макромолекулярного клубка в растворе растет быстрее, чем его молекулярная масса, либо тем, что клубок имеет несферическую форму и частично проницаем для потока растворителя.
Выражая (ћ2)θ1/2 через молекулярную массу полимера: (ћ2)θ=zb2=Mb2/Mc (где Мс – молекулярная масса сегмента) и подставляя это значение в уравнение (III.17), получим:
[η]θ=Ф =KθM1/2
=KθM1/2
Это уравнение связывает характеристическую вязкость с молекулярной массой полимера в θ-условиях.
Для раствора полимера в любом растворителе имеем:
[η]=Ф (III.19)-
уравнения
Марка-Куна-Хаувинка.
(III.19)-
уравнения
Марка-Куна-Хаувинка.
Постоянная К=10-2÷10-5 зависит от температуры и природы полимера и растворителя. а изменяется в пределах: 0≤а≤2,0.
Зависимость приведенной вязкости от концентрации раствора полимера (рис. III.9) описывается уравнением Хаггинса:
ηуд/С=[η]+К'[η]2С (III.21)
где К' – константа Хаггинса, характеризующая взаимодействие макромолекул в данном растворителе.
В хороших растворителях К'=0,2-0,3, в плохих - К'≥0,5.
Характеристическая вязкость определяет поведение изолированных макромолекул. Она представляет собой меру потерь энергии на трение изолированных макромолекул о растворитель при их вращении в результате поступательного движения в потоке с градиентом скорости, отличным от нуля. Характеристическая вязкость зависит от размеров макромолекул в растворе, от природы растворителя и температуры раствора. В хорошем растворителе макромолекулярный клубок набухает и вязкость увеличивается.
Раствор можно считать разбавленным, если для него С<<1/[η]. Последнее неравенство означает, что объем раствора, занятый макромолекулами, значительно меньше общего объема раствора. Раствор считают умеренно концентрированным при условии С≈1/[η] и концентрированным – при С>>1/[η].
Константы К и а не зависят от молекулярной массы, для вязкости раствора полидисперсного полимера можно написать:
ηуд= =КМ¯ηа
откуда
М¯η=
=КМ¯ηа
откуда
М¯η=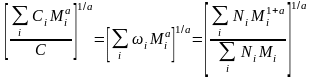
Сопоставляя это уравнение с уравнением (III.13), можно заключить, что М¯η= М¯ω только в частном случае при а=1.
Характеристические вязкости и молекулярные массы для одного и того же полимера, измеренные в двух разных растворителях, для которых константы а уравнения Марка-Куна-Хаувинка различны (например, в хорошем и плохом растворителях), различаются:
М¯η1= ;
М¯η2=
;
М¯η2=
Это обусловлено тем, что в хорошем растворителе макромолекулярные клубки находятся в относительно набухшем состоянии и средняя молекулярная масса более чувствительна к присутствию высокомолекулярной фракции, тогда как в плохом растворителе макромолекулы имеют более компактные конформации и вклады макромолекул разной длины различаются в меньшей степени. Отношение М¯η1/ М¯η2 может служить мерой полидисперсности, как и отношение М¯ω/ М¯n. Чем больше разность между а1 и а2, тем чувствительнее эта характеристика.
