
- •1. Высокомолекулярные соединения: основные понятия и определения.
- •1. Первичные:
- •2. Вторичные:
- •2. Количественные характеристики длины полимерных молекул.
- •3. Свойства высокомолекулярных соединений, обусловленные цепным строением макромолекул.
- •Высокая вязкость растворов полимеров
- •4) Классификация вмс
- •5) Основные этапы развития полимерной науки и производства. Производство полимеров в Беларуси.
- •6) Структура полимерной цепи. Регулярные и нерегулярные полимеры. Уровни конфигурации макромолекулы.
- •7. Уровни иерархии конформации макромолекулы.
- •Сегмент макромолекулы. Определение понятия. Факторы, определяющие длину статистического сегмента. Методы определения длины статистического сегмента. Жесткоцепные и гибкоцепные вмс.
- •Агрегатные, фазовые и релаксационные состояния полимеров.
- •Релаксационные состояния аморфных вмс. Анализ термомеханической кривой аморфного линейного вмс.
- •13. Высокоэластическое состояние вмс.
- •14. Стеклообразное состояние вмс
- •15. Вязкотекучее состояние вмс
- •Радикальная сополимеризация. Уравнение состава сополимера. Схема Алфея-Прайса (q-e).
- •Кинетика радикальной полимеризации при малых степенях превращения.
- •Мономеры и элементарные реакции радикальной полимеризации.
- •1. Инициирование.
- •2. Рост цепи.
- •3. Обрыв цепи.
- •4. Реакции передачи цепи.
- •19)Цепные процессы образования вмс
- •20) Кинетика поликонденсации
- •21)Особенности синтеза полимеров методом поликонденсации.
- •1. Линейная поликонденсация
- •1 Поликонденсация в расплаве.
- •2 Поликонденсация в растворе.
- •3 Межфазная поликонденсация
- •Полимераналогичные превращения целлюлозы.
- •Реакционная способность мономеров и радикалов в радикальной полимеризации. Гель-эффект.
- •25. Классификация и гидродинамические свойства полиэлектролитов.
- •26. Деструкция и деполимеризация макромолекул. Принципы стабилизации высокомолекулярных соединений.
- •27.Прививочная сополимеризация
- •28. Классификация реакций сшивания макромолекул и особенности сшитых вмс.
- •29) Полимераналогичные превращения полиэтилена.
- •30).Классификация реакций вмс.
- •31) Надмолекулярные, конформационные и конфигурационные эффекты в реакциях вмс
- •32) Способы проведения полимеризации
- •33) Анионная полимеризация
- •34. Кинетика катионной полимеризации
- •35. Катионная полимеризация.
- •36. Необходимые и достаточные условия кристаллизации вмс. Основные структурные элементы Кристаллических вмс.
- •37. Способы ориентации и свойства ориентированных вмс.
- •38. Термодинамические понятия, используемые в теории растворов полимеров.
- •39. Особенности термодинамики полимерных растворов. Энергетика растворения полимеров. Набухание полимеров. Фазовые диаграммы систем полимер-растворитель.
- •40) Вязкость растворов полимеров. Определение молекулярной массы и среднеквадратичного расстояния между концами цепи методом вискозиметрии.
- •Характеристика и применение полимерных материалов: пластомеры, эластомеры, волокна, пленки, клеи.
- •1. Полиэтилен:
- •2 Изотактический полипропилен
- •3) Поливиниловый спирт
- •4) Метилметакрилат.
- •5 Фенолформальдегидные олигомеры
- •6 Полимеры и сополимеры акрилонитрила
- •7 Бутадиен
- •8 Полиизопрен
- •9 Хлоропрен
- •10 Полиэтилентерефталат (пэт)
- •11 Поликапролактам
- •12 Белки
- •13 Полиимиды
- •14 Полиуретан
- •15 Целлюлоза и ее производные
- •16 Полистирол
- •17 Полисилоксан
- •18 Поливинилхлорид
34. Кинетика катионной полимеризации
Кинетика катионной полимеризации сильно зависит от способа ограничения цепи.
1. Перегруппировка растущей ионной пары (передача цепи на противоион):
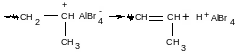
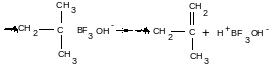
(H2O – сокатализатор)
Такая реакция была обнаружена по фиксации двойной связи на конце цепи.

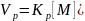
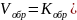
Руководствуясь
принципом стационарности Боденштейна:
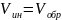
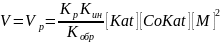
В отличие от радикальной полимеризации имеет второй порядок по мономеру.
Вывод и анализ основного уравнения кинетики катионной полимеризации
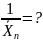 ;
;
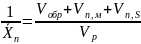 , где
, где
 - скорость передачи цепи на растворитель
- скорость передачи цепи на растворитель
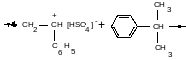
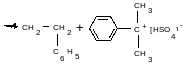
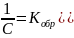
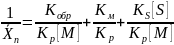
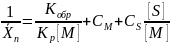
1)
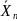 не зависит от
не зависит от
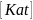 .
Если в основном работает передча цепи,
то в это случае
.
Если в основном работает передча цепи,
то в это случае
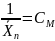 не зависит от [M].
не зависит от [M].
2) C увеличением температуры скорость уменьшается.
Необходимо сопоставить Еакт всех элементарных стадий (процессов роста и обрыва цепи). Еакт (обрыва) (т.к. идет разрыв σ-связи) > Еакт (роста) (гетеролитический разрыв π-связи).
С увеличением температуры более интенсивными становятся процессы гибели материальных цепей. Молекулярная масса уменьшается.
3) Полярность среды (диэлектрическая постоянная среды).
При увеличении полярности среды увеличивается молекулярная масса ВМС. Полярность среды определяет степень разделенности ионной пары. Чем больше полярность среды, тем больше сольватационная способность среды. Процессы инициирования, роста цепи ускоряются, обрыв цепи замедляется (осн. обрыв – мономолекулярная перегруппировка ионной пары, чем больше она разделена, тем меньше скорость процесса).
35. Катионная полимеризация.
Катализаторы катионной полимеризации – кислоты (HClO4, H2SO4, H3PO4, НСl – протонные кислоты; AlCl3, BF3, SnCl4, TiCl4, FeCl3, ZnCl2, TiBr4 – апротонные, кислоты Льюиса или катализаторы Фриделя-Крафтса).
Сокатализаторы: галогеноводороды, спирты.
Элементарные стадии катионной полимеризации.
Инициирование
М – пропилен; кат - AlBr3, сокат – НBr, температура процесса – 60-50°С.
1) НBr + AlBr3 ↔ H+[ AlBr4]- - кислота Бренстеда.
2) σ- σ+
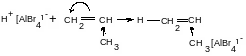 противоион
противоион
H+ притягивает π-электроны двойной связи, поэтому вся пара переходит к Н+ (гетеролитический процесс) => σ-связь между β-углеродным атомом, т.к. это отрицательный конец диполя. Активный центр – ионная пара.
Рост цепи
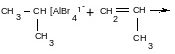
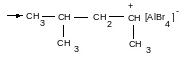 дополнительная
поляризация молекулы мономера в поле
действия ионной пары → α–β – конфигурация
диады → карбокатион притягивает
π-электроны двойной связи =>
гетеролитический разрыв => σ-связь.
дополнительная
поляризация молекулы мономера в поле
действия ионной пары → α–β – конфигурация
диады → карбокатион притягивает
π-электроны двойной связи =>
гетеролитический разрыв => σ-связь.
Обрыв цепи: мономолекулярный
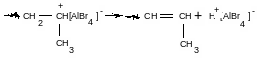
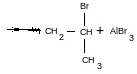
Обрыв цепи – когда макроион имеет большие размеры. Протон отдается противоиону.
Это обрыв материальной цепи, кинетическая цепь жива.
Самопроизвольный обрыв цепи в результате уменьшения кинетической подвижности макрокатиона из-за увеличения его размера.
Соединение макрокатиона с анионным фрагментом противоиона.
Произошла регенерация катализатора. Уменьшается концентрация комплекса катализатор-сокатализатор.
Передача цепи при катионной полимеризации.
1) на мономер (одна из наиболее характерных реакций цепи при катионной полимеризации)
Может осуществляться 2-мя способами:
а) межмолекулярная передача H+
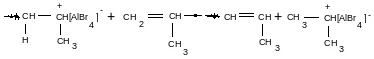
Эти реакции кинетически не отличимы.
б) передача цепи на полимер
вторичный катион
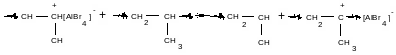 полученного
полипропилена невелика в силу передачи
цепи на полимер.
полученного
полипропилена невелика в силу передачи
цепи на полимер.
в) передача цепи на сокатализатор
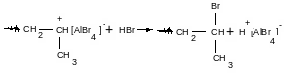
При инициировании апротонными кислотами выше, чем при использовании протонных кислот.
