
- •§1 Енергія та її види. Предмет та метод технічної термодинаміки
- •§2 Термодинамічна система
- •§3 Термодинамічні параметри робочого тіла і термодинамічний стан
- •Лекція 2. . (стор.12-19)
- •§4 Термодинамічна рівновага
- •§5 Загальні властивості термодинамічних параметрів стану
- •§6 Основні параметри стану
- •§7 Рівняння стану ідеального газу
- •§8 Рівняння стану сумішей ідеальних газів (стор. 19-27)(самостійно)
- •§9 Теплоємність
- •1 Кмоль – μс - мольна..
- •§10 Внутрішня енергія (стор. 28-31)
- •§11 Форми енергообміну термодинамічної системи. Теплота і робота
- •§13 Повна енергія робочого тіла або ентальпія (стор. 47-49)
- •Лекція 4. .
- •§14 Вільна та зв’язана енергія. Поняття ентропії (стор. 50-54)
- •15. Термодинамічний процес. Оборотний і необоротний термодинамічні процеси (стор. 54-59)
- •Лекція 5.
- •§17. Перший закон термодинаміки (стор. 59-72)
- •§18. Другий закон термодинаміки (стор. 77-92)
- •Лекція 6.
- •§19. Термодинамічні потенціали та їх диференціальні рівняння (стор. 59-77)
- •§20. Обчислення ентропії
- •Тема 2 Дослідження енергетичної ефективності термодинамічних процесів ідеальних газів (стор. 106-143)
- •§1 Характеристики термодинамічного процесу
- •Лекція 7.
- •2. Ізотермічний процес.
- •3. Ізобарний процес
- •4. Ізохорний процес
- •5. Адіабатний процес
- •§6. Політропний процес
- •Тема 3 Механізм отримання роботи
- •Лекція 8. 8.10..
- •Тема 4 Водяна пара як реальний газ
- •§1 Рівняння стану реального газу (стор. 155-160)
- •§2 Загальні властивості реальних газів (стор. 160-161)
- •§3 Водяна пара. Основні визначення (стор. 162-166)
- •Лекція 9. 15.10..
- •§4 Процес пароутворення. Pv-діаграма водяної пари (стор. 166-169)
- •§6 Параметри стану води та водяної пари
- •§7 Параметри вологої насиченої пари
- •§8 Основні термодинамічні процеси водяної пари (стор. 182-188)
- •Тема 6 Вологе повітря
- •Лекція 11. 23.10.. Вологе повітря(продовження)
- •§2 Характеристики вологого повітря
- •Тема 7 Термодинаміка потоку газів і пари (відкрита термодинамічна система)
- •§1 Рівняння першого закону термодинаміки для відкритих систем (стор. 198-206)
- •§2 Основні закономірності протікання газу і пари в коротких каналах змінного перерізу (стор. 206-211)
- •Лекція 13. 29.10..
- •§3 Визначення маси при протіканні робочого тіла через сопло. Критичні характеристики потоку. Рівняння нерозривності потоку
- •§4 Вибір форми сопла. Розрахунок комбінованого сопла
- •§5 Дроселювання газів і пари
- •§6 Дроселювання водяної пари
- •Загальні термодинамічні властивості кругових термодинамічних процесів або циклів
- •§1 Класифікація і загальна характеристика термодинамічних циклів (стор. 230-242)
- •§2 Прямий оборотний цикл Карно (1824р.)(стор. 242-246)
- •§3 Зворотний оборотний цикл Карно
- •§4 Теореми Карно (стор. 248-250)
- •Тема 9 Термодинамічні потенціали та ексергія (стор. 258-271)
- •Лекція 16. 13.11.
- •Лекція 17. 20.11.. Економічна ефективність перетворення енергії
- •Тема 10 Стиснення (нагнітання робочих тіл) (стор. 272-283) Ідеальний поршневий одноступінчатий компресор
- •Багатоступінчате стиснення
- •Тема 11 Цикли двигунів внутрішнього згоряння (двз)
- •§1 Класифікація циклів двз
- •§2 Цикл двз з ізохорним підведенням теплоти (цикл Отто,1877р.)
- •Лекція №18 Теоретичний цикл Отто
- •§3 Цикл двз з підведенням теплоти під час сталого об’єму і сталого тиску. Цикл Тринклера (1904р)
- •Лекція 19. .
- •Тема 12 Цикл газотурбінної установки (гту)
- •Тема 13 Цикли паросилових установок (псу)
- •§1 Цикл Карно для водяної пари
- •Л.18.29 11*§2 Схема та робочий процес паросилової установки – цикл Ренкіна (стор. 320-329)
- •Лекція 20. 11.12.. Термічний ккд циклу Ренкіна
- •*§3 Вплив на термічний ккд циклу Ренкіна параметрів пари
- •Лекція 21. 18.12..
- •§4 Теплофікаційний цикл псу (стор. 338-341)схема
- •*§5 Узагальнений (регенеративний) цикл Карно (стор. 250-252)
- •*§7 Середньоінтегральна температура (стор. 252)
- •§8 Еквівалентний цикл Карно (стор. 253-254)
- •§9 Еталонний цикл Карно (стор.254)
- •*§10 Регенеративний цикл паросилової установки (стор. 332-337)
- •Тема 14 Парогазові цикли
- •Лекція 22. 25.12..
- •Тема 15 *Установки, що працюють за зворотними циклами (стор. 348-359)
- •§1 Загальна характеристика холодильних установок
- •§2 Цикл парової компресійної холодильної установки (стор. 354-357)
- •§3 Цикл теплового насоса (стор. 362-364)
§9 Теплоємність
Теплоємністю називається похідна від кількості теплоти по температурі, під час якої підводиться теплота.
 ;
;
х
– означає умови, під час яких підво-диться
теплота. Вимірюється в
![]() .
.
Питомою називають теплоємність, яка віднесена до одної кількісної одиниці речовини. Коли за кількісну одиницю приймають 1 кг, тоді теплоємність називають масова питома теплоємність.
1 кг – с -масова,
1
м3
– с´
![]() -обємна,
-обємна,
1 Кмоль – μс - мольна..
![]() ;
;
![]() ,
,
![]() – щільність
речовини.
– щільність
речовини.
Для реального газу теплоємність є фун-кція тиску і температури. Для ідеального газу теплоємність залежить тільки від тем-ператури. Ця залежність може бути:
Криволінійною:


Прямолінійною:


не залежить від температури:

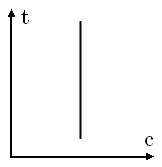
Теплоємність
визначається за таблицями, до
![]() можна вважати, що вона не залежить від
температури.
можна вважати, що вона не залежить від
температури.
Розглядають теплоємність середню та істинну.
Середньою називають таку умовну теп-лоємність, під час якої робоче тіло в межах даних температур поглинає таку ж кількість теплоти, яку воно поглинає під час змінної теплоємності в межах тих же температур.
![]()
![]() – кількість
теплоти, яка підведена в межах даних
температур;
– кількість
теплоти, яка підведена в межах даних
температур;
![]() – межі
температур робочого тіла.
– межі
температур робочого тіла.
Істинною теплоємністю називається границя, до якої прямує середня тепломність під час прямування різниці температур до нуля.
![]()
під час криволінійної залежності від температури теплоємність визначається як:

під час прямолінійної:

Теплоємність
робочого тіла залежить від умов, під
час яких підводиться теплота. Розглядають
теплоємність під час
![]() та під час
та під час
![]() .
.
![]()
Роберт Майєр показав, що:
![]()

Якщо ми вважаємо, що теплоємність не залежить від температури, то її знаходять через мольну теплоємність.
![]()
М ольна
теплоємність
залежить від атомності
газу.
ольна
теплоємність
залежить від атомності
газу.
Тип газу |
|
|
кДж/К |
кмоль/К |
|
1-атомний |
12,5 |
20,8 |
2-атомний |
20,8 |
29,1 |
3-атомний |
29,1 |
37,4 |
![]()
§10 Внутрішня енергія (стор. 28-31)
Внутрішньою енергією називається сума кінетичної і потенціальної енергії молекул газу.
u – 1 кг, Дж/кг
U – m кг, Дж
![]()
Кінетична енергія молекул визначається швидкістю руху молекул, поступального і обертального. Потенціальна енергія виз-начається силами щеплення між молеку-лами, а також розташуванням молекул у просторі. Тому для ідеального газу
![]() ,
,
![]() – маса
1 молекули;
– маса
1 молекули;
![]() – середня
швидкість руху молекул.
– середня
швидкість руху молекул.
Для
реального газу
![]() .
.
Джоуль,
вивчаючи властивості газопо-дібних
речовин, показав, що для ідеального газу
![]() і тому
і тому
 (1)
(1)
Внутрішня енергія є параметр стану, їй притаманні всі властивості параметрів ста-ну.
![]()
Для реального газу
![]()
![]()
![]()
§11 Форми енергообміну термодинамічної системи. Теплота і робота
Термодинамічні системи обмінюються між собою енергією, і внутрішня енергія під час цього передається у двох формах: у формі теплоти і у формі роботи.
Розглянемо два тіла, які знаходя-ться між собою в контакті. Одне із них має температуру
 ,
друге –
,
друге –
 ,
причому
>
.
,
причому
>
.

Якщо два тіла, які мають різні темпера-тури, знаходяться у контакті і обмінюються енергією, яка передається більш нагрітим тілом менш нагрітому у формі енергії хао-тичного руху молекул, то така енергія називається теплотою. Сам процес називається теплообміном, і кількість енергії, яка передається, називається кількістю теплоти.
Теплота Q – m кг, Дж, кДж
q
– 1 кг,
,
![]() .
.
Визначається теплота так:
![]() (4.1)
(4.1)
![]() (4.2)
(4.2)
У робочому тілі теплоти немає. У ньому є лише внутрішня енергія. Теплота не є окремий вид енергії.
Якщо два тіла знаходяться у кон-такті, і одне з них розширюється, збільшує свій об’єм і зміщує друге тіло, то така форма переносу енергії від одного тіла до іншого називається роботою. Сам процес і кількість енергії теж називається роботою.
![]() – m
кг, Дж, кДж
– m
кг, Дж, кДж
![]() – 1
кг,
,
.
– 1
кг,
,
.
 ;
;

