
- •Іщенко а.В.
- •Понятие об атомах
- •1.2. Молекулы, радикалы и ионы
- •1.3. Основные понятия и законы химии
- •2. Строение атомов
- •2.1 Электронная оболочка атома
- •2.2 Система квантовых чисел
- •2.3 Законы, определяющие положение электронов в атоме
- •4. Первый закон Клечковского
- •5. Второй закон Клечковского
- •3. Периодическая таблица Менделеева
- •3.2 Формирование больших периодов
- •3.3 Группы таблицы Менделеева
- •4. Теория химической связи
- •4.1 Ионная связь
- •4.2 Ковалентная связь
- •Донорно – акцепторный механизм ковалентной связи
- •4.3 Водородная связь
- •Способы выражения концентрации растворов
- •Применимость закона действия масс
- •Сильные и слабые электролиты
- •Степень диссоциации. Константа электролитической диссоциации
- •Химическая активность. Ионная сила раствора
- •Гидролиз солей Определения
- •Ионное произведение воды Водородный показатель
- •Три случая гидролиза солей
- •Первый случай гидролиза
- •Второй случай гидролиза
- •Третий случай гидролиза
- •Количественные характеристики гидролиза
- •Кислота является либо легколетучей, либо трудно растворимой и её константа диссоциации не превышает 10-7.
- •Основание является трудно растворимым соединением и её константа диссоциации не превышает 10-8.
- •Способы подавления гидролиза солей
- •Первый способ - регулирование рн солевого раствора
- •Понижение температуры солевого раствора ,
- •Важным свойством буферных растворов является их способность сохранять постоянное значение рН при разбавлении раствора.
- •Комплексные соединения
- •Система названий комплексных соединений
- •1. Анион внешней сферы. 2. Катион внутренней сферы:
- •1. Комплексный анион:
- •2. Катион внешней сферы.
- •Диссоциация комплексных соединений и ионов
- •Классификация комплексных соединений
- •Применение комплексных соединений
- •Окислительно - восстановителные реакции
- •Тема: основы аналитической химии.
- •Общие аналитические свойства элементов. Цель и задачи аналитической химии.
- •Правильность и точность анализа.
- •Понятие о химических и физико-химических методах анализа.
- •Группы методов анализа.
- •3. Классификация методов количественного анализа
- •4. Качественный анализ
- •Методы качественного анализа
- •«Мокрый метод»
- •4.2. Кислотно-основная классификация катионов
- •4.3. Кислотно-щелочная классификация анионов
- •5. Количественный анализ
- •5.1 Гравиметрический метод анализа
- •5.1.1. Общая характеристика метода.
- •5.1.2. Требования к осадкам
- •5.1.3. Требования к весовой форме:
- •5.1.4. Осаждающие реагенты
- •5.1.5.Расчетные формулы в гравиметрии.
- •5.1.6. Основные положения гравиметрии.
- •5.2. Титриметрический метод анализа.
- •5.2.1. Общая характеристика метода.
- •5.2.2. Требования к реакциям в титриметрическом методе.
- •5.2.3. Определение точки эквивалентности.
- •По собственной окраске ионов определяемого элемента, например марганца в виде аниона MnO4-
- •По веществу-свидетелю
- •Классификация методов титриметрического анализа.
- •5.2.5. Способы титрования.
- •5.2.6. Расчеты в титриметрическом анализе.
- •5.2.7. Основные положения титриметрического метода.
- •2. Реакции спиртов с галогеноводородами (sn) (см. Получение галогенугдеводородов)
- •3. Образование простых эфиров
- •4. Образование сложных эфиров (этерификация)
- •5. Окислительно-восстановительные реакции
5.2.6. Расчеты в титриметрическом анализе.
N1V1 = N xV x,
где N1 – нормальность титранта
V1 – количество раствора, которое вылили из бюретки для химической реакции
N xV x – характеристика искомого вещества
![]()
![]()
а – навеска анализируемого вещества
5.2.7. Основные положения титриметрического метода.
1. В титриметрии концентрацию определяют, измеряя объем стандартного или титрованного реагента (титранта), израсходованного в химической реакции с определяемым веществом в растворе (или газовой фазе). Измерение проводят с помощью процедуры титрования. Это простой, относительно быстрый, универсальный и точный метод.
2. При титровании титрант добавляют порциями или непрерывно с небольшой постоянной скоростью и измеряют его объем до тех пор, пока не будет достигнута точка эквивалентности, отвечающая объему титранта, при котором в реакцию вступает все определяемое вещество.
3. Точку эквивалентности находят, непрерывно следя за изменением тех или иных свойств титруемого раствора (цвета, оптической плотности, электрохимических свойств и т.д.) при помощи специальных приборов или визуально.
4. Чтобы данную химическую реакцию можно было использовать в титровании, участвующие в ней вещества должны находиться в строго определенных количественных (стехиометрических) соотношениях. Реакция должна протекать быстро и практически до конца, а точка эквивалентности точно фиксироваться.
5. Чаще всего используют реакции нейтрализации (кислотно-основные), комплексообразования и окислительно-восстановительные. Реакции нейтрализации распространены наиболее широко; именно их мы и рассмотрим для пояснения ключевых моментов всех реакций титрования.
6. Кривые титрования. Кривая титрования – это график зависимости pH, оптической плотности или каких-либо других характеристик титруемого раствора (ось ординат) от объема добавленного титранта (ось абсцисс). Масштаб оси абсцисс всегда линейный, а оси ординат может быть линейным или логарифмическим. Логарифмический масштаб часто используют при визуальном определении конечной точки титрования, поскольку именно в этом масштабе наиболее наглядно проявляется резкое изменение свойств раствора вблизи точки эквивалентности.
7. Зависимость кривых титрования от концентрации и константы равновесия. Для точного определения конечной точки титрования необходимо, чтобы на кривой титрования вблизи точки эквивалентности наблюдался перегиб (скачок). Это требование устанавливает пределы как для минимальной определяемой концентрации, так и для минимальной константы равновесия, приемлемой для реакции титрования.
8. Чтобы визуальное определение конечной точки титрования было надежным, константа равновесия не должна быть меньше 106. При инструментальном контроле титрования или расчете положения конечной точки титрования на основании полученных данных константа равновесия может составлять всего 102.
МОДУЛЬ 3.
Лекция 4.
Основные понятия органической химии. Насыщенные углеводороды: свойства, применение и методы анализа.
ОРГАНИКА
Основным элементом, входящим в состав органических соединений, является углерод. Поэтому А.М. Бутлеров определил органическую химию как химию соединений углерода. Однако существуют простые вещества, содержащие углерод (СО; СО2; СS2, соли синильной кислоты и др.), которые относят к неорганическим соединениям и изучают в курсе общей или неорганической химии. Учитывая это, более точно органическую химию следует определять как химию углеводородов и их производных, в состав которых могут входить почти все элементы периодической системы.
Углерод
Символ С, элемент IVA группы 2-го периода периодической системы элементов атомный номер 6; атомная масса 12,01115. Электронная конфигурация в основном состоянии 1s22s22p2. Углерод - особый элемент. Ни один другой химический элемент не способен образовывать такое многообразие соединений. Причина этого многобразия в том, что атомы углерода способны:
соединяться друг с другом в цепи различного строения: открытые (неразветвленные, разветвленные), замкнутые:

 |
| | | | | |
|
| | | | | |
-c-c-c-c- -c-c-c- c
| | | | | | |
-c- >c c <
| | |

 c
c
<
c
c
<
c
2) образовывать не только простые (одинарные), но и кратные (двойные, тройные) связи: > С = С < - С = С - -С=С-С=С-
3) образовывать прочные связи почти с любым другим элементом.
Эти уникальные свойства углерода объясняются сочетанием двух факторов:
наличие на внешнем энергетическом уровне (2s и 2p) четырех электронов (поэтому атом углерода не склонен ни терять, ни приобретать свободные электроны с образованием ионов) и четырехвалентных орбиталей;
малый размер атома (в сравнении с другими элементами IV группы).
Вследствие этого углерод образует главным образом ковалентные, а не ионные связи, и проявляет валентность, равную 4.
Органические соединения
Критерием деления соединений на органические и неорганические служит их элементный состав.
К органическим соединениям относятся химические вещества, содержащие в своем составе углеродные цепи, в которых большинство из оставшихся валентностей углерода расходуются на связь с водородом. Кстати, у водорода, также как и у углерода, число валентных электронов и орбиталей одинаково. У других элементов такое соответствие отсутствует.
Органические соединения отличаются от неорганических рядом характерных особенностей:
почти все органические вещества горят или легко разрушаются при нагревании с окислителями, выделяя СО2 (по этому признаку можно установить принадлежность исследуемого вещества к органическим соединениям);
в молекулах органических соединений углерод может быть соединен почти с любым элементом Периодической системы;
органические молекулы могут содержать последовательность атомов углерода, соединенных в цепи (открытые или замкнутые);
молекулы большинства органических соединений не диссоциирует на достаточно устойчивые ионы;
реакции органических соединений протекают значительно медленнее и в большинстве случаев не доходят до конца;
среди органических соединений широко распространено явление изомерии;
органические вещества имеют более низкие температуры фазовых переходов (т.кип., т.пл.).
Теория строения органических веществ А.М.Бутлерова
Решающая роль в создании теории строения органических соединений принадлежит великому русскому ученому Александру Михайловичу Бутлерову. 19 сентября 1861 года на 36-м съезде немецких естествоиспытателей А.М.Бутлеров обнародовал ее в докладе "О химическом строении вещества".
Основные положения теории химического строения А.М.Бутлерова можно свести к следующему.
1. Все атомы в молекуле органического соединения связаны друг с другом в определенной последовательности в соответствии с их валентностью. Изменение последовательности расположения атомов приводит к образованию нового вещества с новыми свойствами. Например, составу вещества С2Н6О отвечают два разных соединения: диметиловый эфир (СН3–О–СН3) и этиловый спирт (С2Н5ОН).
2. Свойства веществ зависят от их химического строения. Химическое строение – это определенный порядок в чередовании атомов в молекуле, во взаимодействии и взаимном влиянии атомов друг на друга – как соседних, так и через другие атомы. В результате каждое вещество имеет свои особые физические и химические свойства. Например, диметиловый эфир – это газ без запаха, нерастворимый в воде, t°пл. = -138°C, t°кип. = 23,6°C; этиловый спирт – жидкость с запахом, растворимая в воде, t°пл. = -114,5°C, t°кип. = 78,3°C. Данное положение теории строения органических веществ объяснило явление изомерии, широко распространенное в органической химии. Приведенная пара соединений – диметиловый эфир и этиловый спирт – один из примеров, иллюстрирующих явление изомерии.
3. Изучение свойств веществ позволяет определить их химическое строение, а химическое строение веществ определяет их физические и химические свойства.
4. Атомы углерода способны соединятся между собой, образовывая углеродные цепи различного вида. Они могут быть как открытыми, так и замкнутыми (циклическими), как прямыми, так и разветвленными. В зависимости от числа связей, затрачиваемых атомами углерода на соединение друг с другом, цепи могут быть насыщенными (с одинарными связями) или ненасыщенными (с двойными и тройными связями).
5. Каждое органическое соединение имеет одну определенную формулу строения или структурную формулу, которую строят, основываясь на положении о четырехвалентном углероде и способности его атомов образовывать цепи и циклы. Строение молекулы как реального объекта можно изучить экспериментально химическими и физическими методами.
А.М.Бутлеров не ограничился теоретическими объяснениями своей теории строения органических соединений. Он провел ряд экспериментов, подтвердив предсказания теории получением изобутана, трет. бутилового спирта и т.д. Это дало возможность А.М.Бутлерову заявить в 1864 году, что имеющиеся факты позволяют ручаться за возможность синтетического получения любого органического вещества.
В дальнейшем развитии и обосновании теории строения органических соединений большую роль сыграли последователи Бутлерова - В.В.Марковников, Е.Е.Вагнер, Н.Д.Зелинский, А.Н.Несмеянов и др.
Современный период развития органической химии в области теории характеризуется все возрастающим проникновением методов квантовой механики в органическую химию. С их помощью решаются вопросы о причинах тех или иных проявлений взаимного влияния атомов в молекулах.
В области развития органического синтеза современный период характеризуется значительными успехами в получении многочисленных органических соединений, в число которых входят природные вещества - антибиотики, разнообразные лекарственные соединения, многочисленные высокомолекулярные соединения.
Органическая химия глубоко проникла в сферу физиологии. Так, с химической точки зрения изучена гормональная функция организма, механизм передачи нервных импульсов. Ученые вплотную подошли к разрешению вопроса о строении и синтезе белка.
Органическая химия как самостоятельная наука продолжает существовать и интенсивно развиваться. Это объясняется следующими причинами:
1. Многообразием органических соединений, обусловленным тем, что углерод в отличие от других элементов способен соединяться друг с другом, давая длинные цепочки (изомеры). В настоящее время известно около 20 млн органических соединений, в то время как неорганических - только около 700 тысяч.
2. Сложностью молекул органических веществ, содержащих до 10 тысяч атомов (например, природные биополимеры - белки, углеводы).
3. Специфичностью свойств органических соединений по сравнению с неорганическими (неустойчивостью при сравнительно невысоких температурах, низкой – до 300°С – температурой плавления, горючестью).
4. Медленно идущими реакциями между органическими веществами по сравнению с реакциями, характерными для неорганических веществ, образованием побочных продуктов, спецификой выделения получающихся веществ и технологическим оборудованием.
5. Огромным практическим значением органических соединений. Они - наша пища и одежда, топливо, разнообразные лекарственные препараты, многочисленные полимерные материалы и т.д.
Классификация органических соединений
Огромное количество органических соединений классифицируют с учетом строения углеродной цепи (углеродного скелета) и наличия в молекуле функциональных групп.
На схеме представлена классификация органических соединений в зависимости от строения углеродной цепи.
|
|
Органические соединения |
|
|
|||
|
|
|
|
|
|
|
|
Ациклические (алифатические) (соединения с открытой цепью) |
Циклические (соединения с замкнутой цепью) |
||||||
|
|
|
|
|
|
|
|
Насыщенные (предельные) |
Ненасыщенные (непредельные) |
К |
Гетероциклические (цикл состоит из атомов углерода и других элементов) |
||||
|
|
|
|
|
|
|
|
|
|
|
Алициклические (алифатические циклические) |
Ароматические |
|
||
Простейшими представителями ациклических соединений являются алифатические углеводороды - соединения, содержащие только атомы углерода и водорода. Алифатические углеводороды могут быть насыщенными (алканы) и ненасыщенными (алкены, алкадиены, алкины).
Простейшим представителем алициклических углеводородов служит циклопропан, содержащий цикл из трех углеродных атомов.
Ароматический ряд объединяет ароматические углеводороды - бензол, нафталин, антрацен и т.д., а также их производные.
Гетероциклические соединения могут содержать в цикле, кроме атомов углерода, один или несколько атомов других элементов - гетероатомов (кислород, азот, серу и др.).
В каждом представленном ряду органические соединения делятся на классы в зависимости от состава и строения. Наиболее простым классом органических соединений являются углеводороды. При замене атомов водорода в углеводородах на другие атомы или группы атомов (функциональные группы) образуются другие классы органических соединений данного ряда.
Функциональная группа - атом или группа атомов, устанавливающие принадлежность соединения к классам органических соединений и определяющие главнейшие направления его химических превращений.
Соединения с одной функциональной группой называются монофункциональными (метанол СН3–ОН), с несколькими одинаковыми функциональными группами - полифункциональными (глицерин
СН2– I OH |
СН– I OH |
СН2), I OH |
с несколькими разными функциональными группами - гетерофункциональными (молочная кислота
СН3– |
СН–СООН). I OH |
Соединения каждого класса составляют гомологические ряды. Гомологический ряд – это бесконечный ряд органических соединений, имеющих сходное строение и, следовательно, сходные химические свойства и отличающихся друг от друга на любое число СН2– групп (гомологическая разность).
Основные классы органических соединений следующие:
I. Углеводороды (R–H).
II. Галогенопроизводные (R–Hlg).
III. Спирты (R–OH).
O // IV. Эфиры простые и сложные (R–O–R’, R–C ). \ OR |
O // V.Карбонильные соединения (альдегиды и кетоны) (R–C , \ H |
O || R–C–R). |
O // VI. Карбоновые кислоты R–C ). \ OH |
R | VII. Амины (R–NH2, NH, R–N–R’). | | . R’ R’’ |
VIII. Нитросоединения (R–NO2).
IX. Сульфокислоты (R–SO3H).
Число известных классов органических соединений не ограничивается перечисленными, оно велико и с развитием науки все время увеличивается.
Все классы органических соединений взаимосвязаны. Переход от одних классов соединений к другим осуществляется в основном за счет превращений функциональных групп без изменения углеродного скелета.
Значение органической химии
Органическая химия имеет исключительно важное познавательное и народнохозяйственное значение.
Природные органические вещества и их превращения лежат в основе явлений Жизни. Поэтому органическая химия является химическим фундаментом биологической химии и молекулярной биологии - наук, изучающих процессы, происходящие в клетках организмов на молекулярном уровне. Исследования в этой области позволяют глубже понять суть явлений живой природы.
Множество синтетических органических соединений производится промышленностью для использования в самых разных отраслях человеческой деятельности. Это - нефтепродукты, горючее для различных двигателей, полимерные материалы (каучуки, пластмассы, волокна, пленки, лаки, клеи и т.д.), поверхностно-активные вещества, красители, средства защиты растений, лекарственные препараты, вкусовые и парфюмерные вещества и т.п. Без знания основ органической химии современный человек не способен экологически грамотно использовать все эти продукты цивилизации.
Сырьевыми источниками органических соединений служат: нефть и природный газ, каменный и бурый угли, горючие сланцы, торф, продукты сельского и лесного хозяйства.
АЛКАНЫ (предельные углеводороды, парафины)
Алканы – алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи.
Алканы – название предельных углеводородов по международной номенклатуре. Парафины– исторически сложившееся название, отражающее свойства этих соединений (от лат. parrum affinis – имеющий мало сродства, малоактивный). Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода.
Простейшие представители алканов:
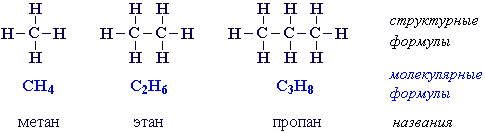
Модели молекул:
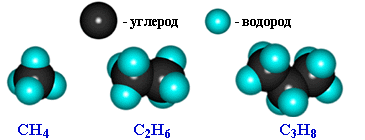
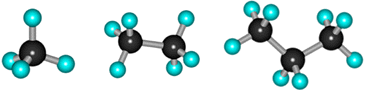
При сравнении этих соединений видно, что они отличаются друг от друга на группу -СН2- (метилен). Добавляя к пропану еще одну группу -СН2-, получим бутан С4Н10, затем алканы С5Н12, С6Н14 и т.д.
Алканы — углеводороды, состав которых выражается общей формулой CnH2n+2, где n – число атомов углерода.
Реакция замещения (галогенирование)
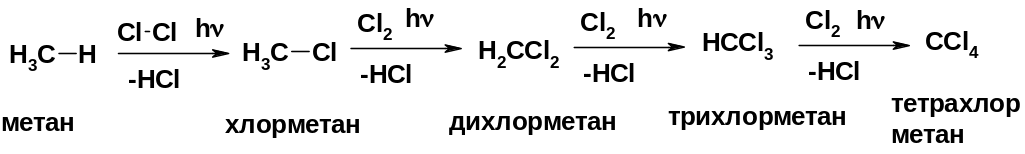
Механизм реакции
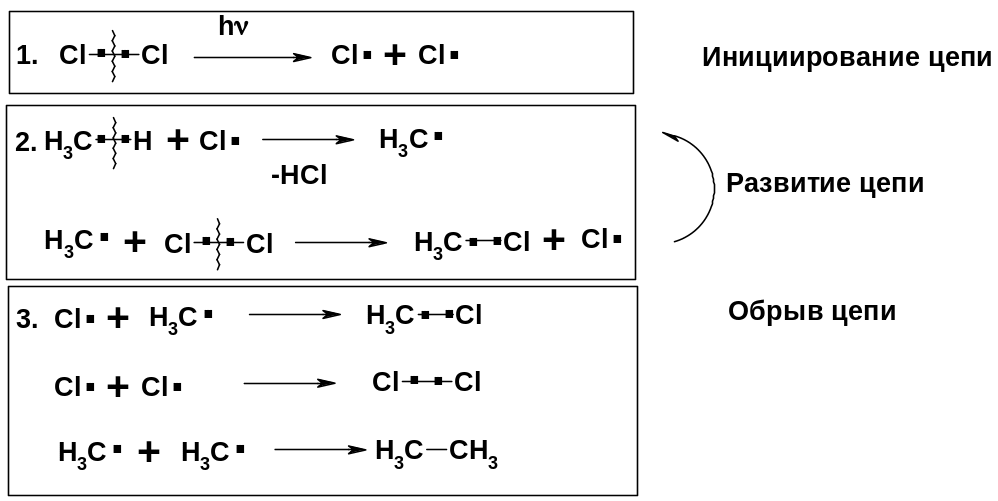
Сульфохлорирование

Cульфоокисление

Нитрование

Горение

Управляемое окисление

Циклоалканы CnH2n

Получение
Внутримолекулярная реакция Вюрца
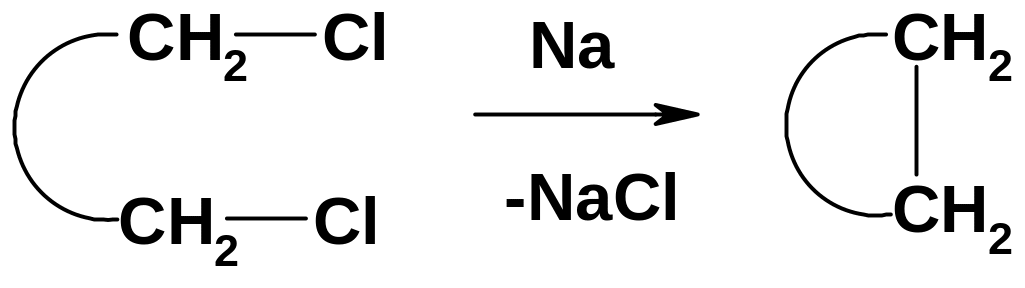

Хим. свойства см. алканы
Реакции присоединения (для напряженных циклов С3-С4)
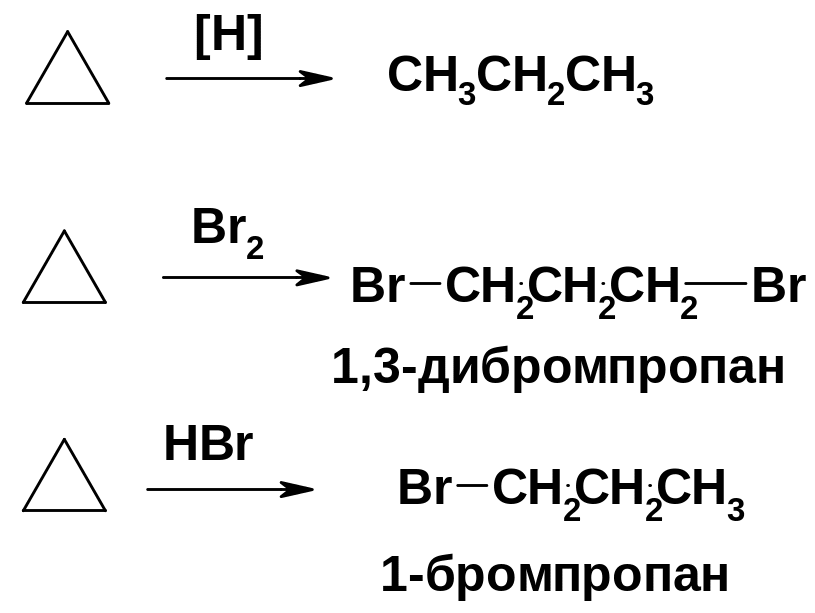
ЛЕКЦИЯ 5.
АЛКЕНЫ
СnH2n ненасыщенные углеводороды с двойной связью
Номенклатура -
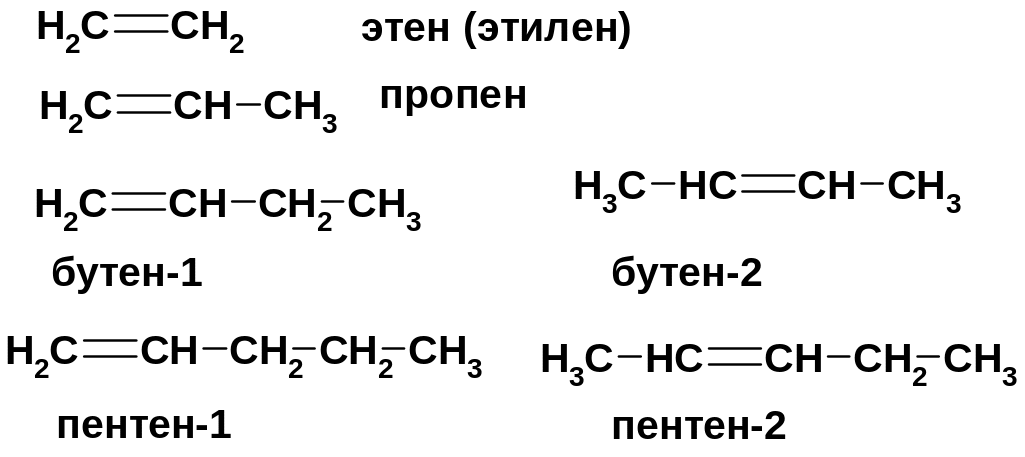
Двойная связь
sp2-гибридизация

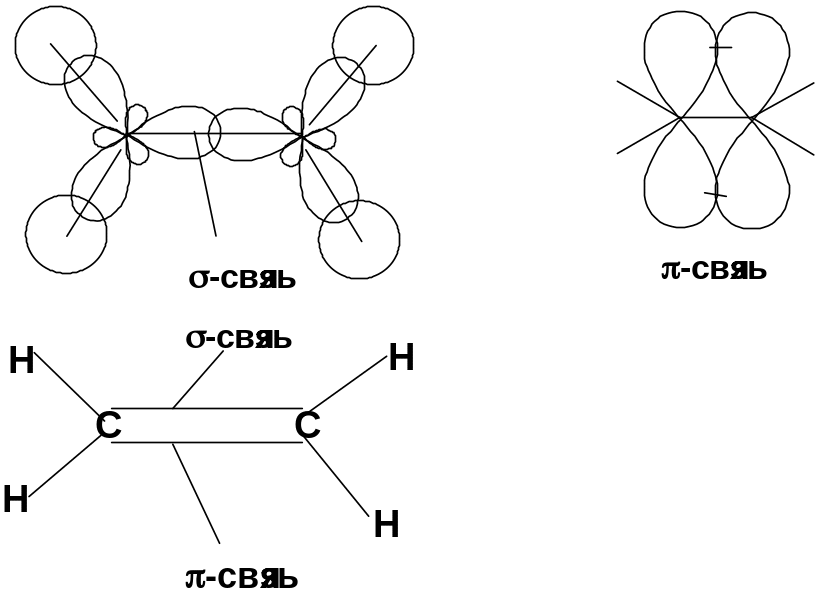
Пространственная изомерия относительно двойной связи

Способы получения
1. Дегидратация спиртов

2.Дегидрогалагенирование галогеналканов

3.Дегалагенирование 1,2-дигалогеналканов

4.Дегидрирование алканов

Химические свойства
Реакция присоединения
1. Гидрирование
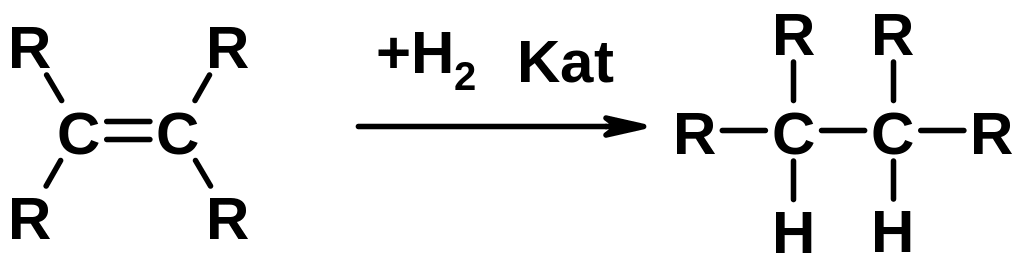
2. Присоединение галогеноводорода
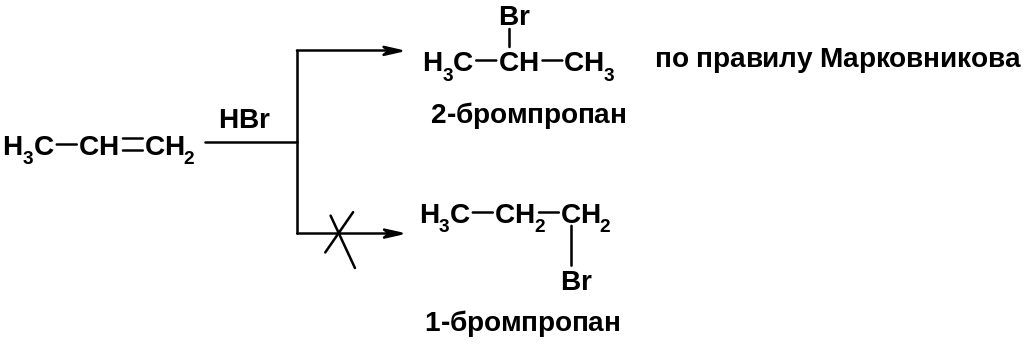
3. Гидратация

4. Окисление KMnO4

5. Озонолиз

Алкадиены

Классификация диенов

Особенности хим. свойства сопряженных диенов, по сравнению с алкенами
Присоединение
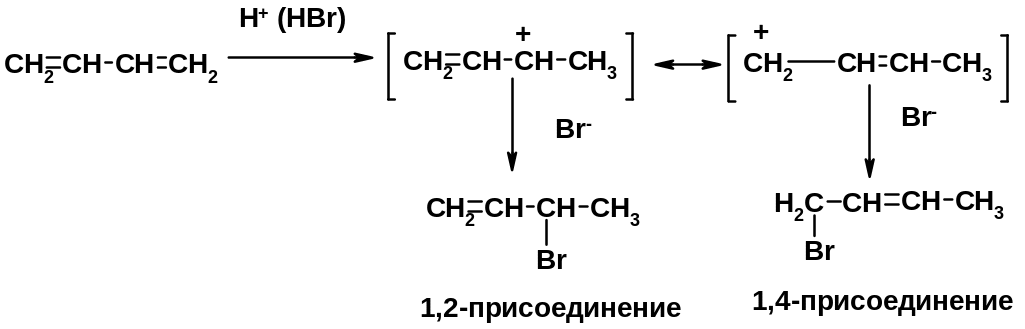
Диеновый синтез (реакция Дильса-Альдера)
 Из
3 p-связей
образуется новые 1 p-
и 2 s-связи
Из
3 p-связей
образуется новые 1 p-
и 2 s-связи
АЛКИНЫ

sp-гибридизация углерода при тройной связи

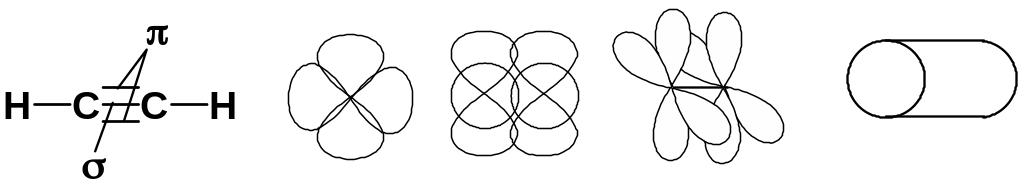
Методы получения
1.
![]()
2. Дегидрогалогенирование 1,1- и 1,2-дигалогеналканов
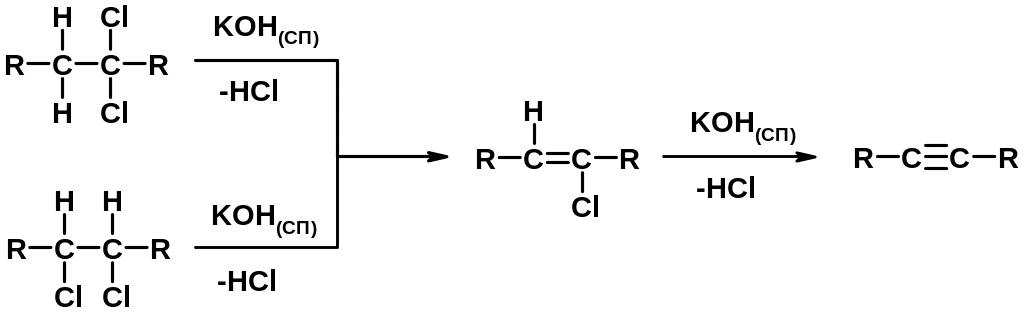
Химические свойства
1. Гидрирование

2. Галогенирование

3. Гидрогалогенирование
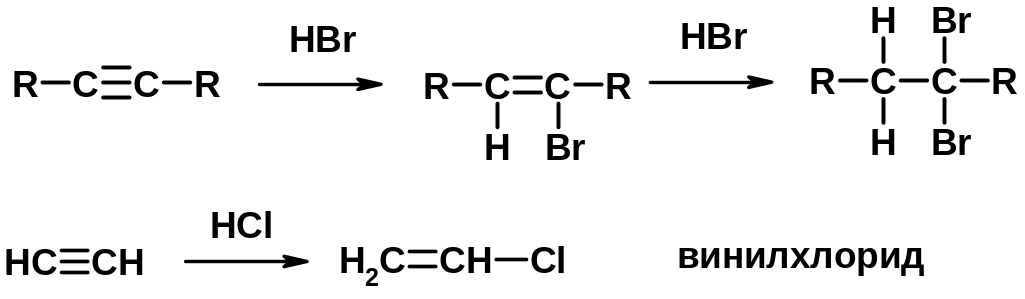
4. Винилирование

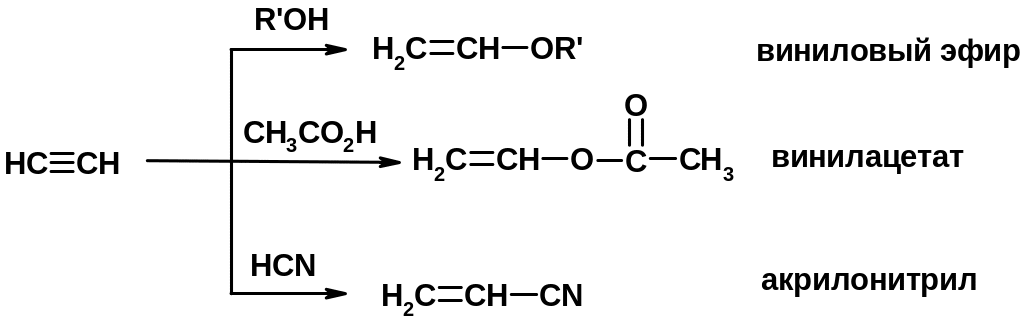
5. Кислотность алкинов с концевой тройной связью
 Соли алкинов – ацетилениды
Соли алкинов – ацетилениды
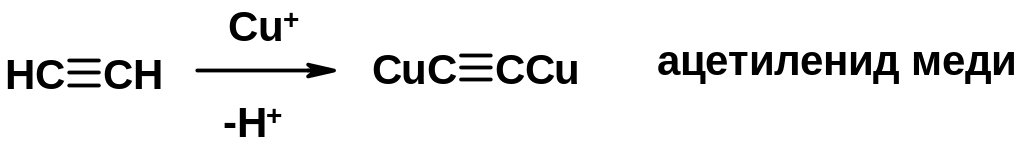
6. Циклизация
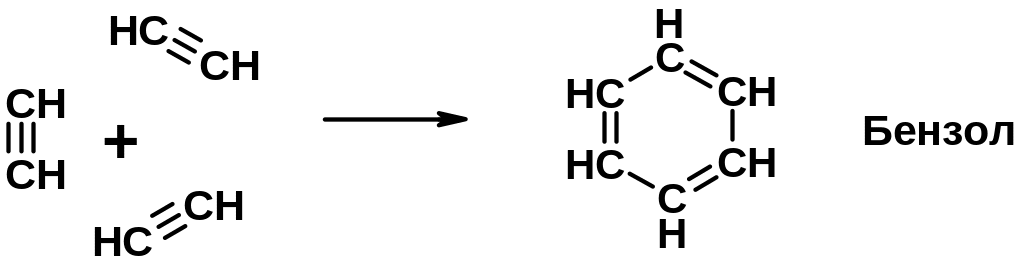
Ароматические углеводороды (арены)


Углерод в ароматическом ядре – sp2-гибридизован
Принцип ароматичности – принцип Хюккеля
Замкнутая циклическая система сопряженных p-электронов
Количество p-электронов – 4n+2 (n = 0, 1, 2...)
С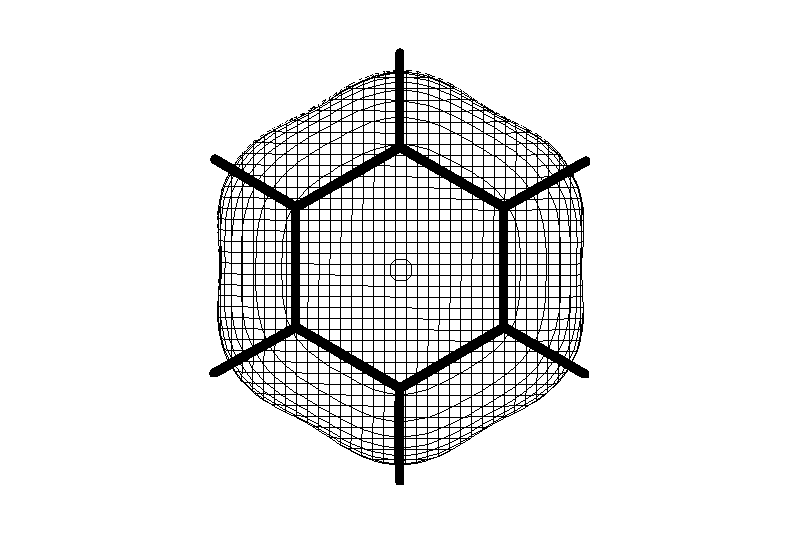
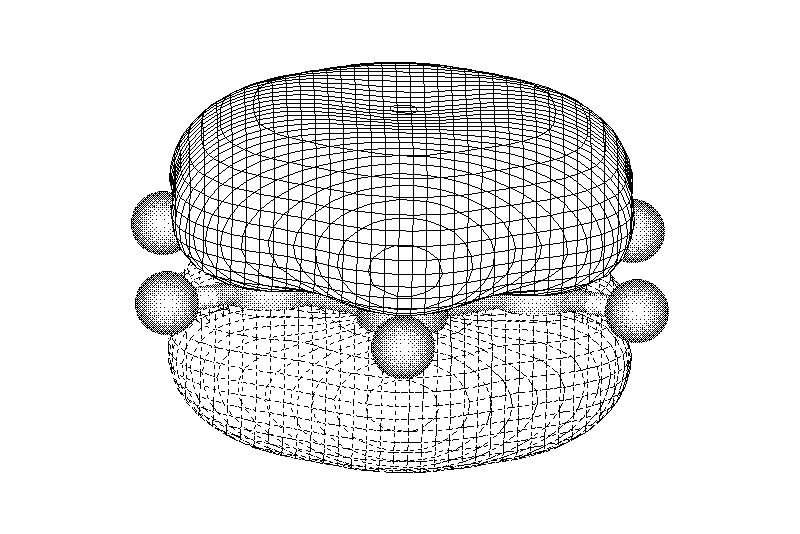
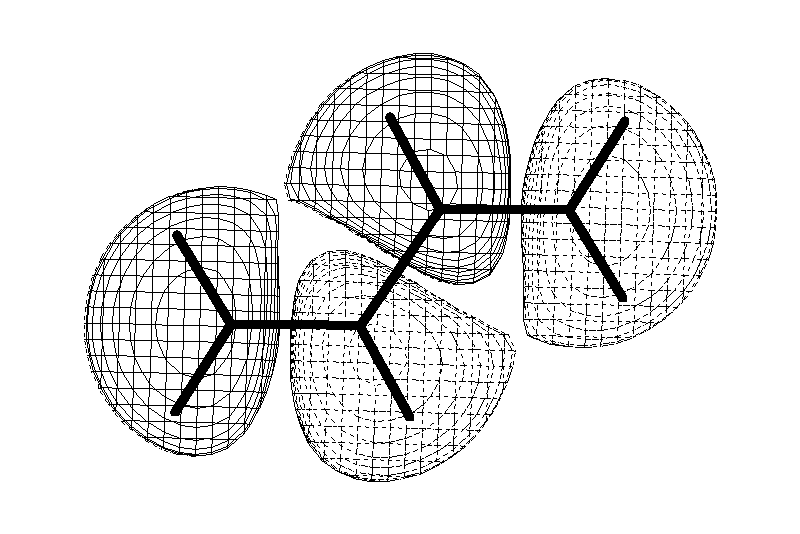
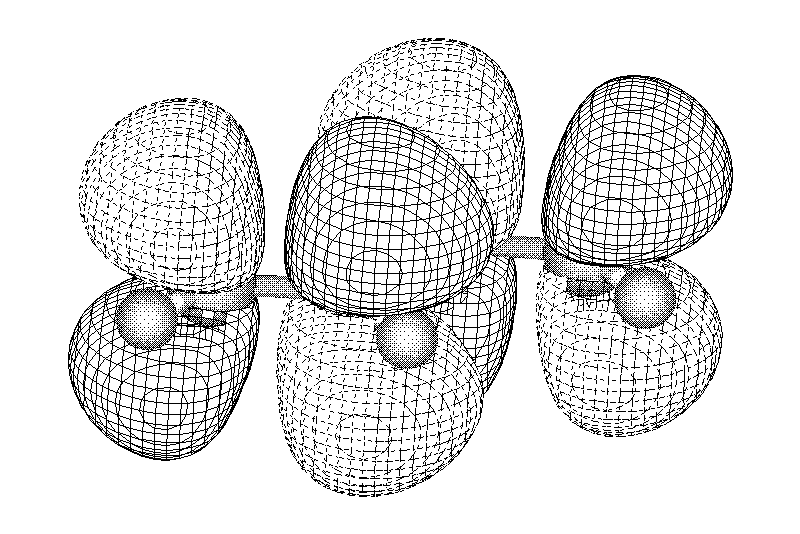
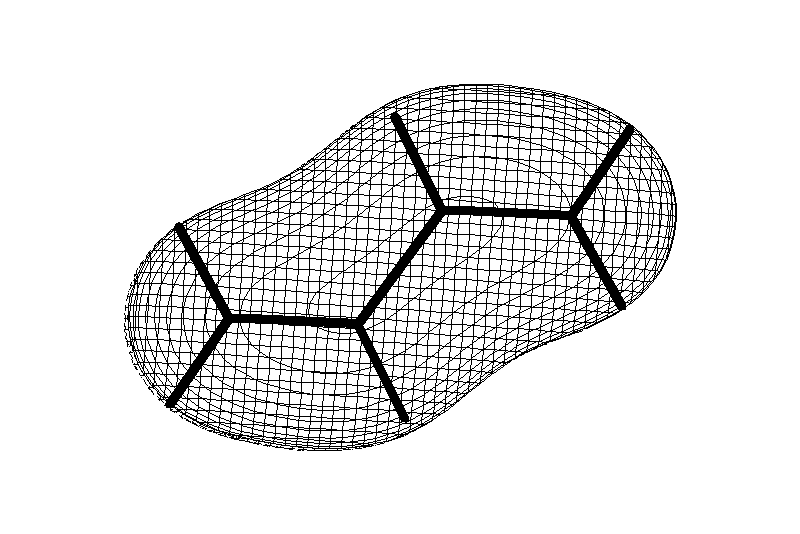
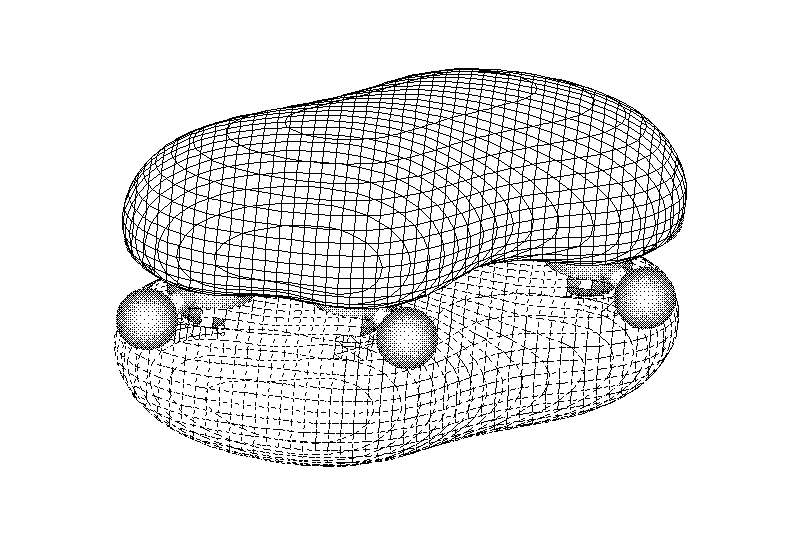
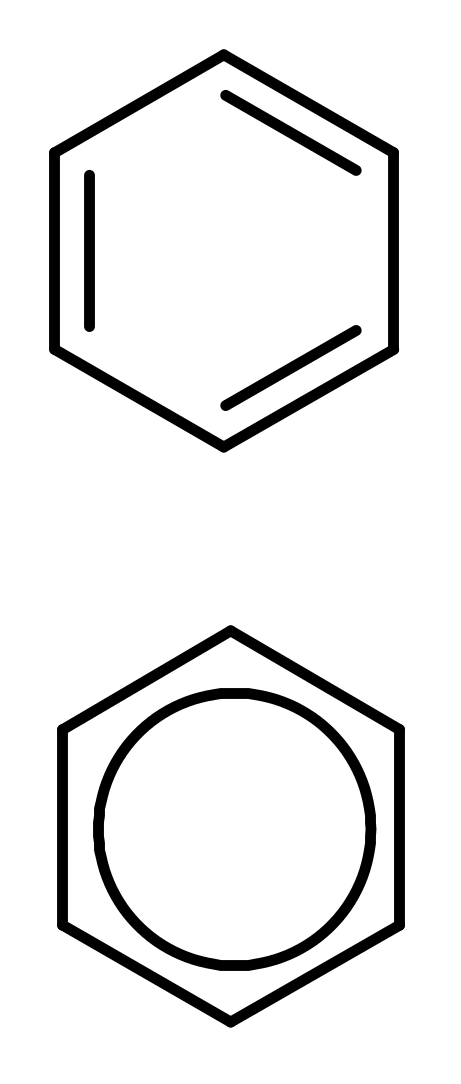
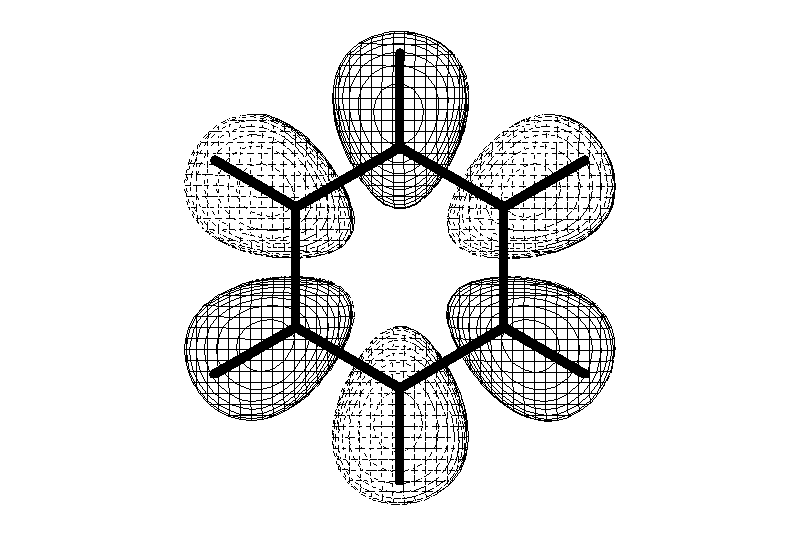
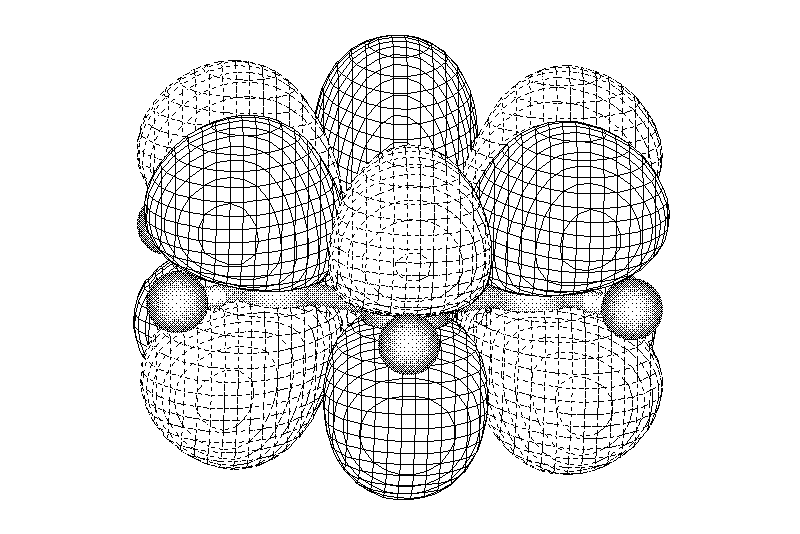 опряжение
опряжение

Химические свойства
Электрофилы (Е+) – акцепторы электронной плотности
E+ = R+ (H3C+) – карбокатионы, NO2+, Br+, SO3, и др.
Нуклеофилы (Nu-) – доноры электронной плотности
Nu- = R- (H3C-) – карбанион, ОН-, RO-, NH2-, Br-, HOH, RNH2 и др.
Электрофильное ароматическое замещение SEAr
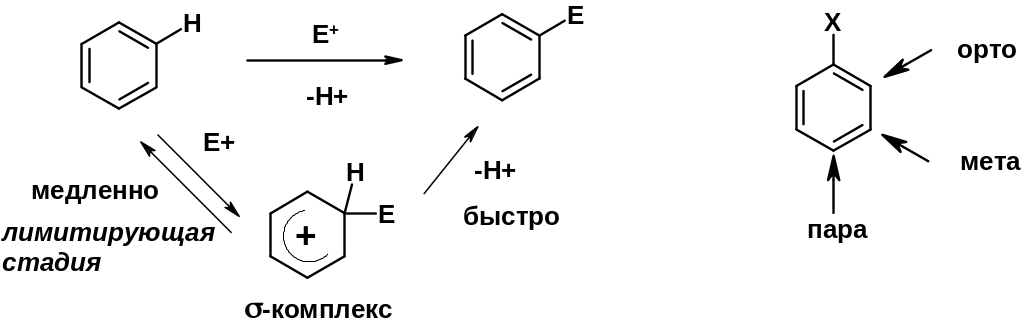
Влияние заместителей в бензольном кольце на реакцию SEAr
Электронные эффекты заместителей
Индуктивный эффект (I – эффект) – изменение распределения электронной плотности в молекуле из=за разницы электроотрицательности атомов.

Мезомерный эффект (М – эффект) – возникает в сопряженных системах (заместитель связан с sp2- или sp-гибридизованным углеродом)
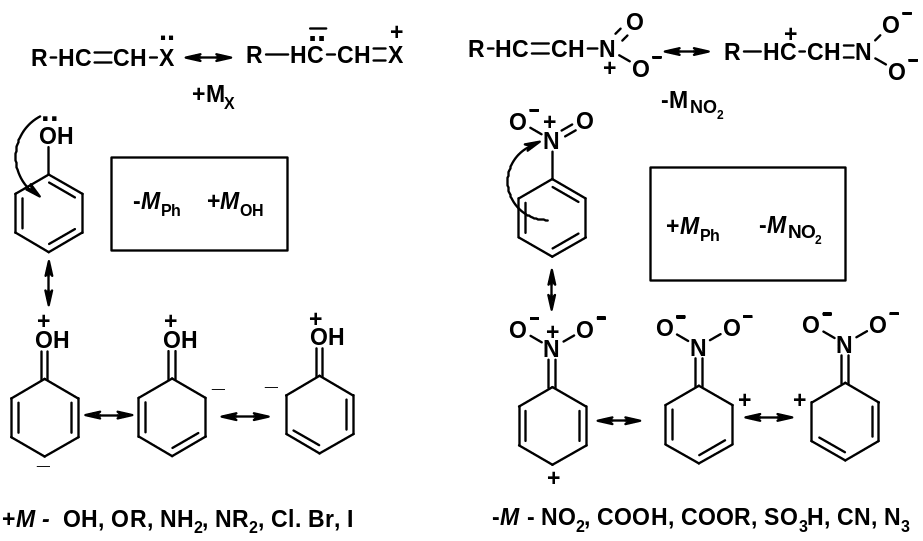
Заместители I рода – направляют реакцию в орто- и пара-положение
СН3 (R), OH, OR, NH2, NR2 (ускоряют реакцию), Cl, Br, I (замедляют)
+I или +М -I, но +M

Заместители II рода – направляют реакцию в мета-положение и замедляют реакцию
NO2, NO, СООН, COOR, SO3H, CN, N3, CСl3
-M и/или -I

1. Хлорирование

2. Нитрование

3. Сульфирование

4. Алкилирование по Фриделю-Крафтсу
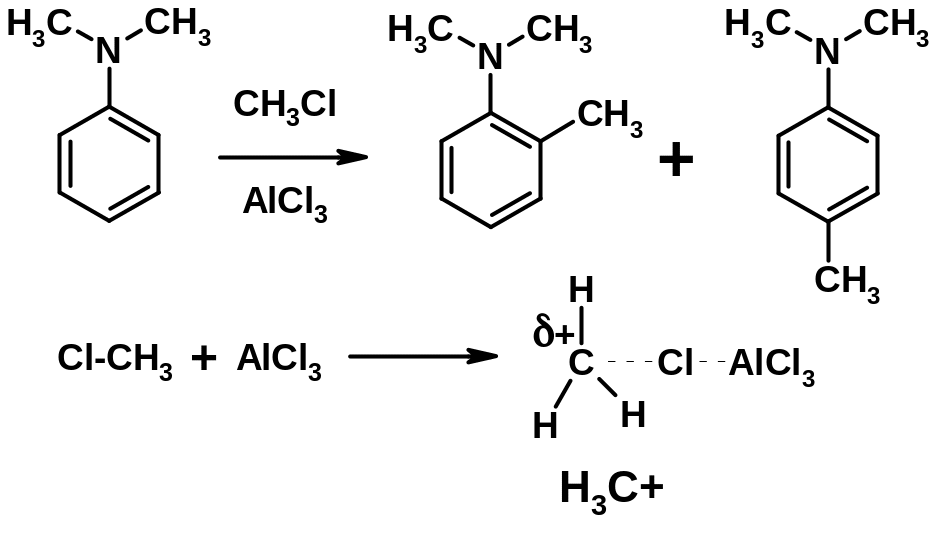
5. Ацилирование по Фриделю-Крафтсу
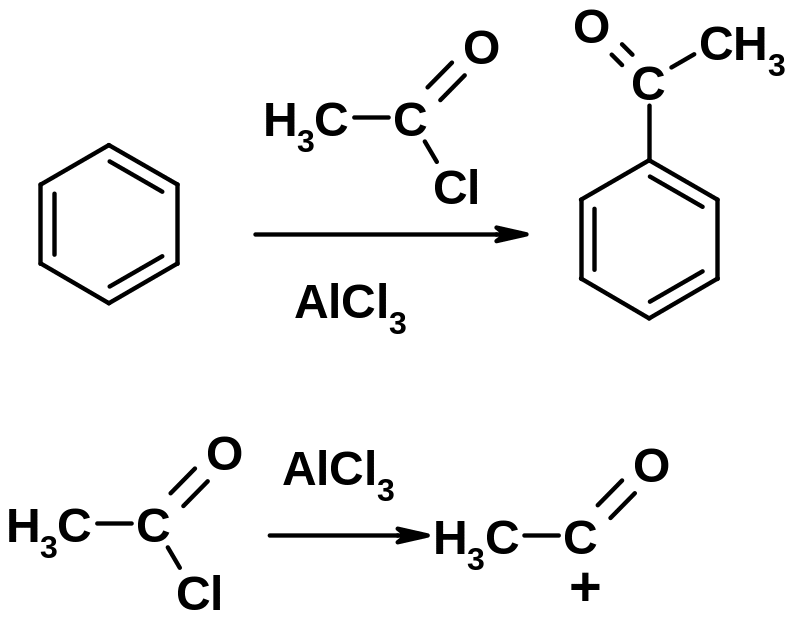
Согласованная ориентация

ЛЕКЦИЯ 6. СПИРТЫ и ФЕНОЛЫ
(ОН – гидроксил или гидрокси-группа)
(приставка для обозначения гидроксила – гидрокси, суффикс – ол)

Методы получения
Получение спиртов
1. Гидратация алкенов (см. алкены)
2. Замещение галогена на гидроксил (OH) (см. галогенуглеводороды)
3. Восстановление карбоновых кислот
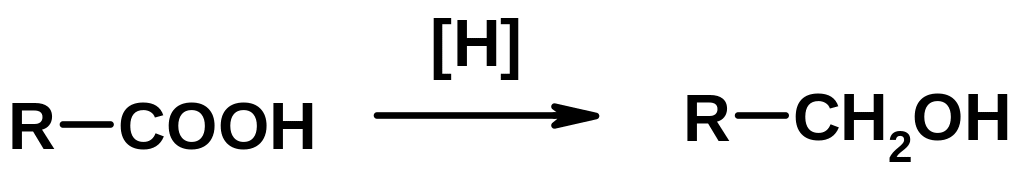
Получение фенолов
1. Кумольный метод получения фенола в промышленности

2. Сплавление сульфокислот с щелочами
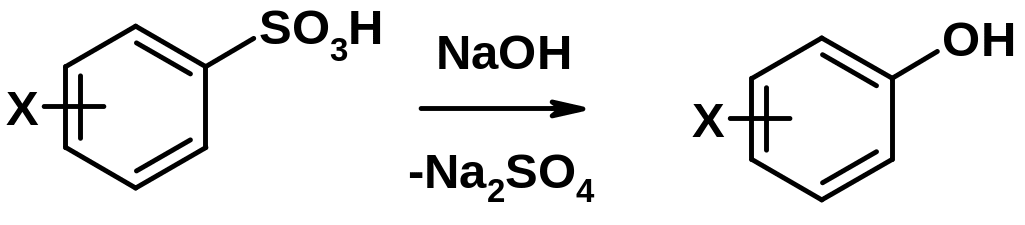
Химические свойства
1. Кислотность (способность отдавать протон)
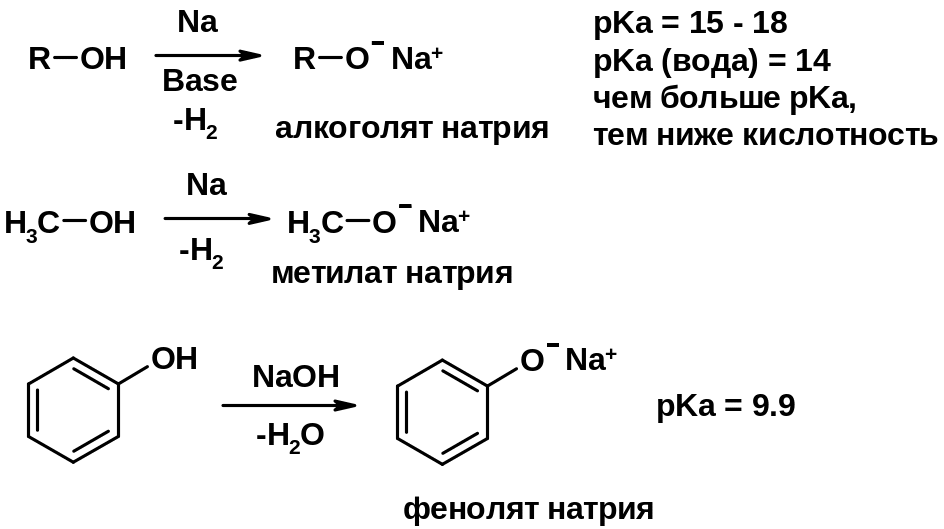
Кислотность фенолов выше, чем алифатических спиртов
Кислотность тем выше, чем выше стабильность образующегося аниона
Стабильность заряженной частицы тем выше, чем выше делокализация заряда







 арбоциклические
(цикл состоит только из атомов углерода)
арбоциклические
(цикл состоит только из атомов углерода)