
- •1.Основные понятия коллоидной химии; классификация, основные особенности, количественные характеристики дисперсных систем.
- •2. Диспергационные методы получения дисперсных систем
- •3. Конденсационные методы получения дисперсных систем
- •4. Закон Эйнштейна-Смолуховского, броуновское движение.
- •5. Первый и второй законы Фика, диффузия, движущая сила диффузии, связь коэффициента диффузии с размерами частиц
- •6. Гипсометрический закон Лапласа, диффузионно-седиментационное равновесие. Кривая седиментации для монодисперсных и полидисперсных систем.
- •7. Строение двойного электрического слоя (фи-потенциал и дзета-потенциал), теория Квинке-Гельмгольца-Перрена, теория Гуи-Чепмена, теория Штерна, строение мицеллы.
- •8. Рассеяние света. Опалесценция. Эффект Тиндаля.
- •9. Закон Бугера-Ламберта-Бера, оптические свойства коллоидных растворов, оптические методы анализа дисперсности.
- •10. Работа когезии. Связь поверхностной энергии с взаимодействиями между молекулами (атомами, ионами), правило Трутона, уравнение Дюпре. .
- •12. Закон Лапласа: общая форма, частные случаи, капиллярное поднятие жидкости, уравнение Жюрена.
- •13. Томсона (Кельвина), зависимость давления насыщенного пара от кривизны поверхности жидкости, капиллярная конденсация.
- •14. Закон Гиббса-Оствальда-Фрейндлиха, влияние дисперсности на растворимость твердых частиц, процессы изотермической перегонки в дисперсных системах.
- •15. Лиофильные коллоидные системы, методы получения. Самопроизвольное диспергирование макрофаз: критерий самопроизвольного диспергирования (по Ребиндеру-Щукину, примеры).
- •16. Мицеллообразование в водных растворах пав. Критическая концентрация мицеллообразования (ккм), основные методы определения ккм
- •17. Солюбилизация
- •18. Термодинамика мицеллообразования, диаграмма фазовых состояний, точка Крафта, жидкокристаллические системы.
- •19. Образование и строение обратных мицелл
- •20. Аэрозоли. Молекулярно-кинетические свойства. Седиментация
- •21. Термопреципитация
- •22. Фотофорез
- •23. Термофорез.
- •24. Коалесценция.
- •25. Быстрая и медленная коагуляция.
- •26. Концентрационная и нейтрализационная коагуляция
- •27. Изотермическая перегонка.
- •28. Пены, классификация и строение, разрушение пен и практическое применение.
- •29. Эффект Марангони.
- •30. Тиксотропия.
- •31. Флотация.
- •32. Эмульсии. Обращение фаз, разрушение эмульсий и практическое применение.
- •33. Правило Банкрофта
- •34. Правило Дюкло-Траубе
- •35. Правило Шульца-Гарди.
- •36.Критерий Эйлера-Корфа.
- •37. Теория длфо.
- •38. Слои Шиллера
- •39. Тактоиды
- •40. Биконтинуальные дисперсные системы
- •41. Кольца и слои Лизеганга
- •42. Пептизация.
- •43. Флокуляция
- •44. Гетерокоагуляция.
- •45. Адагуляция.
- •46. Аддитивность коагуляции.
- •47. Антагонизм коагуляции
- •48. Синергизм коагуляции
- •49. Коагуляционные структуры
- •50. Структуры с фазовыми контактами
- •51. Синерезис.
- •52. Конденсационные структуры
- •53. Кристаллизационные структуры
- •54. Когезия.
- •55. Адгезия
- •56. Физико-химические методы регулирования структурно-механических свойств дисперсных систем.
- •57. Смачивание.
- •58. Капиллярное давление
- •59. Закон Ньютона (трение)
- •60. Диссипация энергии
- •61. Застудневание
- •62.Ползучесть
- •63. Вязкость коллоидных растворов. Зависимость вязкости раствора от концентрации взвешенных частиц (уравнение Эйнштейна)
- •64.Аномалия вязкости коллоидных систем. Причины, которые вызывают аномалии вязкости
- •65. Как образуется снежинка
- •66. Хемосорбция и каталитическая сорбция, сходства и отличия, привести примеры
- •67. Почему “химические дожди” выпадают недалеко от источника загрязнения?
- •68. Адсорбция
- •69. Абсорция.
- •70. Хемосорбция.
- •71. Каталитическая сорбция
- •72. Обеспечивает вертикальную устойчивость облаков?
- •73. В чём сходство и различие газовой и жидкой дисперсионных сред?
- •74. Почему туман в вечернее время распространяется в приземном слое, не оседая на поверхность?
- •75. Почему снег выпадает иногда в виде “крупы”?
- •76. Почему иней в большей степени образуется на открытых участках, чем в лесу?
- •77. Адсорбция и адагуляция, сходства и отличия, привести примеры
- •78. Количественные характеристики дисперсных систем
- •78. Количественные характеристики дисперсных систем.
- •79. Классификация дисперсных систем по размеру частиц дисперсной фазы ( отличительные особенности частиц разных размеров)
- •80. Классификация дисперсных систем по фракционному составу частиц.
- •81. Классификация дисперсных систем по концентрации частиц.
- •82. Классификация дисперсных систем по характеру взаимодействий дисперсной фазы с дисперсной средой.
- •83. Классификация дисперсных систем по характеру распределения фаз.
- •84. Классификация дисперсных систем по агрегатному состоянию дисперсной фазы и дисперсной среды.
- •85. Классификация дисперсных частиц по размерам.
- •86. Классификация дисперсных частиц по форме
- •87. Классификация дисперсных частиц по строению.
- •88. Классификация дисперсных частиц по химическому составу.
- •89. Размерные эффекты, наблюдаемые в дисперсных системах.
- •90. Термодинамические свойства дисперсных частиц.
- •91. Механические свойства дисперсных частиц.
- •92. Магнитные свойства дисперсных частиц.
- •93. Каталитические свойства дисперсных частиц.
- •94. Энергетическое и силовое определение поверхностного натяжения.
- •95. Факторы, влияющие на поверхностное натяжение жидкостей.
- •96. Дисперсионная и полярная составляющая поверхностного натяжения жидкостей.
- •97. Метод избыточных величин Гиббса.
- •98. Капиллярное давление (определение, физический смысл, от чего зависит)
- •99. Несмачивание, полное смачивание, гидрофильность и гидрофобность.
- •100. Правило Антонова.
- •101. Эффект Марангони
- •102. Зависимость смачиваемости от свойств твердой поверхности
- •103. Смачивание нанокаплями
- •104. Адгезия, когезия, уравнение Дюпре.
- •105. Изотермическая перегонка
- •106. Перекристаллизация
- •107. Капиллярная конденсация
- •108. Закон Жюрена. (высота подъема жидкости в капиллярных трубках)
- •109. Измерение поверхностного натяжения методом капиллярного подъема.
- •110. Измерение поверхностного натяжения методом сидящей капли.
- •111. Измерение поверхностного натяжения методом максимального давления.
- •112.Измерение поверхностного натяжения методом пластинки Вильгельми.
- •113. Измерение поверхностного натяжения методом вращающейся капли.
- •114. Измерение поверхностной энергии твердых тел
- •115. Адсорбция пав на поверхности раздела жидких фаз.
- •116. Адсорбция пав из растворов на поверхности твердых тел.
- •117. Химическое модифицирование твердых тел.
- •118. Классификация пав по растворимости.
- •119. Классификация пав по диссоциации в воде.
- •120. Классификация пав по происхождению и по способности к образованию мицелл.
- •121. Классификация пав по физико-химическому воздействию на поверхность раздела между фазами.
- •122. Гидрофильно-липофильный баланс.
- •123. Критический параметр упаковки
- •125. Строение дэс
- •126. Влияние электролитов на дэс.
- •127. Электрофорез.
- •128. Электроосмос.
- •129. Потенциал течения.
- •130. Потенциал оседания.
- •131. Электрокапиллярные явления. (Электрокапилярная кривая, уравнение Липпмана)
5. Первый и второй законы Фика, диффузия, движущая сила диффузии, связь коэффициента диффузии с размерами частиц
Диффузией называют самопроизвольно протекающий в системе процесс выравнивания концентрации молекул, ионов или коллоидных частиц под влиянием их теплового хаотического движения; макроскопическое проявление теплового движения молекул, всегда идет тем быстрее, чем выше температура. Явление диффузии необратимо. Колличественный процесс диффузии описывается законом Фика: скорость процесса диффузии в ДС прямо пропорциональна площади, через которую осуществляется диффузия и градиенту концентрации диффундиующего вещества первый закон Фика :
 m
– количество продиффундировавшего
вещества
D
– коэффициент диффузии, зависящий от
свойств диффундирующих частиц и
среды
dc/dx
– градиент концентрации –движущая
сила диффузии
S
– площадь, через которую идет диффузия
dT
– продолжительность диффузии
Второй
закон Фика связывает пространственное
и временное изменения концентрации:
m
– количество продиффундировавшего
вещества
D
– коэффициент диффузии, зависящий от
свойств диффундирующих частиц и
среды
dc/dx
– градиент концентрации –движущая
сила диффузии
S
– площадь, через которую идет диффузия
dT
– продолжительность диффузии
Второй
закон Фика связывает пространственное
и временное изменения концентрации:
![]()
Коэффициент диффузии(D) – масса вещества диффундирующего через ед. площади(1м2) за ед. времени (1с) при ед. градиенте концентрации. Энштейн установил связь КД с параметрами Д системы: D = (RT)/(6П r ДФ η ДСNA)
ПРИМЕРЫ:Распространение запахов, смешивание разнородных жидкостей, растворение твердых тел в жидкостях, сварка металлов при их расплавлении или под давлением.
5. закона Фика в форме принимают в качестве кинематической характеристики скорость фильтрации.
6.Проникновение растворённого вещества в клетку может быть выражено законом Фика, в котором значение коэффициента Диффузии заменено коэффициентом проницаемости мембраны, а градиент концентрации — разностью концентраций вещества по обе стороны мембраны.
7, Диффузионное проникновение в клетку газов и воды (Осмос) также описывается законом Фика; при этом значения разности концентраций заменяются значениями разности давлений газов и осмотических давлений внутри и вне клетки.
Примеры:Д. кислорода из лёгких в кровь и из крови в ткани, всасывание продуктов пищеварения из кишечника, поглощение элементов минерального питания клетками корневых волосков, Д. ионов при генерировании биоэлектрических импульсов нервными и мышечными клетками).
8, Различная скорость Д. ионов через клеточные мембраны — один из физических факторов, влияющих на избирательное накопление элементов в клетках организма.
6. Гипсометрический закон Лапласа, диффузионно-седиментационное равновесие. Кривая седиментации для монодисперсных и полидисперсных систем.
Суспензия (ж,т)
была получена равномерным перемешиванием
вещества в ТВ.ф. в Vд.с.(жидкой)
в результате чего вещества д.ф.равномерно
распределились с начальной концентрацией
 Седиментационная
скорость направлена вниз.
Седиментационная
скорость направлена вниз.
После прекращения
перемешивания в системе начинается
процесс седиментации, который нарушает
начальное распределение частиц д.ф. по
Vд.с.
В результате возникает градиент
концентраций частиц д.ф. в верхней и
нижней областях цилиндра. По мере
развития процесса седиментации градиент
будет расти.

Из-за возникшего градиента концентрации начинает развиваться процесс диффузии причём диффузионный поток направлен от большей частичной концентрации(низ) к меньшей частичной концентрации(верх)скорость диффузии направлена вверх.
При выравнивании скоростей седиментации и диффузии в д.сист. устанавливается седиментационно-диффузионное равновесие, при котором частицы д.ф.не равномерно распределены по высоте сосуда. Если на д.сист. находящуюся в состоянии этого равновесия не оказывать воздействия, частицы д.ф. останутся на своём месте без оседания сколь угодно долго!
Количественной оценкой с-д равновесия ф-ла Лапласа, которая имеет вид

Которая показывает на какой высоте в данной д.сист. устанавливается равновесие для частиц радиусом r.
 - концентрация
частиц в единице объёма на высоте h
от дна сосуда.
- концентрация
частиц в единице объёма на высоте h
от дна сосуда.
Анализ формулы позволяет сделать вывод:
Между высотой и частичной концентрацией на данной высоте, существует обратно пропорциональная зависимость.
Эмульсии (жидкая – д.ф. и жидкая д.ср.)
В эмульсиях
соотношение между h
и
обратное по отношению к суспензиям
из-за отрицательного знака в скобке
 .
.
Связь между высотой и размером частиц обратно пропорциональна.
Гипсометрическая формула Лапласа широко используется для экспериментального установления распределения частичной концентрации как функции от высоты.

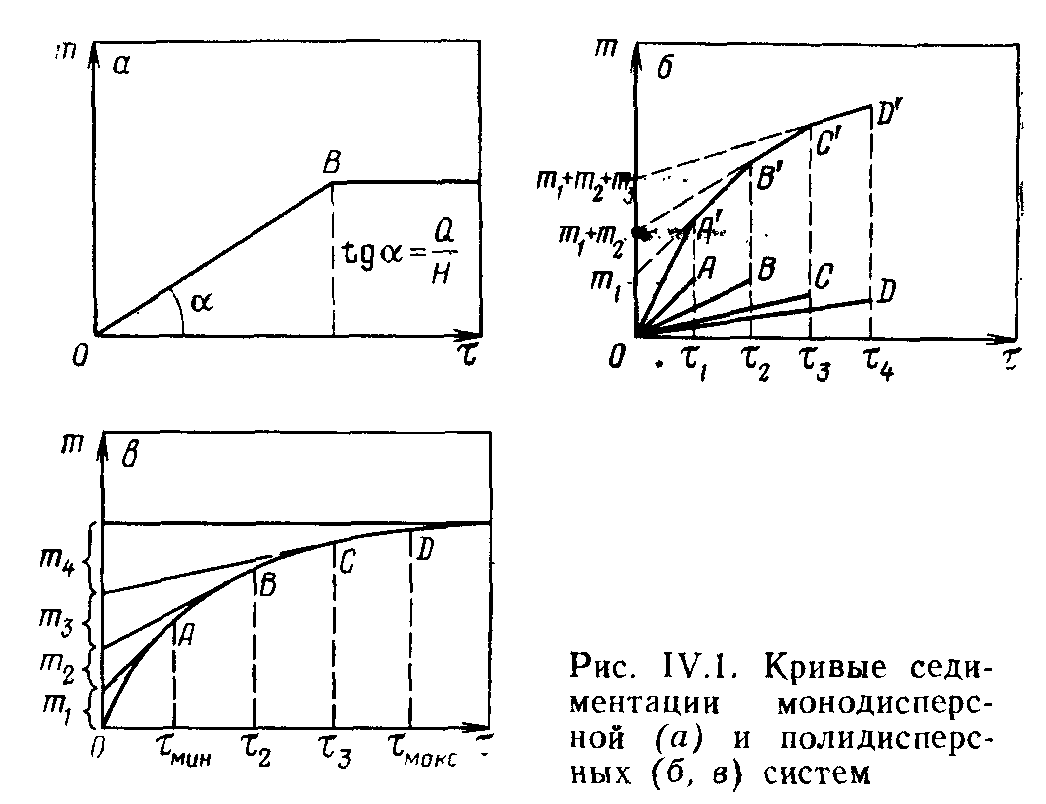
Процесс седиментации монодисперсной системы графически выражается прямой (см. рис. IV.1). Для полидисперсной системы осаждение каждой фракции описывается отдельными прямыми, представленными на рисунке IV.1б: ОА, ОВ, ОС и OD. Чем меньше размер частицы, тем меньше наклон прямой
